
科目: 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:选择题
制备(NH4)2Fe(SO4)2·6H2O的实验中,需对过滤出产品的母液(pH<1)进行处理。常温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
A.通入过量Cl2:Fe2+、H+、NH4+、Cl-、SO42-
B.加入少量NaClO溶液:NH4+、Fe2+、H+、SO42-、ClO-
C.加入过量NaOH溶液:Na+、Fe2+、NH4+、SO42-、OH-
D.加入过量NaClO和NaOH的混合溶液:Na+、SO42-、Cl-、ClO-、OH-
查看答案和解析>>
科目: 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:选择题
有关能量的判断或表示方法正确的是 ( )
A.2H2(g)+O2(g) =2H2O(g)ΔH=—483.6 kJ·mol-1,则H2燃烧热为241.8 kJ·mol-1
B.从C(石墨,s)= C(金刚石,s) ΔH=+1.9 kJ/mol,可知:金刚石比石墨更稳定
C.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多
D.化学反应中的能量变化,通常表现为热量的变化
查看答案和解析>>
科目: 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:选择题
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,在制备乙醛的同时能获得电能,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法不正确的是( )
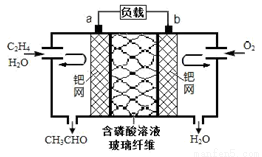
A.该电池可将化学能转化为电能
B.每有0.1mol O2反应,则迁移0.4mol H+
C.正极反应式为:CH2=CH2-2e-+2OH-═CH3CHO+H2O
D.负极区溶液的pH减小
查看答案和解析>>
科目: 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:选择题
已知A、B、C、D均为中学化学常见的纯净物,A是单质,它们有如图反应关系。下列说法错误的是( )
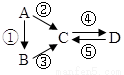
A.若A是大气中含量最多的气体,C、D是氧化物且会造成光化学污染。则D转化成C的反应化学方程为3NO2+H2O=2HNO3+2NO
B.若A、B、C分别为C(s)、CO(g)和CO2(g),且通过与O2(g)反应实现图示的转化。在同温同压且消耗含碳物质均为1mol时,反应①、②、③的焓变依次为△H 1、△H 2、△H 3,则它们之间的关系为 △H 2=△H 1+△H 3
C.若C为一元强碱且阴、阳离子所含的电子数相同,D为日常生活中常用的调味品,工业上用D制备A的化学方程式2Na2O(熔融) 4Na+O2↑
4Na+O2↑
D.若A是应用最广泛的金属。④反应用到A,②、⑤反应均用 到同一种气态非金属单质实验室保存D溶液的方法是加入适量铁粉与适量盐酸
到同一种气态非金属单质实验室保存D溶液的方法是加入适量铁粉与适量盐酸
查看答案和解析>>
科目: 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:选择题
向59.2 g Fe2O3和FeO的混合物中加入某浓度的稀硝酸1.0 L,固体物质完全反应,生成NO和Fe(NO3)3。在所得溶液中加入1.0 mol/L的NaOH溶液2.8 L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为85.6 g。下列有关说法错误的是( )
A.Fe2O3与FeO的物质的量之比为1∶6
B.硝酸的物质的量浓度为3.0 mol/L
C.产生的NO在标准状况下的体积为4.48 L
D.Fe2O3,FeO与硝酸反应后剩余HNO3为0.2 mol
查看答案和解析>>
科目: 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:推断题
A、B、C、D、E是原子序数依次递增的五种常见元素。A、B元素组成的气态化合物M的水溶液呈碱性,C元素是地壳中含量最多的元素,D的单质在C的单质中燃烧后的产物可以使品红溶液褪色,E是金属元素。
(1)写出A、C两种元素组成的化合物A2C2的电子式: ;
(2)A、B、C三种元素可组成一种强酸U,M在适当条件下被U吸收生成一种盐。该盐的水溶液的PH (填大于,小于或等于)7,原因是 ;(用离 子方程式表示)
子方程式表示)
(3)若将E金属投入盐酸中,生成了浅绿色溶液N。则N的酸性溶液与A2C2反应的离子方程式为 ;
(4)R是B的氧化物,通常情况下呈红棕色。现有一试管R,欲使元素B全部转化为它的最高价氧化物对应的水化物,故进行如下实验操作:将盛有R的试管倒扣在水槽中, ;
(5)有人设想寻求合适的催化剂和电极材料,以A2、B2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式: ,放电时,溶液中的H+移向 (填正或负极)
查看答案和解析>>
科目: 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:填空题
HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+.AgNO2是一种难溶于水、易溶于酸的化合物.试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是__________(填序号).
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式: ______________.
(3)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是 __________ (填序号).
a.Cl2b.Fec.H2O2d.HNO3
(4)FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾高铁酸钾(K2FeO4),氧化性比Cl2、O2、ClO2、KMnO4更强,主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应中的氧化剂是 __________ ,还原剂是 __________ .
②简要说明K2FeO4作为水处理剂时所起的作用 __________ .
查看答案和解析>>
科目: 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:实验题
资源的高效利用对保护环境、促进经济持续健康发展具有重要作用。磷尾矿主要含Ca5(PO4)3F和CaCO3·MgCO3 。某研究小组提出了磷尾矿综合利用的研究方案,制备具有重要工业用途的CaCO3、Mg(OH)2、P4和H 2,其简化流程如下:
2,其简化流程如下:
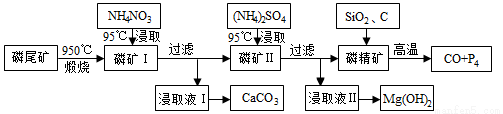
已知:①Ca5(PO4)3F在950℃不分解;
②4Ca5(PO4)3F+18SiO2+30C 2CaF2+30CO+18CaSiO3+3P4
2CaF2+30CO+18CaSiO3+3P4
(1)950℃煅烧磷尾矿生成气体的主要成分是___________。
(2)实验室过滤所需的玻璃仪器是_____________。
 (3)NH4NO3溶液能从磷矿I中浸取出Ca2+的原因是__________。
(3)NH4NO3溶液能从磷矿I中浸取出Ca2+的原因是__________。
(4)在浸取液II中通入NH3,发生反应的化学方程式是____________。
(5)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO( s)+H2SO4(l)=CaSO4(s)+H2O(l) △H=-271kJ/mol
s)+H2SO4(l)=CaSO4(s)+H2O(l) △H=-271kJ/mol
5CaO(s)+H3PO4(l)+HF(g)=Ca5(PO4)3F(s)+5H2O(l) △H=-937kJ/mol
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是_________________。
查看答案和解析>>
科目: 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:实验题
FeCl3在现代工业生产中应用广泛。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。工业上,向500—600℃的铁屑中通入氯气可生产无水氯化铁;向炽热铁屑中通入氯化氢可以生产无水氯化亚铁。
某化学研究性学习小组模拟工业生产流程制备无水FeCl3并对产物做了如下 探究实验,请回答下列问题:
探究实验,请回答下列问题:
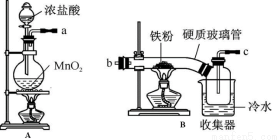

(1)装置的连接顺序为 (用a 、b、c…h表示)。
(2)i.A装置中反应的化学方程式为 。
ii.D中碱石灰的作用是 。
(3)反应结束后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管B中硬质玻璃管的右端。要使沉积得FeCl3进入收集器, 需进行的操作是
需进行的操作是  。
。
(4)FeCl3溶液常用于吸收有毒气体H2S。反应的离子方程式为 。
(5)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(过程中不振荡),充分反应后,进行如下实验:

淡黄色溶液中加入试剂X生成淡红色溶液的离子方程式为 。
(6)已知红色褪去的同时有气体生成,经检验为O2。该小组同学对红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无 明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
②另取同物质的量浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
根据上述实验得出溶液褪色的原因是: 。
查看答案和解析>>
科目: 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:简答题
人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
(1)工业上常用高浓度的K2CO3 溶液吸收CO2,得溶液X,再利用电解法使K2CO3  溶液再生,其装置示意图如下:
溶液再生,其装置示意图如下:
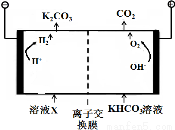
①在阳极区发生的反应包括 和H++HCO3- H2O+CO2↑。
H2O+CO2↑。
②简述CO32-在阴极区再生的原理 。
(2)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25 ℃,101 KPa下:
H2(g)+ 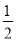 O2(g)
O2(g) H2O(g)ΔH1=-242kJ·mol-1
H2O(g)ΔH1=-242kJ·mol-1
CH3OH(g)+(3/2) O2(g) CO2(g)+2H2O(g)ΔH2=-676kJ·mo
CO2(g)+2H2O(g)ΔH2=-676kJ·mo l-1
l-1
①写出CO2和H2生成气态甲醇等产物的热化学方程式 。
②下面表示合成甲醇的反应的能量变化示意图,其中正确的是 (填字母序号)。
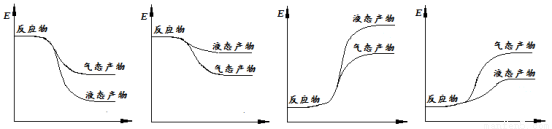
A B C D
(3)微 生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:
生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:
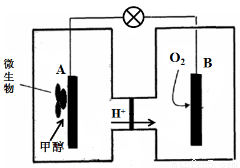
①该电池外电路电子的流动方向为 (填写“从A到B”或“从B到A”)。
②A电极附近甲醇发生的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com