
科目: 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
下列关于纯净物,混合物,强电解质,弱电解质和非电解质的正确组合是( )
纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
A | 纯盐酸 | 水煤气 | 硫酸 | 醋酸 | 干冰 |
B | 冰醋酸 | 空气 | 硫酸钡 | 亚硫酸 | 二氧化硫 |
C | 氯气 | 盐酸 | 苛性钠 | 氢硫酸 | 碳酸钙 |
D | 漂白粉 | 氨水 | 氯化钠 | 次氯酸 | 氯气 |
查看答案和解析>>
科目: 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH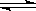 CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
①加少量烧碱固体 ②升高温度 ③加少量冰醋酸 ④加水
A.①② B.②③ C.③④ D.②④
查看答案和解析>>
科目: 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
H+浓度相同的等体积的两份溶液A和B,A为盐酸,B为醋酸,分别和锌反应,若最后仅有一份溶液中存在锌,且放出的氢气的体积相等,则下列说法正确的是( )
①反应所需要的时间B>A
②开始反应时的速率A>B
③参加反应的锌的物质的量A=B
④反应过程的平均速率B>A
⑤盐酸里有锌剩余 ⑥醋酸里有锌剩余
A.③④⑤ B.③④⑥ C.②③⑤ D.②③⑥
查看答案和解析>>
科目: 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
能说明醋酸是弱电解质的事实是( )
A.醋酸溶液的导电性比盐酸弱
B.醋酸溶液与碳酸钙反应,缓慢放出二氧化碳
C.醋酸溶液用水稀释后,氢离子浓度下降
D.0.1mol/L的CH3COOH溶液中,氢离子浓度约为0.001mol/L
查看答案和解析>>
科目: 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12[ | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
则下列说法中不正确的是( )
A.碳酸的酸性强于氢硫酸
B.多元弱酸的酸性主要由第一步电离决定
C.多元弱酸的各步电离之间无影响
D.向弱酸溶液中加少量NaOH溶液,电离常数不变
查看答案和解析>>
科目: 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
室温下向10 mL 0.1 mol/L的醋酸溶液中加水稀释并达到新平衡后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.平衡时,溶液中 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.溶液的pH减小
查看答案和解析>>
科目: 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:填空题
(1)氨气催化氧化生产硝酸,硝酸厂常用催化还原法处理尾气:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ/mol
则H2将NO2还原为N2的热化学反应方程式:__________________
(2)2SO2(g)+O2(g)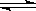 2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1molSO3(g)的ΔH= —99kJ/mol。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1molSO3(g)的ΔH= —99kJ/mol。请回答下列问题:
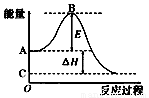
①图中A点表示: ;C点表示2mol SO3(g)的总能量。E所代表的能量是 ;E的大小对该反应的反应热 (填“有”或“无”)影响。
②图中△H= 。
查看答案和解析>>
科目: 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:填空题
现有常温下c(H+)=0.01mol/L的盐酸甲和c(H+)=0.01mol/L的醋酸溶液乙,回答下列问题:
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据变大的是___________。
A.c(H+) 
 B.c(H+)/c(CH3COOH)
B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-) D.c(OH-)/c(H+)
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡 (填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将 (填“增大”、“减小”或“无法确定”)。
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲)__ _________pH(乙)( 填“>”、“<”或“=”)。
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲) V(乙)( 填“>”、“<”或“=”)。
(5)已知25℃时,三种酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
K2 | 5.6×10-11 |
下列四种离子结合H+能力最强的是______________。
A.HCO3- B.CO32- C.ClO- D.CH3COO-
请写出在次氯酸钠溶液中通入少量二氧化碳气体的离子方程式:________________。
查看答案和解析>>
科目: 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:填空题
在2L密闭容器,800℃时发生如下反应:
2CuO(s)+CO(g)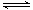 Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
n(CuO)(mol) | 0.080 | 0.060 | 0.040 | 0.020 | 0.020 | 0.020 |
(1)写出该反应的平衡常数表达式 。
已知:K(400℃)>K(350℃),则该反应 是 热反应。
是 热反应。
(2)右图中表示Cu2O的物质的量随时间变化的曲线是 (选填“A”或“B”),800℃时,0~3min内该反应的平均速率v (CO2)= 。
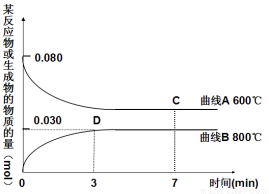
(3) 能说明该反应已达到平衡状态的是 。
a.v(CO)=v(CO2) b.容器内压强保持不变
c.v逆(CO)=v正(CO2) d.容器内气体的密度保持不变
(4)能使该反应的正反应速率增大,且平衡向正反应方向移动的是 。
A.增加CuO的量
B.适当升高温度
C.及时移去CO2
D.增大CO的浓度
E.选择高效催化剂
F.增大压强
查看答案和解析>>
科目: 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:填空题
有a、b两个极易导热的密闭容器,a保持容积不变,b中的活塞可上下移动,以保持内外压强相等。在相同条件下将3mol A,1mol B分别同时混合于a、b两容器中,发生反应:3A(g)+B(g)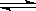 2C(g)+D(g)
2C(g)+D(g)
(1)达到平衡时,a中A的浓度为M mol/L。C的浓度为N mol/L,b中A的浓度为m mol/L,C的浓度为n mol/L,则M________m;N_________n(填>、<、=、无法比较)。
(2)保持温度不变,按下列配比分别充入a、b两容器,达平衡后,a中C的浓度为N mol·L-1的是 ,b中C的浓度为n mo1·L-1的是 。
A、6molA+2molB
B、3molA+2molC
C、2molC+1molB+1molD
D、2molC+1molD
E、1.5molC+0.5molB+1molC+0.5molD
(3)若将2mol C和2mol D充入a中,保持温度不变,平衡时A的浓度为W mol·L-1,C的浓度为Y mol·L-1,则W和M,Y和N之间的关系为W_____________M,Y_____________N(填>、<、=、无法比较)。
(4)保持温度不变,若将4mol C和2mol D充入a中,平衡时A的浓度为R mo1·L-1,则 。
A、R=2M B、R<M
C、M<R<2M D、R>2M
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com