
科目: 来源:2017届湖南省长株潭岳益五市十校高三12月联考化学卷(解析版) 题型:选择题
将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO).向反应后的溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加 5.1g.下列叙述不正确的是( )
A.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol
B.参加反应的金属的总质量 3.6g<m<9.6 g
C.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V=100mL
D.当金属全部溶解时收集到NO气体的体积在标况下为 2.24L
查看答案和解析>>
科目: 来源:2017届湖南省长株潭岳益五市十校高三12月联考化学卷(解析版) 题型:填空题
(1)汽车剧烈碰撞时,安全气囊中发生反应NaN3+KNO3→K2O+Na2O+X↑(未配平),已知X为单质,在反应中NaN3失去电子.则该反应的氧化剂为______,X的化学式为______.
(2)工业上制取高纯度MnO2的某一步骤如图所示:
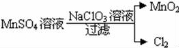
请写出该反应的离子方程式__ ___.
(3)草酸钙晶体(CaC2O4•H2O)可用作分离稀有金属的载体.
①在一定温度下向2L的密闭容器放入足量草酸钙(固体所占体积忽略不计)发生反应:CaC2O4(s)?CaO(s)+CO(g)+CO2(g),若前5min内生成CaO的质量为11.2g,则该段时间内v(CO)=__________mol•L﹣1•min﹣1;当反应达到平衡后,将容器体积压缩到原来的一半,则下列说法正确的是__________(填答案选项编号).
A.平衡不移动,CaO的质量不变
B.平衡发生移动,且CaC2O4的分解率增大
C.平衡发生移动,但CO和CO2的浓度都没有改变
D.平衡向逆反应方向移动,且该反应的化学平衡常数减小
②某温度下,向0.3mol/L的Na2CO3溶液中加入足量CaC2O4粉末后(忽略溶液体积变化),充分搅拌,发生反应:CO32﹣(aq)+CaC2O4(s)?CaCO3(s)+C2O42﹣(aq).静置后沉淀转化达到平衡.求此时溶液中的c(C2O42﹣)= mol•L﹣1.已知:该温度下,KSP(CaC2O4)=5.0×10﹣9;KSP(CaCO3)=2.5×10﹣9.
查看答案和解析>>
科目: 来源:2017届湖南省长株潭岳益五市十校高三12月联考化学卷(解析版) 题型:实验题
化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:①该牙膏摩擦剂由碳酸钙、氢氧化铝组成;
②牙膏中其它成分遇到盐酸时无气体产生。
实验内容:Ⅰ.摩擦剂中氢氧化铝的定性检验。
取适量牙膏样品,加水充分搅拌、过滤,往滤渣中加入过量NaOH溶液。
(1)该过程涉及主要反应的离子方程式是 。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的沉淀质量,以确定碳酸钙的质量分数。
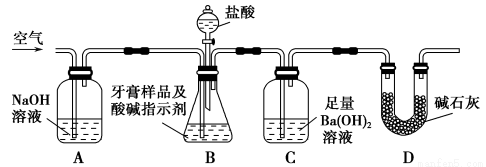
依据实验过程回答下列问题:
(2)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:_________________________。
(3)C中反应生成沉淀的化学方程式是_____________________。
(4)下列各项措施中,能提高测定准确度的是________(填标号)。
a.滴加盐酸不宜过快
b.在A~B之间增添盛有浓硫酸的洗气装置
c.在加入盐酸之前,应排净装置内的CO2气体
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取10.00 g样品三份,进行三次测定,测得C中产生沉淀平均质量为3.94 g。则样品中碳酸钙的质量分数为________。
(6)有人认为只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是______________________。
查看答案和解析>>
科目: 来源:2017届湖南省长株潭岳益五市十校高三12月联考化学卷(解析版) 题型:实验题
高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂。工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下:
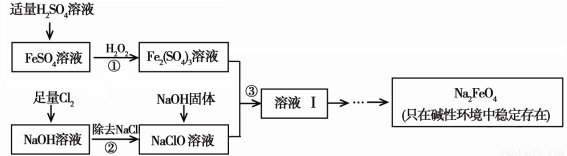

(1)高铁酸钠中铁元素的化合价为 ,次氯酸钠的电子式是________。
(2)步骤①反应的离子方程式是 。
(3)从溶液I中分离出Na2FeO4后,还有副产品Na2SO4 、NaCl,则步骤③中反应的离子方程式为 。
(4)工业上还可用电解浓NaOH溶液的方法制Na2FeO4,其工作原理如图所示:
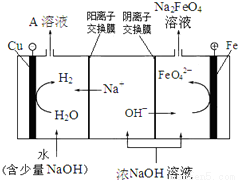
阳极的电极反应式为 。可循环使用的物质是 。
(5)计算Na2FeO4的消毒效率(以单位质量得到的电子数表示)约是氯气的________倍,
查看答案和解析>>
科目: 来源:2017届湖南省长株潭岳益五市十校高三12月联考化学卷(解析版) 题型:推断题
芳香化合物A(C9H9O3Cl)可以发生如下图所示的转化(其他产物和水已略去)
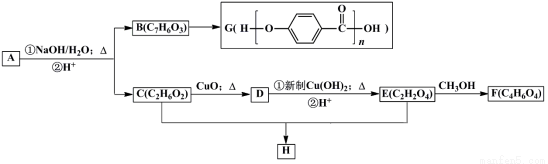
已知A遇氯化铁溶液变紫色,请回答下列问题:
(1)B的结构简式为是__________.
(2)D的名称是__________.
(3)E生成F的化学方程式为 。
(4)A与足量NaOH水溶液在加热条件下发生反应的方程式为 .
(5)H的结构简式为______________.
(6)B的同系物I比B相对分子质量大14,I的同分异构体中能同时满足如下条件:①分子中除 苯环外,无其他环状结构;②遇FeCl3溶液显紫色;③能发生水解反应,共有 种(不考虑立体异构)。其中核磁共振氢谱为五组峰,且峰面积比为1:2:2:2:1的同分异构体的结构简式为 。
苯环外,无其他环状结构;②遇FeCl3溶液显紫色;③能发生水解反应,共有 种(不考虑立体异构)。其中核磁共振氢谱为五组峰,且峰面积比为1:2:2:2:1的同分异构体的结构简式为 。
查看答案和解析>>
科目: 来源:2016-2017学年贵州省高二上期中化学卷(解析版) 题型:选择题
某物质熔融状态可导电,固态可导电,将其投入水中溶液也可导电,推测该物质可能是 ( )
A.金属 B.非金属 C.可溶性 碱
碱  D.可溶性盐
D.可溶性盐
查看答案和解析>>
科目: 来源:2016-2017学年贵州省高二上期中化学卷(解析版) 题型:选择题
下列物质按照纯净物、混合物、电解质和非电解质顺序排列的是( )
A.盐酸、天然气、醋酸、干冰 B.胆矾、漂白粉、氯化钾、氯气
C.氯化钠、福尔马林、硫酸钠、乙醇 D.单甘油酯、混甘油酯、苛性钾、石灰
查看答案和解析>>
科目: 来源:2016-2017学年贵州省高二上期中化学卷(解析版) 题型:选择题
下列叙述正确的是( )
A.生成物总能量一定低于反应物总能量
B.酒精可用作燃料,说明酒精燃烧是放热反应
C.硝酸铵溶于水温度 降低,这个变化是吸热反应
降低,这个变化是吸热反应
D.同温 同压下,H2和Cl2在光照和点燃条件下的ΔH不同
同压下,H2和Cl2在光照和点燃条件下的ΔH不同
查看答案和解析>>
科目: 来源:2016-2017学年贵州省高二上期中化学卷(解析版) 题型:选择题
已知HCN(aq)与NaOH(aq)反应生成1 mol正盐的ΔH=-12.1 kJ/mol;强酸、强碱的稀溶液反应的中和热ΔH=-57.3 kJ·mol-1。则HCN在水溶液中电离的ΔH等于( )
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1
C.+69.4 kJ·m ol-1 D.+45.2 kJ·mol-1
ol-1 D.+45.2 kJ·mol-1
查看答案和解析>>
科目: 来源:2016-2017学年贵州省高二上期中化学卷(解析版) 题型:选择题
一定温度下,反应N2(g)+O2(g) 2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
A.降低体系温度 B.恒容,充入He
C.恒容,充入N2 D.恒压,充入He
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com