
科目: 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是
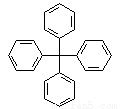
A. 分子式为C25H20
B. 所有碳原子可能在同一平面上
C. 该化合物分子一定处于同一平面的原子至少有12个
D. 分子中可能处于同一平面的原子最多有23个
查看答案和解析>>
科目: 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
下列有关电解质溶液中微粒的物质的量的浓度关系正确的是
A.在0.1mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
B.在0.1mol·L-1Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H2CO3)+ c(H+)
C.向0.2 mol·L-1NaHCO3溶液中加入等体积0.1mol·L-1NaOH溶液:
c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
D.常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1mol·L-1]:
c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
查看答案和解析>>
科目: 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
室温下向10mLpH=3的醋酸溶液中加入水稀释后,下列说法正确是的
A.溶液中导电粒子的数目减少
B.溶液中 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mLpH=11的NaOH溶液,混合液的pH=7
查看答案和解析>>
科目: 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
25℃时,在等体积的①pH=0的H2SO4溶液②0.05 mol·L-1的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是
A.1∶10∶1010∶109 B.1∶5∶5×109∶5×108
C.1∶20∶1010∶109 D.1∶10∶104∶109
查看答案和解析>>
科目: 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①CH3COONa②CH3COONa与NaOH;③CH3COONa与NaCl④CH3COONa与NaHCO3下列各项排序正确的是
A.pH:②>③>④>① B.c(CH3COO-):②>④>③>①
C.溶液中c(H+):①>③>②>④ D.c(CH3COOH):①>④>③>②
查看答案和解析>>
科目: 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:填空题
填写对应的结构简式(键线式)或名称:
(1)2-甲基-1,3-丁二稀的结构简式____________
(2)2-丙醇的结构简式__________________
(3)丙酸乙酯的键线式_____________
(4)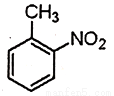 的名称______________。
的名称______________。
查看答案和解析>>
科目: 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:填空题
⑴室温时,pH=a的氨水与PH =b的盐酸等体积混合,恰好完全反应,则氨水电离度可表示为_______________ (用百分数来表示)
(2)室温下,0.1 mol/LNaClO溶液的pH_________0.1 mol/LNa2SO3溶液的pH。(选填“大于”、“小于”,或“等于”)。浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为 。
已知:
H2SO3 | Kal=1.54×l0-2 | Ka2=1.02×10-7 |
HCIO | Ka1=2.95×10-8 | |
H2CO3 | Kal=4.3×10-7 | Ka2=5.6×10-11 |
查看答案和解析>>
科目: 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:填空题
核磁共振氢谱是研究有机物结构的重要方法之一。在研究的化合物分子中:所处环境完全相同的氢原子在谱图中出现同一种信号峰:如 (CH3)2CHCH2CH3在谱图中有四种信号峰。请填写下列空白:
(1)化学式为C3H6O2的物质在核磁共振氢谱上观察到下列两种情况下氢原子给出的信号峰:第一种情况出现两个信号峰,第二种情况出现三个信号峰,由此可推断对应于这两种情况该有机物结构简式可能为:第一种:____________,第二种_____________(各写一个)
(2)测定CH3CH=CHCl时,能得到氢原子给出的信号峰有6种由此可推断该有机物可能的结构简式为:_____________________。
查看答案和解析>>
科目: 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:填空题
常温下,将0.05mol/L盐酸溶液和未知浓度的NaOH溶液以1: 2的体积比混合,所得溶液的pH=12。用上述NaOH溶液滴定pH=3的某一元弱酸溶液20mL,达到终点时消耗NaOH溶液13mL,试求:
(1)NaOH溶液的物质的量浓度为_____________mol/L
(2)此一元弱酸的物质的量浓度为___________mol/L
(3)求此条件下该一元弱酸的电离平衡常数为 ___________。
查看答案和解析>>
科目: 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:填空题
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示________,K值大小与温度的关系是:温度升高,K值_______。(填增大、减小、不变、或可能增大也可能减小)。
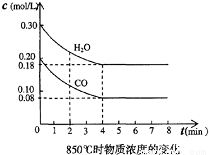
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g) + H2O(g)  CO2(g) + H2(g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)= mol·L-1·min-1。
CO2(g) + H2(g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)= mol·L-1·min-1。
(3 )t℃(高于850℃ ),在相同容器中发生上述反应,容器内各物质变化如下表。
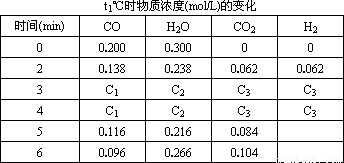
①表中3 min~4 min之间反应________(达到平衡,正向进行,逆向进行);C1数值________0.08 mol·L-1(填大于、小于或等于)。
②反应在4 min~5 min问,平衡向逆方向移动,可能的原因是________(单选),表中5 min~6 min之间数值发生变化,可能的原因是________(单选).
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com