
科目: 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:选择题
实验室用标准 KMnO4 溶液滴定未知浓度的 FeSO4,下列说法或操作正确的是( )
A.盛 FeSO4溶液的锥形瓶滴定前用 FeSO4溶液润洗 2—3 次
B.选碱式滴定管盛放标 准 KMnO4溶液,并用碘化钾淀粉溶液作指示剂
准 KMnO4溶液,并用碘化钾淀粉溶液作指示剂
C.锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度
D.滴定前仰视读数,滴定后俯视读数会导致滴定 结果偏低
结果偏低
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:选择题
有甲、乙、丙三瓶等体积、等物质的量浓度的NaOH溶液,若 甲不变,将乙蒸发掉一半水(溶质不析出),丙中通入一定量的CO2。然后以酚酞作指示剂,用相同浓度的盐酸滴定,分别达到终点消耗盐酸的体积是( )
甲不变,将乙蒸发掉一半水(溶质不析出),丙中通入一定量的CO2。然后以酚酞作指示剂,用相同浓度的盐酸滴定,分别达到终点消耗盐酸的体积是( )
A.V甲=V乙>V丙 B.V丙>V乙>V甲 C.V乙>V丙>V甲 D.V甲=V乙=V丙
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:选择题
在密闭容器中,5 mol H2与2 mol CO2发生反应:3H2(g)+C O2(g)
O2(g)  CH3OH(g)+H2O(g)。反应达到平衡时,改变温度(T)和压强(p),反应混合物中甲醇(CH3OH)的物质的量分数变化情况如下图所示。下列说法错误的是( )
CH3OH(g)+H2O(g)。反应达到平衡时,改变温度(T)和压强(p),反应混合物中甲醇(CH3OH)的物质的量分数变化情况如下图所示。下列说法错误的是( )
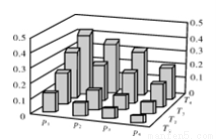
A.P1>P2>P3>P4
B.若T1> T2> T3>T4,则该反应为放热反应
C.甲醇的物质的量分数越高,反应的平衡常数越大
D.缩小容积,可以提高CH3OH在混合物中的质量分数
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:选择题
在空气中直接蒸发下列盐的溶液:①Fe2(SO4)3②Na2CO3③KCl④CuCl2⑤NaHCO3可以得到相应盐的晶体(可以含有结晶水)的是( )
A.①②③ B.①③⑤ C.②④ D.①③④⑤
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:选择题
25℃时,在10 mL浓度均为0.1 mol/LNaOH和NH3·H2O混合溶液中滴加0.1 mol/L盐酸,下列有关溶液中粒子浓度关系正确的是( )
A.未加盐酸时:c( OH-)>c(Na+)=c(NH3·H2O)
OH-)>c(Na+)=c(NH3·H2O)
B.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
C.加入10 mL盐酸时:c(NH )+c(H+)=c(OH-)
)+c(H+)=c(OH-)
D.加入20 mL盐酸时:c(Cl-)=c(NH )+c(Na+)
)+c(Na+)
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:选择题
T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g),反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2,Y的百分含量与时间的关系如图2所示。下列分析不正确的是( )

A.容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g)
B. 0~3min内,v(X)=0.1 mol/(L•min)
C.若改变条件,使反应进程如图3所示,则改变的条件可能是增大压强
D.达平衡后,升高温度,v正、v逆都增大,且再次平衡前v正>v逆
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:选择题
某Na2CO3、NaAlO2的混合溶液中逐滴加入1 mol/L的盐酸,测得溶液中CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是( )

A.a曲线表示的离子方程式为AlO2-+H++H2O==Al(OH)3↓
B.原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
C.V1∶V2=l∶5
D.M点时生成的CO2为0.05 mol
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:选择题
在体积都为1L,pH=2的盐酸和醋酸溶液中,投入0.65g锌粒,则下图所示比较符合客观事实的是( )
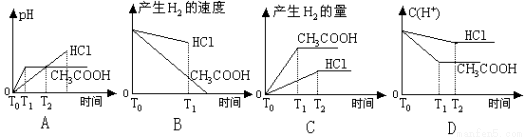
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:填空题
实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求。试运用所学知识,解决下列问题:
(1)煤化工通常通过研究不同温度下的平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:
CO(g)+H2O(g) H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表所示:
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
①若在500℃时进行反应,设CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为 。
②800℃时,在固定容积的密闭容器中放入混合物,起始浓度为:c(CO) =0.01mol/L,c(H2O)=0.03mol/L,c(CO2)=0.01mol/L, c(H2)=0.05mol/L ,则
=0.01mol/L,c(H2O)=0.03mol/L,c(CO2)=0.01mol/L, c(H2)=0.05mol/L ,则 反应开始时,H2的消耗速率比生成速率 (填“大”、“小”或“不能确定”)。
反应开始时,H2的消耗速率比生成速率 (填“大”、“小”或“不能确定”)。
(2)2SO2(g)+O2(g) 2SO3(g)反应过程中的能量变化如图所示:又已知1molSO2
2SO3(g)反应过程中的能量变化如图所示:又已知1molSO2 (g)氧化为1molSO3(g)的ΔH=-99 kJ·mol-1,请回答问题:
(g)氧化为1molSO3(g)的ΔH=-99 kJ·mol-1,请回答问题:

该反应通常用V2O5作催化剂,加V2O5会使图中B点 (填“升高”或“降低” )△H (填“变大”、“变小”或“不变”);
(3)已知某反应的平衡常数表达式为: ,它所对应反应的化学方程式为
,它所对应反应的化学方程式为
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:填空题
化合物AX3和单质X2在一定条件下反应可生成化合物AX5。回答下列问题:
(1)反应AX3(g)+X2(g) AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。

① 图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为 (填实验序号);与实验a相比,其他两组改变的实验条件及判断依据是:b 、c 。
②用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,则α的表达式为 ;实验a平衡转化率:α(a)为 。
(2)已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成lmol AX5,放出热量123.8 kJ。该反应的热化学 方程式为 。
方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com