
科目: 来源:2017届河北省高三上调研四化学试卷(解析版) 题型:选择题
某小组用下图装置进行实验,下列说法正确的是
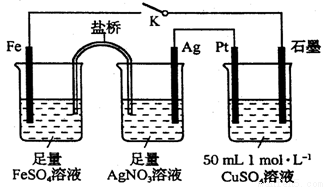
A.盐桥中的电解质可以用KCl
B.闭合K,外电路电流方向为Fe电极→石墨电极
C.闭合K,石墨电极上只生成铜
D.导线中流过0.15mol电子时,加入5.55gCu2(OH)2CO3,CuSO4溶液可恢复原组成
查看答案和解析>>
科目: 来源:2017届河北省高三上调研四化学试卷(解析版) 题型:实验题
在实验室中某实验小组同学关于硫酸铜的制取和应用,设计了以下实验:
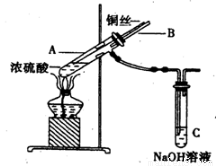
(1)装置A中发生反应的化学方程式为________________________。
(2)为符合绿色化学的要求,某同学进行如下设计:将铜粉在___________(填仪器名称)中反复的灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应,反应后溶液经过_________、___________、过滤、洗法、干燥,即可得到产品CuSO4·5H2O晶体。
(3)将空气或氧气直接通入到钢粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4作催化剂,即发生反应,生成硫酸铜。其反应过程的第2步是:___________,Fe3++Cu==2Fe2++Cu2+,请写出其第1步反应的离子方程式_________________。
(4)制取的CuSO4溶液和“另一物质”在40~50℃混合时生成了一种难溶物质氢化亚铜(CuH)。将CuH溶解在稀盐酸中时生成了一种气体,这种气体是 _____________,经收集测定生成的该气体为标况下11.2 L,则被还原的离子得电子的物质的量是___________。
查看答案和解析>>
科目: 来源:2017届河北省高三上调研四化学试卷(解析版) 题型:推断题
A、B、C、X是中学化学中常见的4种物质,它们均由短周期元素组成,转化关系如图所示。请针对以下两种情况回答下列问题。
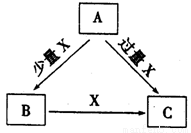
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得白色胶状沉淀B。
① A中含有的金属元素为__________(填元素名称)。
②该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨,此反应的化学方程式为:__________。
(2)若A、B、C的焰色反应均呈黄色,水溶液均呈碱性。
① A中所含有的化学键是________、__________。
②将4.48 L(标准状况下)X通入100 mL3 mol/LA的水溶液后,溶液中离子浓度由大到小的顺序为__________。
③自然界中存在由B或C与H2O按一定比例结晶而成的固体。将一定置的由C与H2O按一定比例形成的晶体溶于水配制成100 mL溶液,测得溶液中金属阳离子的浓度为0.5mol/L。若取相同质量的此晶体加热至恒重,剩余固体的质量为________________。
查看答案和解析>>
科目: 来源:2017届河北省高三上调研四化学试卷(解析版) 题型:填空题
以含有Al2O3、Fe2O3等杂质的铬铁矿[主要成分为Fe(CrO2)2]为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O)的主要工艺流程如下:
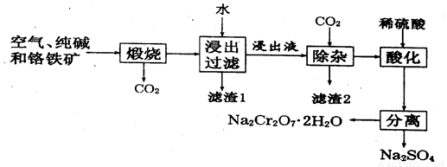
己知:铬铁矿在空气中与纯减煅烧生成Na2CrO4和一种红棕色固体,同时释放出CO2气体,
且 Al2O3+Na2CO3 2NaAlO2+ CO2↑。请回答:
2NaAlO2+ CO2↑。请回答:
(1)在铬铁矿Fe(CrO2)2中,Cr的化合价为___________。
(2)滤渣2的成分为_____________。
(3)将滤渣1放入稀硫酸溶解后得溶液W,检验该溶液中金属离子的方法是_________。
(4)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol/L以下才能排放。含CrO42-的废水处理通常有以下两种方法。
①沉淀法:
加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于________________mol/L,后续废水处理方能达到国家排放标准。
②还原法:CrO42-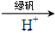 Cr3+
Cr3+ Cr(OH)3。写出酸性条件下CrO42-与绿巩在溶液中反应的离子方程式:_________________________________。
Cr(OH)3。写出酸性条件下CrO42-与绿巩在溶液中反应的离子方程式:_________________________________。
(5)某高效净水剂是由K2FeO4得到的,工业上以溶液w、次氯酸钾和氢氧化钾为原料制备K2FeO4,该反应的离子方程式是______________________。
查看答案和解析>>
科目: 来源:2017届河北省高三上调研四化学试卷(解析版) 题型:填空题
欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源显得更加紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯, 请完成该反应的化学方程式
_____C+____ KMnO4+____H2SO4→____CO2↑+_____MnSO4+ ______K2SO4+_____H2O
(2)焦炭可用于制取水煤气,测得12g碳与水蒸气完全反应生成水煤气时,吸收了131.6kJ热量。
反应的热化学方程式为_________________。
(3)工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g)  CH3OH(g) △H=akJ/mol 如表所列数据是反应在不同温度下的化学平衡常数(K)。
CH3OH(g) △H=akJ/mol 如表所列数据是反应在不同温度下的化学平衡常数(K)。

① 判断反应达到平衡状态的依据是___________。(填序号)
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的平均相对分子质量不变
C.混合气体的密度不变
D.CH3OH、CO、H2的浓度都不再发生变化
②某温度下,将2molCO和一定量的H2充入2L的密闭容器中,充分反应l0min后,达到平衡时测得c(CO)=0.2 mol/L,则以H2表示的反应速率v(H2)=________。
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混和气为正极助燃气,制得在650℃下的燃料电池,其正极反应式:O2+2CO2+4e-=2CO32-,则负极反应式为___________________。
(5)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层淸液,如此处理多次,可使BaSO4 全部转化为BaCO3发生反应:BaSO4(s) + CO32-(aq)=BaCO3(s) +SO42-(aq)。己知某温度下该 反应的平衡常数 K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积 Ksp=______。
查看答案和解析>>
科目: 来源:2017届河北省高三上调研四化学试卷(解析版) 题型:填空题
下图所示的四个容器中分别盛有不同的溶液,除a、b外,其余电极均为石墨电极。甲为铅蓄电池,其工作原理为:Pb + PbO2+2H2SO4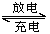 2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb。闭合K,发现g电极附近的溶液先变红,20min后,将K断开,此时c、d两极上产生的气体体积相同:据此回答:
2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb。闭合K,发现g电极附近的溶液先变红,20min后,将K断开,此时c、d两极上产生的气体体积相同:据此回答:
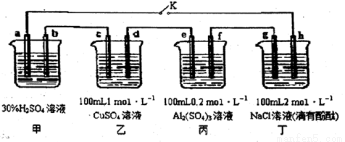
(1) a电极的电极材料是____________________ (填“PbO2”或“Pb”)。
(2)丙装置中发生电解的总反应方程式为_____________________。
(3)电解20min时,停止电解,此时要使乙中溶液恢复到原来的状态,需要加入的物质及其物质的量是________________。
(4)20min后将乙装置与其他装置断开,然后在c、d两极间连接上灵敏电流计,发现电流计指针偏转,则此时c电极为_______极,d电极上发生反应的电极反应式为_____________。
(5)电解后取amL丁装置中的溶液,向其中逐滴加入等物质的量浓度的CH3COOH溶液,当加入 bmLCH3COOH溶液时,混合溶液的pH恰好等于7(体积变化忽略不计)。己知CH3COOH 的电离平衡常数为1.75×10-5,则a/b=________。
查看答案和解析>>
科目: 来源:2016-2017学年广东省高一上大考二化学卷(解析版) 题型:选择题
下列物质分类正确的是
A.SO2、SiO2、CO均为酸性氧化物
B.碳酸、次氯酸、亚硫酸均为弱电解质
C.烧碱、冰醋酸、四氯化碳均为电解质
D.氯化钠溶液、硫酸均为强电解质
查看答案和解析>>
科目: 来源:2016-2017学年广东省高一上大考二化学卷(解析版) 题型:选择题
下列事故处理正确的是
A. 钠燃烧,可用砂子灭火,不能用二氧化碳灭火器来灭火
B. 眼睛里不慎溅进了稀药液,应立即用水冲洗,并且用手使劲揉眼睛
C. 少量浓硫酸沾到皮肤上,立即用氢氧化钠溶液冲洗
D. 熄灭酒精灯可直接用嘴吹
查看答案和解析>>
科目: 来源:2016-2017学年广东省高一上大考二化学卷(解析版) 题型:选择题
下列关于胶体的叙述不正确的是
A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间
B.光线透过胶体时,胶体中可发生丁达尔效应
C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
D.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
查看答案和解析>>
科目: 来源:2016-2017学年广东省高一上大考二化学卷(解析版) 题型:选择题
下列各组离子中能大量共存的是
A.无色溶液中:K+、Na+、MnO4﹣、SO42﹣
B.在酸性溶液中:Mg2+、Na+、SO42﹣、Cl﹣
C.能使pH试纸变蓝色的溶液:Cl﹣、HCO3﹣、SO42﹣、NH4+
D.碱性溶液中:K+、Cl﹣、NO3﹣、Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com