
科目: 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:选择题
高铁酸钾( K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂.工业制备高铁酸钾的反应离子方程式为 Fe(OH)3+C1O-+OH-→FeO42-+C1-+H2O(未配平).下列有关说法不正确的是
A.由上述反应可知,C1O-的氧化性强于FeO42-
B.高铁酸钾中铁显+6 价
C.上述反应中氧化剂和还原剂的物质的量之比为 2︰3
D. K2FeO4处理水时,不仅能消毒杀菌,而且生成的 Fe3+与水反应形成Fe(OH)3胶体
查看答案和解析>>
科目: 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:选择题
2.3g 纯净金属钠一定条件下在干燥空气中被氧化后得到 3.5g 固体,由此判断其产物是 ( )
A.氧化钠 B.过氧化钠 C.氧化钠和过氧化钠 D.无法确定
查看答案和解析>>
科目: 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:选择题
现有一块已知质量的铝镁合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案
实验设计1:铝镁合金 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积
实验设计2:铝镁合金 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积
实验设计3:铝镁合金 溶液
溶液 过滤,测定得到沉淀的质量
过滤,测定得到沉淀的质量
则能测定出镁的质量分数的是( )
A.都能 B.都不能 C. ①不能,其它都能 D. ②③不能, ①能
查看答案和解析>>
科目: 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:选择题
下列除杂质(括号中物质为杂质)所用试剂或方法不正确的是( )
A. NaCl 溶液(I2): CCl4 萃取分液
B. Mg (Al): NaOH 溶液
C. NaHCO3 溶液( Na2CO3):过量的 CO2
D. CO2(HCl):饱和 Na2CO3溶液
查看答案和解析>>
科目: 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:选择题
下列各项操作中, 不发生 “先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入 CO2至过量
②向Fe(OH)3胶体中逐滴加入稀盐酸至过量
③向 NaAlO2 溶液中通入 CO2至过量
④向 AlCl3溶液中加入 Ba(OH)2溶液至过量
⑤向 CaCl2 溶液中通入 CO2 至过量
A. ①③⑤ B. ①② C. ①③ D. ②③⑤
查看答案和解析>>
科目: 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:选择题
某干燥粉末可能由 Na2O、 Na2O2、 Na2CO3、 NaHCO3、 NaCl 中的一种或几种组成。将该粉末与足量盐酸反应有气体 X 逸出, X 通过足量的 NaOH 溶液后体积缩小(同温同压下测定)。若将原来的粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原混合粉末的质量。下列判断正确的是( )
①粉末中一定有 Na2O, Na2O2, NaHCO3
②无法确定是否含有 NaHCO3
③粉末中一定不含有 Na2O 和 NaCl
④无法确定是否含有 Na2CO3和 NaCl
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
科目: 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:选择题
某温度下,将Cl2通入NaOH 溶液中,反应得到NaCl.NaClO.NaClO3 的混合溶液,经测定 ClO-与 ClO3-的浓度之比为 1:3,则 Cl2与 NaOH 溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为( )
A. 21:5 B. 11:3 C. 3:1 D. 4:1
查看答案和解析>>
科目: 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:填空题
(1)请将5种物质: N2O、 FeSO4、 Fe(NO3)3、 HNO3 和 Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
______+______=______+______+______+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1mol 氧化剂_______(填“得到”或“失去”) ___________ mol 电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中,标出电子转移的方向和数目(用单线桥表示)______+______→______
查看答案和解析>>
科目: 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:实验题
某学生欲配制6.0 mol/L的H2SO4480 mL,实验室有三种不同浓度的硫酸:①240mL 1.0 mol/L的硫酸; ②20 mL 25%的硫酸(ρ=1.18 g/mL); ③足量的18 mol/L的硫酸。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为______mol/L(保留1位小数)。
(2)配制该硫酸溶液应选用容量瓶的规格为______mL。
(3)配制时,该同学的操作顺序如下,请将操作步骤 B、D 补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18 mol/L 的浓硫酸________mL,沿玻璃棒倒入上述混合液中。并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.____________________________;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2 cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(4)如果步骤C中的硫酸溶液未冷却就转移到容量瓶并定容,对所配溶液浓度有何影响?____________(填“偏大”、“偏小”或“无影响”下同)。如果省略步骤 D,对所配溶液浓度有何影响?________________。
查看答案和解析>>
科目: 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:填空题
化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,不恰当的一种物质是__________.(填化学式)
(2)“三酸”与“两碱”之间均可反应,酸过量时若用化学方程式表示有六个,若用离子方程式表示却只有两个,请写出这两个离子方程式_____________,_______________。
(3) “三酸”常用于溶解金属和金属氧化物.某化学兴趣小组在烧杯中放入铜屑和稀硫酸,加热并不断通入空气,观察到溶液逐渐变为蓝色,用化学方程式表示这一实验过程:_________________。
(4)烧碱可吸收CO2,当含0.2molNaOH的溶液吸收一定量CO2后,向溶液中逐滴滴加稀盐酸,下图表示加入盐酸体积和生成的CO2的体积的关系:
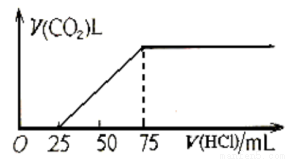
曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是__________,所用的稀盐酸的物质的量浓度为________(保留2位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com