
科目: 来源:2017届湖南省怀化市高三上学期期中质检化学试卷(解析版) 题型:选择题
用下表提供的仪器和药品,能完成实验目的的是 ( )
| 仪器 | 药品 | 实验目的 |
A | 烧杯、分液漏斗、 | 待提纯AlCl3溶液、NaOH溶液 | 除去AlCl3溶液中的 |
B | 分液漏斗、烧瓶、 | 盐酸、大理石、 | 证明非金属性: |
C | 酸式滴定管、锥形瓶、 | 已知浓度的盐酸、 | 测定NaOH溶液的浓度 |
D | 胶头滴管、试管 | Na2CO3溶液、稀盐酸 | 鉴别Na2CO3溶液、稀盐酸 |
查看答案和解析>>
科目: 来源:2017届湖南省怀化市高三上学期期中质检化学试卷(解析版) 题型:选择题
将0.03 mol Cl2缓缓通入含0.02 mol H2SO3和0.02 mol HBr的混合溶液中,在此过程溶液的c(H+)与Cl2用量的关系示意图是(溶液的体积视为不变)( )
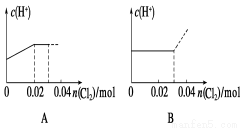
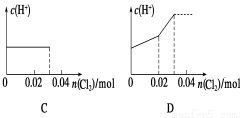
查看答案和解析>>
科目: 来源:2017届湖南省怀化市高三上学期期中质检化学试卷(解析版) 题型:选择题
在25 ℃时,将0.2 mol CH3COONa晶体和0.1 mol HCl气体同时溶于水中制得1 L溶液,若此溶液中c(CH3COO-)>c(Cl-),则下列判断不正确的是( )
A.该溶液的pH小于7
B.c(CH3COOH)+c(CH3COO-)=0.20 mol·L-1
C.c(CH3COOH)<c(CH3COO-)
D.c(CH3COO-)+c(OH-)=0.10 mol·L-1
查看答案和解析>>
科目: 来源:2017届湖南省怀化市高三上学期期中质检化学试卷(解析版) 题型:填空题
硫及许多化合物有很多重要的应用。
(1)古代四大发明之一的黑火药是由硫磺、木炭粉和__________按一定比例混合而成。
(2)黄铁矿的主要成分是FeS2,用于工业制取硫酸。生产硫酸经历三个生产阶段:
①第一阶段将黄铁矿粉末投入沸腾炉里与空气燃烧生成氧化铁等,其反应的化学方程式为__________________,氧化产物是_______________。
②第二阶段是在氧化炉中将S进行催化氧化。已知6.4g SO2气体完全氧化为SO3气体放出14.8kJ的热量。写出该反应的热化学方程式为________________________。工业上采用常压生产,则提高SO3产率的措施还有______________________(写2种即可)
(3)亚硫酸钠(Na2SO3)可用于生产饮用水作去氯剂,写出去氯(Cl2)的离子方程式:_____________。
(4)五水硫代硫酸钠(Na2S2O3·5H2O)是一种重要的化工原料。工业上的一种生产方法是将SO2通入由Na2S与Na2CO3按特定比例配成的混合液中并在合适温度下进行反应,然后经一系列工艺结晶获得。写出SO2通入Na2S与Na2CO3混合液发生反应的化学方程式为_________________________。
查看答案和解析>>
科目: 来源:2017届湖南省怀化市高三上学期期中质检化学试卷(解析版) 题型:推断题
现有A、B、C、D、E、F、G七种原子序数依次增大的元素,其中前六种属于短周期主族元素。A与B可构成三核10电子的分子;E原子的核外电子数是B原子的核内质子数的2倍;C、D、F同周期,且它们的最高价氧化物的水化物两两之间相互发生复分解反应;G的一种氧化物常作红色油漆的颜料。
(1)G在元周期表中的位置是_____________,E形成的单核阴离子的结构简图为______________________。
(2)X是由B、C按原子个数为1︰1组成的化合物,而Y是由A、B、C组成的常见化合物。则X的电子式为____________,Y中的化学键类型有___________________。
(3)C、D的最高价氧化物的水化物相互反应的离子方程式为________________________,G的单质与水蒸气反应的化学方程式为________________________。
(4)化合物DF3溶液通过蒸发并灼烧得到的固体是_________________(写化学式)。
查看答案和解析>>
科目: 来源:2017届湖南省怀化市高三上学期期中质检化学试卷(解析版) 题型:填空题
CO2是目前最主要的温室气体,减小CO2的排放并用来制造有价值的化学用品是目前的研究目标。
(1)利用CO2与CH4生产合成气(CO、H2):
已知:CH4(g)+2O2(g) CO2(g)+2H2O(g) ΔH=-890.3 KJ·mol-1
CO2(g)+2H2O(g) ΔH=-890.3 KJ·mol-1
CO(g)+H2O(g) CO2(g)+H2(g) ΔH=+2.8 KJ·mol-1
CO2(g)+H2(g) ΔH=+2.8 KJ·mol-1
2CO(g)+O2(g) 2CO2(g) ΔH=-566.0 KJ·mol-1
2CO2(g) ΔH=-566.0 KJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g) ΔH= ____________。
2CO(g)+2H2(g) ΔH= ____________。
②250℃时,以镍合金为催化剂,向体积为4 L的密闭容器中通入6 mol CO2、6 mol CH4,开始发生如下反应:CO2(g)+CH4(g) 2CO(g)+2H2(g)。经过一段时间达到平衡,平衡体系中各组分体积分数(某一成分物质的量占总气体物质的量的百分数)如下表:
2CO(g)+2H2(g)。经过一段时间达到平衡,平衡体系中各组分体积分数(某一成分物质的量占总气体物质的量的百分数)如下表:
物质 | CH4 | CO2 | CO | H2 |
体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
此温度下该反应的平衡常数K=________________。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如下图所示。250~300℃时,乙酸的生成速率减小的可能原因是____________________。

(3) 如以氢氧化钾水溶液作电解质进行电解,CO2在铜电极上可转化为甲烷,该电极反应方程式为_____________________。
(4)将2mol CO2和6molH2容积相同而温度不同的Ⅰ、Ⅱ两个恒容密闭容器中开始发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如下图1所示。
CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如下图1所示。


①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ_______KⅡ(填“>”“=”或“<”),可知该 反应是一个_______(填“放热”或“吸热”)反应。
②下列事实说明该反应已达到平衡状态的是_________________:
A.容器内气体压强保持不变
B.容器内气体的密度保持不变
C.CO2的体积分数保持不变
D.CO2的消耗速率与CH3OH的生成速率相等
E.容器内混合气体的平均相对分子质量保持不变
(5)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如上图2所示。在0~15小时内,CH4的平均生成速率Ⅰ、Ⅱ和Ⅲ从大到小的顺序为_____________(填序号)。
查看答案和解析>>
科目: 来源:2017届湖南省怀化市高三上学期期中质检化学试卷(解析版) 题型:实验题
硫酸厂的烧渣主要成分是Fe2O3,其次含少量的SiO2和FeS。工业上利用硫酸厂烧渣经回收处理制得绿矾(FeSO4·7H2O)和一种聚铁胶体[Fe(OH)SO4]n。绿矾是治疗缺铁性贫血药品的重要成分,而聚铁胶体是重要的水处理剂。上述生产工艺流程如下:

请通过分析回答下列相关问题:
(1)灼烧产生的尾气对大气有污染,因此工业生产中必须进行回收处理,下列方法可行的是_______________:
A.用氨水吸收 B. 直接用水吸收
C. 用浓硫酸吸收 D. 与空气混合用石灰石粉末悬浊液吸收
(2)操作Ⅲ是_____________、_______________、过滤、洗涤、干燥保存等;
(3)在由溶液X制聚铁胶体过程中①调节pH及②控制温度目的是___________________。
(4)在反应釜中FeS、O2及稀H2SO4反应硫酸铁等物质,则反应的离子方程式为___________________________;
(5)某研究性小组为探究绿矾(相对分子质量:278)在隔绝空气条件下加热分解反应的产物(已知分解产物全为氧化物),进行了如图所示的实验:

① 实验开始时,在点燃C处酒精喷灯之前应先打开活塞通CO2,其目的是_____________。 装置D的作用是______________________。
②该组同学设计的装置存在着一个明显的缺陷是____________________________。
③该组同学称取55.6 g绿矾按上图装置进行实验。待绿矾分解完全后,E瓶中产生了23.3 g白色沉淀。将C中固体产物投入足量稀硫酸中完全溶解得到溶液,取少量该溶液滴入KSCN溶液呈红色;另取少量该溶液滴入酸性KMnO4溶液,KMnO4溶液不褪色。据写出绿矾分解的化学方程式为__________________________。
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三上考试化学试卷(解析版) 题型:选择题
下列化合物中,属于碱的是
A.MgO B.SO2 C.H2SO4 D.Ca(OH)2
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三上考试化学试卷(解析版) 题型:选择题
下列物质属于电解质的是
A.石墨 B.液态HCl C.葡萄糖 D.Na2CO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com