
科目: 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.常温常压下11.2 L乙烯气体含有的分子数为0.5NA
B.1 L 1 mol·L-1CH3 COONa溶液中含有NA个CH3 COO-
C.1 mol —OH(羟基)中含有10 NA个电子
D.16gCH3OH分子中含有的共价键数目为2.5NA个
查看答案和解析>>
科目: 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大。X是地壳中含量最高的元素,Y+与X2-具有相同的电子层结构,Y与Z位于相邻主族,W与X同主族。下列说法正确的是
A. W的氢化物比X的氢化物稳定
B. Y在周期表中的位置为第3周期、IB族
C. Z的最高价氧化物对应的水化物的碱性比Y的弱
D. X的单质与含W化合物不可能发生置换反应
查看答案和解析>>
科目: 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
下列关于物质性质或检验的叙述不正确的是
A.在溶液中加KSCN,溶液显红色,证明原溶液中一定有 Fe3+,可能有Fe2+
Fe3+,可能有Fe2+
B.气体通过湿润的红色石蕊试纸,试纸变蓝,证明原气体中一定含有氨气
C.用铂丝蘸取白色粉末灼烧,火焰成黄色,证明原 粉末中一定有Na+,可能有K+
粉末中一定有Na+,可能有K+
D.向某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有CO32-或SO32-
查看答案和解析>>
科目: 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
工业上用粗盐(含Ca2+、Mg2+、SO42-等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示。下列有关说法正确的是
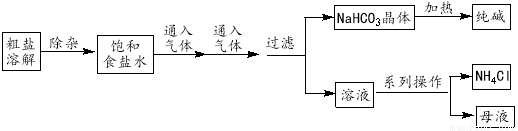
A.对粗盐溶液除杂可依次加入NaOH、Na2CO3、BaCl2,再加入盐酸调节溶液pH
B.饱和食盐水中先通入的气体为CO2
C.流程图中的“系列操作”若在实验室中进行,一定需要玻璃棒
D.如图所示装置可以比较Na2CO3和Na HCO3晶体的热稳定性
HCO3晶体的热稳定性
查看答案和解析>>
科目: 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g) + Y(g)  2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.0~2min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C.该温度下此反应的平衡常数K =1.44
D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
查看答案和解析>>
科目: 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
下列图示与对应的叙述不相符的是

A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1醋酸溶液得到滴定曲线
D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入NaOH溶液,随着NaOH溶液体积V的变化,沉淀总物质的量n的变化
查看答案和解析>>
科目: 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
环保、安全的铝--空气电池的工作原理如图所示,下列有关叙述错误的是
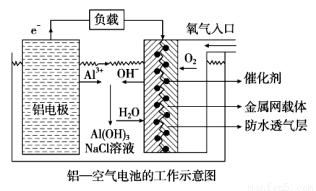
A.电池工作过程中,电解质溶液的pH不断增大
B.正极的电极反应式为O2 + 4e-+ 2H2O =4OH-
C.NaCl的作用是增强溶液的导电性
D.用该电池做电 源电解KI溶液制取1 mol KIO3,消耗铝电极的质量为54 g
源电解KI溶液制取1 mol KIO3,消耗铝电极的质量为54 g
查看答案和解析>>
科目: 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
有一未完成的离子方程式:( )+ XO3- + 6H+ ═3X2+3H2O,据此判断下列说法错误的是
A.X原子最外层电子数为5
B.当有3mol X2生成时,转移5mol电子
C.氧化产物和还原产物的物质的量之比为5︰1
D.“( )”括号中所填的微粒为X-
查看答案和解析>>
科目: 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
常温下,0.2 mol•L-1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
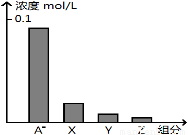
A.HA为强酸
B.该混合液pH=7
C.图中X表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)
查看答案和解析>>
科目: 来源:2017届福建省高三上联考二化学卷(解析版) 题型:实验题
Ⅰ.某化学兴趣小组用以下装置探究SO2的某些化学性质。
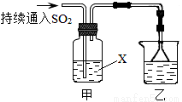
(1)装置乙的作用是 。
(2)若X为品红溶液,观察到溶液褪色,说明SO2具有 (填序号,下同);
若X为Na2S溶液,观察到溶液中出现淡黄色浑浊,说明SO2具有 ;
a.氧化性 b.还原性 c.漂白性
(3)若试剂X为Ca(ClO)2溶液,可观察到白色沉淀生成,完成该过程的离子方程式:
 Ca2++
Ca2++ ClO-+
ClO-+ SO2+
SO2+ H2O=
H2O= CaSO4↓+
CaSO4↓+ Cl-+
Cl-+ SO42-+
SO42-+ 。
。
Ⅱ.某兴趣小组为探究沉淀溶解平衡的原理并测定某温度下PbI2溶度积常数,设计如下实验。
i.取100mL蒸馏水,加入过量的PbI2固体(黄色),搅拌,静置,过滤到洁净的烧杯中,得到滤液。
(4)搅拌的目的是 。
(5)取少量滤液于试管中,向其中滴加几滴0.1 mol·L-1KI溶液,观察到的现象是 。
ii.准确量取10.00mL滤液,与离子交换树脂(RH)发生反应:2RH + Pb2+= R2Pb + 2H+,交换完成后,流出溶液用滴定法测得n(H+)=3.000×10-5 mol。
(6)在此实验温度下,PbI2的溶度积常数Ksp= 。若步骤i盛装滤液的烧杯中有少量水,Ksp测定结果将会 (填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com