
科目: 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:选择题
如图所示,a和b是盐酸和氢氧化钠溶液相互反应的pH值变化曲线,下列说法不正确的是
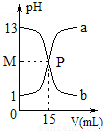
A.NaOH的物质的量浓度:c(NaOH)=0.1mol·L-1
B.a和b曲线上的任何一点都有:c(Na+)+c(H+)=c(Cl-)+c(OH-)
C.P点溶液中:c(Na+)=c(Cl-)> c(H+)=c(OH-)
D.曲线b是氢氧化钠溶液中逐滴加入盐酸的pH值变化曲线
查看答案和解析>>
科目: 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:选择题
向含amol H2S水溶液中通入bmol Cl2,当通入的Cl2少量时,产生浅黄色浑浊,增加通入Cl2的量,浅黄色浑浊逐渐消失,最后成为无色溶液,却溶液呈强酸性,下列说法不正确的是
A.当b≤a时,发生的离子方程式:H2S+Cl2=2H++S↓+2Cl-
B.当2a=b时,发生的离子方程式:3H2S+6Cl2+4H2O=14H++2S↓+SO42-+12Cl-
C.当a≤b≤4a时,反应中转移电子的物质的量n(e-)为2amol≤n(e-)≤8amol
D.当a<b<4a时,溶液中的S、SO42-、Cl-的物质的量比为(4a-b)∶(b-a)∶2b
查看答案和解析>>
科目: 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:选择题
某待测溶液(阳离子为Na+)中可能含有SO42-、SO32-、NO3-、Cl-、Br-、CO32-、HCO3-中的一种或多种,进行如图所示的实验,每次实验所加试剂均过量,已知稀HNO3有强氧化性,下列说法不正确的是
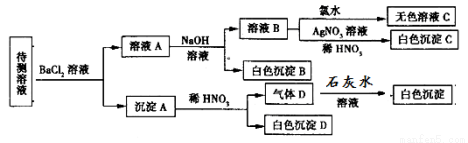
A.SO42-、SO32-至少含有一种
B.沉淀B的化学式为BaCO3
C.肯定存在的阴离子有CO32-、HCO3-、Cl-
D.肯定没有的离子是Br-
查看答案和解析>>
科目: 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:推断题
已知:A是石油裂解气的主要成份。现以A为主要原料合成 乙酸乙酯,其合成路线如下图所示。回答下列问题:
乙酸乙酯,其合成路线如下图所示。回答下列问题:
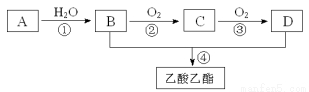
(1)A转化为B的反应类型___________。
(2)D分子中官能团的名称_______。
(3)写出B与金属钠反应的化学方程式是____________________。
(4)下列说法正确的是________________。
A.B分子中的所有原子在同一平面上
B.一定条件下,C中的官能团可以用银氨溶液来检验
C.A可以在其他条件下被氧气氧化成乙酸
D.A使酸性KMnO4溶液褪色和使溴水褪色,其原理相同
查看答案和解析>>
科目: 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:实验题
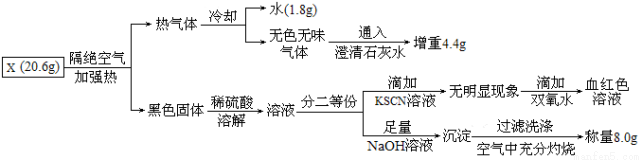
有一种埋在地下的矿物X(仅含四种元素),挖出后在空气中容易发黄,现探究其组成和性质,设计完成如下实验:
请回答:
(1)X的化学式_________ ________,挖出后在空气中容易发黄的原因______________。
________,挖出后在空气中容易发黄的原因______________。
(2)写出溶液分二等份,加KSCN无明显现象后,滴加双氧水的两个离子方程式:___________________,_________________。
查看答案和解析>>
科目: 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:实验题
某化学课外小组以海带为原料制取了少量碘水。现用四氯化碳从碘水中萃取碘并用分液漏斗分离这两种溶液,其实验操作可分为如下几步:
①检验分液漏斗活塞和上口玻璃塞是否漏液。
②把50 mL碘水和15 mL四氯化碳加入分液漏斗中,并盖好玻璃塞。
③倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正。
④把盛有溶液的分液漏斗放在铁架台的铁圈中。
⑤将漏斗上口的玻璃塞打开或使塞上的凹槽、小孔对准漏斗口上的小孔。
⑥静置,分层。
⑦旋开活塞,用烧杯接收溶液。
⑧从分液漏斗上口倒出上层水溶液。
回答下列问题:
(1)在上述实验过程中,不必要的玻璃仪器是____________。
A.烧杯 B.玻璃棒 C.胶头滴管 D.量筒
(2)步骤⑦的操作中最应注意的是:_______________________________,及时关闭旋塞。
(3)下列操作或说法正确的是______________。
A.分液漏斗使用前须检漏,方法是向漏斗中加水,观察水是否从漏斗口流出,若不流出,则不漏水
B.萃取后分液漏斗内观察到的现象是液体分二层,上层接近无色,下层紫红色
C.可以由苯代替四氯化碳,但不可以用乙醇
D.可以采用蒸馏的方法来进一步分离碘和四氯化碳
查看答案和解析>>
科目: 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:填空题
有一包铁粉和铜粉混合均匀的粉末样品,为确定其组成,某同学将不同质量的该样品分别与40 mL 1 mol·L-1的FeCl3溶液反应,实验结果如下表所示(忽略反应前后溶液体积的微小变化)。
实验序号 | ① | ② | ③ | ④ |
m(粉末样品)/g | 0.90 | 1.80 | 3.60 | 7.20 |
m(反应后剩余固体)/g | 0 | 0.64 | 2.48 | 6.08 |
计算:(1)样品中铁和铜的物质的量之比n(Fe)∶n(Cu)=_______________。
(2)实验②的滤液中c(Fe2+)=__________________。
查看答案和解析>>
科目: 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:填空题
研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)已 知:2SO2(g)+O2(g)
知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ·mol-1
2SO3(g) ΔH=-196.6kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0kJ·mol-1
2NO2(g) ΔH=-113.0kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=____________ kJ·mol-1。
SO3(g)+NO(g)的ΔH=____________ kJ·mol-1。
(2)一定条件下,将NO2与SO2以体积比2∶1置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是____________。
A.体系压强保持不变 B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变 D.每消耗1molSO3的同时生成1mol NO
若测得上述反应达平衡时NO2与SO2的体积比为5∶1,则平衡常数K= 。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g
CH3OH(g )。CO在不同温度下的平衡转化率与压强的关系如图甲所示。该反应ΔH________0(填“>”或“<”)。
)。CO在不同温度下的平衡转化率与压强的关系如图甲所示。该反应ΔH________0(填“>”或“<”)。
图甲: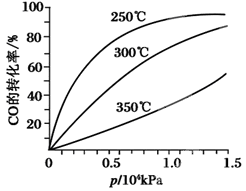 图乙:
图乙: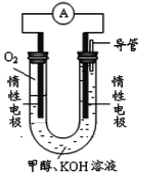
(4)依据燃烧的反应原理,合成的甲醇可以设计如图乙所示的原电池装置。
①该电池工作时,OH-向_______极移动(填“正”或“负”)。
②该电池正极的电极反应式为______________________。
查看答案和解析>>
科目: 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:实验题
实验室用下列方法测定某水样中O2的含量。
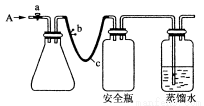
(1)用如上图所示装置,c是长橡胶管。使水中溶解的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为______________________。
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的________________。
②用注射器抽取20.00mL某水样从A处注入锥形瓶。
③再分别从A处注入含m mol NaOH的溶液及过量的MnSO4溶液。
④完成上述操作后,下面应进行的操作是___________。
A.微热锥形瓶 B.夹紧止水夹a、b C.充分振荡锥形瓶 D.继续通入N2
(2)用I-将生成的MnO(OH)2再还原为Mn2+,反应的离子方程式为:MnO(OH)2+2I-+4H+=Mn2++I2+3H2O
⑤接着④操作后,分别从A处注入足量NaI溶液及含n mol H2SO4的硫酸溶液。
⑥重复第④步操作。
(3)用Na2S2O3标准溶液滴定(2)中生成的I2,反应方程式为:I2+2Na2S2O3=2NaI+Na2S4O6
⑦取下锥形瓶,向其中加入2~3滴__________作指示剂。
⑧用 0.005mol·L-1 Na2S2O3滴定至终点,终点现象_______________________。
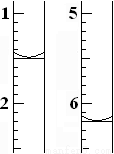
(4)滴定过程中,滴定前后滴定管中的液面读数如图所示。
⑨经计算,此水样中氧(O2)的含量为(单位:mg·L-1)_______________。
查看答案和解析>>
科目: 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:推断题
抑制结核杆菌的药物PAS-Na(对氨基水杨酸钠)的合成:
已知:
① (苯胺、弱碱性、易氧化)
(苯胺、弱碱性、易氧化)
②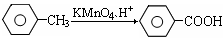
③R-Cl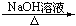 R-OH
R-OH
下面是PAS-Na的一种合成路线(部分反应的条件未注明):
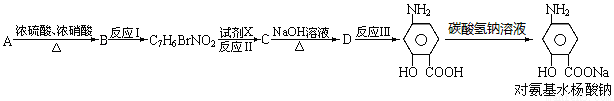
按要求回答问题:
(1)下列说法正确的是_______________;
A.化合物A只能发生氧化反应,不能发生还原反应
B.反应A →B为取代反应
C.反应II和反应III可以调换顺序
D.对氨基水杨酸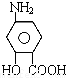 即能与酸反应,也能与碱反应
即能与酸反应,也能与碱反应
(2)写出反应:B→C7H6BrNO2的化学方程式_______________________;
(3)写出下列物质的结构简式:C:____________________;
(4)指出反应II中所加试剂X: ________________;反应III的反应类型:_______________;
(5)比化合物A多二个碳原子的A的同系物,写出同时符合下列条件的A的所有同分异构体的结构筒式:
①1H-NMR谱显示分子中含有苯环,且苯环上有一种不同化学环境的氢原子:_______________。
②1H-NMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com