
科目: 来源:2016-2017学年甘肃省嘉峪关市高二上学期期末考试化学试卷(解析版) 题型:选择题
现有常温下pH=3的醋酸和pH=3的硫酸两种溶液,下列叙述中正确的是 ( )
A. 两溶液中水电离出的c(H+)均为1×10-11mol·L-1
B. 加水稀释100倍后两溶液的pH仍相同
C. 醋酸中的c(CH3COO-)和硫酸中的c(SO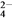 )相同
)相同
D. 等体积的两溶液中分别加入足量锌片时放出H2的体积相同
查看答案和解析>>
科目: 来源:2016-2017学年甘肃省嘉峪关市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列溶液中微粒浓度关系一定正确的是 ( )
A. 氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH )
)
B. pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+)
C. 0.1 mol·L-1的硫酸铵溶液中:c(NH )>c(SO
)>c(SO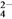 )>c(H+)
)>c(H+)
D. 0.1 mol·L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目: 来源:2016-2017学年甘肃省嘉峪关市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列各溶液中,微粒的物质的量浓度关系正确的是 ( )
A. 10 mL 0.5 mol·L-1CH3COONa溶液与6 mL 1 mol·L-1盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+)
B. 0.1 mol·L-1pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
C. 在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-)
D. 0.1 mol·L-1CH3COONa溶液中:c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目: 来源:2016-2017学年甘肃省嘉峪关市高二上学期期末考试化学试卷(解析版) 题型:简答题
常温下有浓度均为0.5mol/L的四种溶液:①Na2CO3、②NaHCO3、③HCl、④NH3·H2O.
(1)上述溶液中,可发生水解的是________(填序号,下同).
(2)向④中加入少量氯化铵固体,此时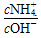 的值________(填“增大”、“减小”或“不变”).
的值________(填“增大”、“减小”或“不变”).
(3)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积________④的体积(填“大于”、“小于”或“等于”),此时溶液中离子浓度由大到小的顺序是__________________________.
(4)取10mL溶液③,加水稀释到500mL,则此时溶液中由水电离出的c(H+)=________.
查看答案和解析>>
科目: 来源:2016-2017学年甘肃省嘉峪关市高二上学期期末考试化学试卷(解析版) 题型:选择题
某温度(T)下的溶液中,c(H+)=10-xmol·L-1,c(OH-)=10-ymol·L-1,x与y的关系如图所示,请回答下列问题:
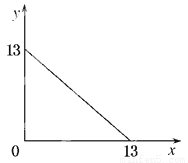
(1)此温度下,水的离子积KW为________,则该温度T________25℃(填“>”、“<”或“=”),pH=7的溶液显________性(填“酸”、“碱”或“中”)。
(2)若将此温度(T)下,pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合(假设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两种溶液的体积比。①若所得混合液为中性,则a:b=______;,②若所得混合液的pH=2,则a:b=______。
查看答案和解析>>
科目: 来源:2016-2017学年甘肃省嘉峪关市高二上学期期末考试化学试卷(解析版) 题型:简答题
已知在25℃时,Ksp[Mg(OH)2]=3.2×10-11,Ksp[Cu(OH)2]=2.0×10-20
(1)在25℃时,向0.02mol/L的MgCl2溶液中加入NaOH固体,如果生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为______mol/L;
(2)在25℃时,向浓度均为0.02mol/L的MgCl2和CuCl2混合溶液中逐滴加入NaOH溶液,先生成______沉淀(填化学式);生成该沉淀的离子方程式为_______;当两种沉淀共存时,c(Mg2+)/c(Cu2+)=________。
查看答案和解析>>
科目: 来源:2016-2017学年甘肃省嘉峪关市高二上学期期末考试化学试卷(解析版) 题型:简答题
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),图1表示该反应进行过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应进行过程中能量(单位为kJ·mol—1)的变化。
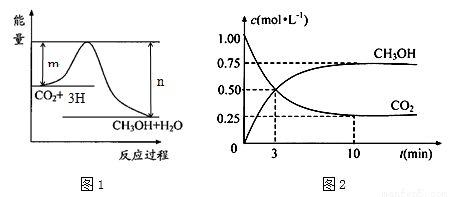
(1)写出该反应的热化学方程式__________________________。
(2)关于该反应的下列说法中,正确的是___________。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(3)该反应的平衡常数K的表达式为:________________。
(4)温度降低,平衡常数K____________(填“增大”、 “不变”或“减小”)。
(5)为探究反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1 molCO2和3 molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=______________________。
(6)下列措施中能使n(CH3OH)/n(CO2)增大的有____________。
A.升高温度 B.加入催化剂
C.将H2O(g)从体系中分离 D.充入He(g),使体系总压强增大
查看答案和解析>>
科目: 来源:2016-2017学年甘肃省嘉峪关市高二上学期期末考试化学试卷(解析版) 题型:实验题
实验室中有一瓶含有一定量杂质的烧碱样品,某学生用中和滴定法测定烧碱的纯度,若烧碱中所含杂质与酸不反应,请根据实验回答:

(1)将准确称取的5g烧碱样品配成100 mL待测液,需要的主要仪器除量筒、烧杯、
玻璃棒、托盘天平外,还必须用到的仪器有:____________、_____________。
(2)取10.00 mL待测液,选择右图中_________(填A或B)来移取。
(3)用0.5000mol/L标准盐酸滴定待测烧碱溶液,以酚酞为指示剂。滴定时左手
旋转滴定管玻璃活塞,右手不停地摇动锥形瓶,两眼注视___________________,
直到滴定终点。滴定达到终点的标志是:_______________________________。
(4)根据下列数据,烧碱的纯度为:_______________________

(5)判断下列操作引起的误差(填偏大、偏小或无影响)
①滴定前读数正确,滴定终点读数时仰视_________________
②装待测液前,锥形瓶内残留少量蒸馏水_______________
查看答案和解析>>
科目: 来源:2016-2017学年甘肃省嘉峪关市高二上学期期末考试化学试卷(解析版) 题型:简答题
某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
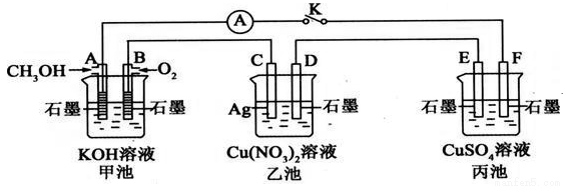
请回答下列问题:
(1)甲池为___________(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为____________________。
(2)丙池中F电极为___________(填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为___________________。
(3)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为________ml(标准状况)。
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是________(填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(0H)2CO3
查看答案和解析>>
科目: 来源:2016-2017学年安徽省六安市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列表述不正确的是( )
A. 人造刚玉熔点很高,可用作高级耐火材料,主要成分是Al2O3
B. 硅是制造太阳能电池的常用材料
C. 四氧敏化三铁俗称铁红.可用作油漆、红色涂料
D. 分散系中分散质粒子的直径:Fe(OH)3恳浊液> Fe(OH)3胶体>FeCl3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com