
科目: 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:推断题
我国从国外进口某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大。元素A、B、C、D、E的原子结构等信息如下:
元素 | 元素性质或原子结构 |
A | 周期表中原子半径最小的元素 |
B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
C | 最外层p轨道半充满 |
D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
E | 位于第四周期,内层电子全充满,且原子的最外层电子数与A的相同 |
请回答下列问题(用A、B、C、D、E所对应的元素符号作答):
(1)B、C、D第一电离能由小到大为_________________。
(2)E的基态原子的核外电子排布式为____________。
(3)A2B2D4常用作除锈剂,该分子中B的杂化方式为______________;1 mol A2B2D4分子中含有σ键数目为_____________。
(4)与化合物BD互为等电子体的阴离子化学式为_____________(任写一种)。
(5)B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是____________。
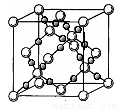
(6)BD2在高温高压下所形成晶体的晶胞如图所示。一个该晶胞中含___________个D原子。
查看答案和解析>>
科目: 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法错误的是( )
A. 食盐中加有碘,用其配成的溶液遇淀粉变蓝
B. 厕所清洁剂、食用醋、肥皂水、厨房清洁剂四种溶液的pH逐渐增大
C. 使用氯气自来水消毒时,氯气会与自来水中的有机物反应,生成的有机氯化物可能对人有害
D. 硅胶、生石灰、氯化钙等都是食品包装袋中常用的干燥剂
查看答案和解析>>
科目: 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:选择题
苯乙烯的结构为 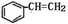 ,该物质在一定条件下能和氢气完全加成,加成产物的一溴取代物有( )
,该物质在一定条件下能和氢气完全加成,加成产物的一溴取代物有( )
A. 4种 B. 5种 C. 6种 D. 7种
查看答案和解析>>
科目: 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A. 化合物 的分子式为C13H9O4N2
的分子式为C13H9O4N2
B. 在碱性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH
C. 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应
D. 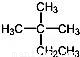 的系统命名为2﹣甲基﹣2﹣乙基丙烷
的系统命名为2﹣甲基﹣2﹣乙基丙烷
查看答案和解析>>
科目: 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:选择题
短周期元素a、b、c、d原子序数依次增大。a的核外电子总数与其周期数相同,b的某种单质是空气的主要成分,c的最外层电子数为其内层电子数的3倍,d与c同族;下列说法错误的是( )
A. a、b、d均可以与c形成两种或多种二元化合物
B. 阴离子的还原性d大于c
C. a与d形成的化合物可以抑制水的电离
D. 常温下,由这四种元素构成的某种盐的溶液pH=4,则水电离出的H+浓度肯定是1×10-4mol/L
查看答案和解析>>
科目: 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:选择题
为实现实验目的,选用的装置、实验操作均正确的是( )
实验目的 | 实验步骤和装置 | |
A | 探究温度对反应速率的影响 | 不同温度下,取0.1 mol/LKI 溶液,向其中先加入淀粉溶液,再加入0.1 mol/L 硫酸,记录溶液出现蓝色的时间 |
B | 配制100mL1.0mol/L NaOH溶液 | 向100mL容量瓶中加入4. 0gNaOH固体,加水到刻度线 |
C | 验证牺牲阳极的阴极保护法 |
往铁电极附近滴加铁氰化钾溶液 |
D | 比较H2O2 和Fe3+的氧化性 | 将盐酸酸化的双氧水滴入Fe(NO3)2溶液中 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:选择题
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,越来越成为人们研制绿色原电池的关注焦点.其中一种镁原电池的反应为:xMg+Mo3S4 MgxMo3S4,下列说法正确的是( )
MgxMo3S4,下列说法正确的是( )
A. 电池放电时,Mg2+向负极迁移
B. 电池放电时,正极反应为Mo3S4+2xe﹣+xMg2+═MgxMo3S4
C. 电池充电时,阴极发生还原反应生成Mo3S4
D. 电池充电时,阳极反应为xMg﹣2xe﹣═xMg2+
查看答案和解析>>
科目: 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:选择题
室温下,用0.100mol/L NaOH溶液分别滴定20.00mL 0.100mol/L 的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是( )

A. Ⅱ表示的是滴定醋酸的曲线
B. PH=7时,滴定醋酸消耗V(NaOH)小于20mL
C. V(NaOH)=20mL时,c(Cl﹣)=c(CH3COO﹣)
D. V(NaOH)=10mL时,醋酸溶液中:c(Na+)>c(CH3COO﹣ )>c(H+)>c(OH﹣ )
查看答案和解析>>
科目: 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:实验题
天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染.
资料:氰化钠化学式NaCN(C元素+2价,N元素﹣3价),白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢.
I、(1)NaCN水溶液呈碱性,其原因是____________(用离子方程式解释).
(2)双氧水氧化法除NaCN:碱性条件下加入H2O2,可得到纯碱和一种无色无味的无毒气体,该反应的离子方程式为____________________.
(3)非金属性N______C(填“<”、“>”或“=”),请设计实验证明:_____________。
II、某化学兴趣小组实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放.
[实验一]实验室通过如图装置制备Na2S2O3.
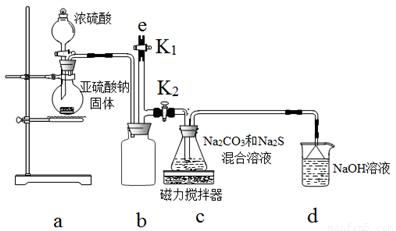
(3)b装置的作用是_______________.
(4)c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有__.
(5)实验结束后,在e处最好连接盛__(选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1防止拆除装置时污染空气.
[实验二]测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量.
己知:①废水中氰化钠的最高排放标准为0.50mg/L.
②Ag++2CN—=[Ag(CN)2] —,Ag++I—=AgI↓,AgI呈黄色,且CN —优先与Ag+反应.
实验如下.取25.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.000×10﹣4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50mL.
(6)滴定终点的判断方法是_______________.
(7)处理后的废水中氰化钠的含量为_______________mg/L.
查看答案和解析>>
科目: 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:简答题
铈元素(Ce)是镧系金属中自然丰度最高的一种,常见价态有+3、+4,铈的合金耐高温,可以用来制造喷气推进器零件。

(1)雾霾中含有大量的污染物NO,可以被Ce4+溶液吸收,生成NO2-、NO3-(二者物质的量之比为1∶1),该反应氧化剂与还原剂的物质的量之比为___________。
(2)可采用电解法将上述吸收液中的NO2-转化为无毒物质,同时再生Ce4+,其原理如右图所示。
①Ce4+从电解槽的__________(填字母序号)口流出。
②写出阴极的电极反应式____________________________。每消耗1mol NO2-,阴极区H+物质的量减少______mol。
(3)铈元素在自然中主要以氟碳矿形式存在,主要化学成分为CeFCO3,工业上利用氟碳铈矿提取CeCl3的一种工艺流程如下:
①焙烧过程中发生的主要反应方程式为______________________________________。
②酸浸过程中有同学认为用稀硫酸和H2O2替换盐酸更好,他的理由是_________________________。
③Ce(BF4)3、KBF4的Ksp分别为a、b,则Ce(BF4)3(s) + 3KCl(aq) 3KBF4(s) + CeCl3 (aq)平衡常数为______________________。
3KBF4(s) + CeCl3 (aq)平衡常数为______________________。
④加热CeCl3·6H2O和NH4Cl的固体混合物可得到无水CeCl3,其中NH4Cl的作用是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com