
科目: 来源:2017届江苏省常州市高三第一次模拟考试化学试卷(解析版) 题型:简答题
黄铜灰渣(含有Cu、Zn、CuO、ZnO及少量的FeO、Fe2O3)生产硝酸铜溶液的流程如下:
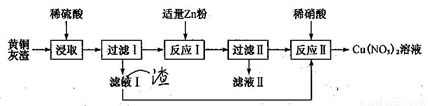
(1)写出酸浸时Fe2O3和稀硫酸反应的离子方程式:_________________。
(2)反应I中所加Zn不能过量的原因是________________。
(3)滤液II中含有的金属阳离子主要有_____________。
(4)写出反应II的离子方程式:______________。反应II应控制温度不能过高也不能过低的原因是___________________。
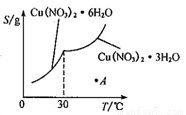
(5)已知Cu(NO3)2·6H2O和Cu(NO3)2·3H2O的溶解度随温度的变化如图所示。则由A点对应的溶液获取Cu(NO3)2·3H2O的方法是_______________。
查看答案和解析>>
科目: 来源:2017届江苏省常州市高三第一次模拟考试化学试卷(解析版) 题型:推断题
二甲氧苄氨嘧啶是一种用于家禽细菌感染防治药。其合成路线如下:
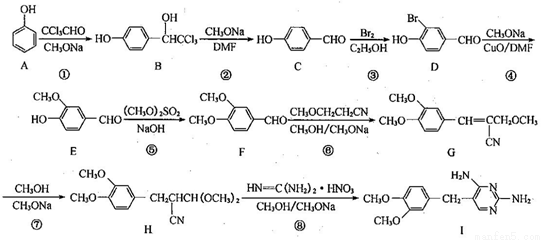
(1)化合物F的含氧官能团为_________(填官能团名称);合成路线中步骤①、④的反应类型分别是_____________。
(2)反应⑥先加成后消去,消去反应的化学方程式为____________。
(3)写出同时满足下列条件的E的同分异构体的结构简式:____________
I.核磁共振氢谱有5个峰
II.能发生银镜反应和酯化反应
Ⅲ.不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应
(4)实际生产的产品中存在一种结构为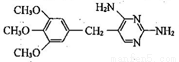 的副产物,为了使该副产物的含量降到最低,需将合成路线中第______步反应的工艺最优化。
的副产物,为了使该副产物的含量降到最低,需将合成路线中第______步反应的工艺最优化。
(5)已知: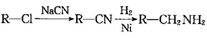 。化合物
。化合物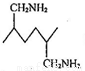 是合成染料的中间体,请写出以氯乙烷和1,2-二氯乙烷为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下______
是合成染料的中间体,请写出以氯乙烷和1,2-二氯乙烷为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下______
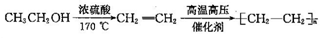
查看答案和解析>>
科目: 来源:2017届江苏省常州市高三第一次模拟考试化学试卷(解析版) 题型:填空题
碱式次氯酸镁[Mga(ClO)b(OH)c·xH2O]是一种有开发价值的微溶于水的无机抗菌剂。为确定碱式次氯酸镁的组成,进行如下实验:
① 准确称取1.685g碱式次氯酸镁试样于250mL锥形瓶中,加入过量的KI溶液,用足量乙酸酸化,用O.8000mol/LNa2S2O3标准溶液滴定至终点(离子方程式为2S2O32-+I2=2I-+S4O62-),消耗25.00mL。
② 另取1.685g碱式次氯酸镁试样,用足量乙酸酸化,再用足量3%H2O2溶液处理至不再产生气泡(H2O2被ClO-氧化为O2),稀释至1000mL。移取25.00mL溶液至锥形瓶中,在一定条件下用0.020 00mol/L EDTA(Na2H2Y)标准溶液滴定其中的Mg2+(离子方程式为Mg2++H2Y2-=MgY2-+2H+) ,消耗25.00 mL
(1)步骤① 中需要用到的指示剂是_______。
(2)步骤② 中若滴定管在使用前未用EDTA标准溶液润洗,测得的Mg2+物质的量将____(填“偏高”、“偏低”或“不变”)。
(3)通过计算确定碱式次氯酸镁的化学式(写出计算过程)。____
查看答案和解析>>
科目: 来源:2017届江苏省常州市高三第一次模拟考试化学试卷(解析版) 题型:实验题
过硫酸钾(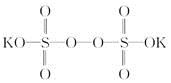 )具有强氧化性(常被还原为硫酸钾),80℃以上易发生分解。实验室模拟工业合成过硫酸钾的流程如下:
)具有强氧化性(常被还原为硫酸钾),80℃以上易发生分解。实验室模拟工业合成过硫酸钾的流程如下:
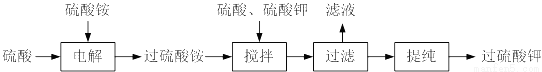
(1)硫酸铵和硫酸配制成电解液,以铂作电极进行电解,生成过硫酸铵溶液。写出电解时发生反应的离子方程式___________________。
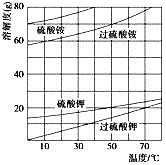
(2)已知相关物质的溶解度曲线如下图所示。在实验室中提纯过硫酸钾粗产品的实验具体操作依次为:将过硫酸钾粗产品溶于适量水中,___________,干燥。
(3)样品中过硫酸钾的含量可用碘量法进行测定。实验步骤如下:
步骤1:称取过硫酸钾样品0.3000g于碘量瓶中,加入30 mL水溶解。
步骤2:向溶液中加入4.000g KI固体(略过量),摇匀,在暗处放置30 min。
步骤3:在碘量瓶中加入适量醋酸溶液酸化,以淀粉溶液作指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,共消耗Na2S2O3标准溶液21.00mL。
(已知反应:I2+2S2O32-=2I-+S4O62-)
①若步骤2中未将碘量瓶“在暗处放置30 min”,立即进行步骤3,则测定的结果可能__________(选填“偏大”、“偏小”、“无影响”);上述步骤3中滴定终点的现象是__________。
②根据上述步骤可计算出该样品中过硫酸钾的质量分数为__________。
③为确保实验结果的准确性,你认为还需要____________________。
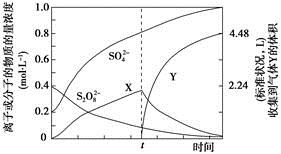
(4)将0.40mol过硫酸钾与0.20mol硫酸配制成1 L溶液,在80℃条件下加热并在t时刻向溶液中滴加入少量FeCl3溶液,测定溶液中各成分的浓度如图所示(H+浓度未画出)。图中物质X的化学式为
__________。
查看答案和解析>>
科目: 来源:2017届江苏省常州市高三第一次模拟考试化学试卷(解析版) 题型:填空题
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH1=+489.0kJ·mol-1,
C(s) +CO2(g)=2CO(g) ΔH2=+172.5kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为_________ 。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:_________ 。
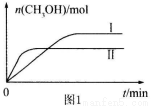
(3)CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g) +3H2(g) CH3OH(g) +H2O(g)测得CH3OH的物质的量随时间的变化见图1。
CH3OH(g) +H2O(g)测得CH3OH的物质的量随时间的变化见图1。
①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ KⅡ(填“>”或“=”或“<”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容器 | 甲 | 乙 |
反应物投入量 | 1 mol CO2、3 mol H2 | a mol CO2、b mol H2 |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为 。
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化见图2。在0~15小时内,CH4的平均生成速率Ⅰ、Ⅱ和Ⅲ从大到小的顺序为 (填序号)。

(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图3。
①乙酸的生成速率主要取决于温度影响的范围是__________________。
②Cu2Al2O4可溶于稀硝酸,写出有关的离子方程式:________________________。
查看答案和解析>>
科目: 来源:2017届江苏省常州市高三第一次模拟考试化学试卷(解析版) 题型:简答题
铁是最常见的金属材料。铁能形成[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)〕 和Fe(CO)x等多种配合物。
(1)基态Fe3+的核外电子排布式为_____,与NO3-互为等电子体的分子是__________。
(2)尿素(H2NCONH2)分子中C、N原子的杂化方式依次为______。C、N、O三种元素的第一电离能由大到小的顺序是______。
(3)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=______。Fe(CO)x常温下呈液态,熔点为-20 .5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于_______(填晶体类型)。
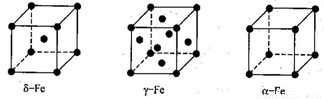
(4)铁有δ、γ、a三种同素异形体,δ、γ、a三种晶胞中铁原子的配位数之比为_______。
查看答案和解析>>
科目: 来源:2017届安徽省淮南市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
化学与社会、生活密切相关。对下列现象或事实的解释错误的是
选项 | 现象或事实 | 解释 |
A | 用浸有酸性高锰酸钾溶液的硅藻土作水果保鲜剂 | 酸性高锰酸钾溶液能氧化水果释放的催熟剂乙烯 |
B | 加热能杀死流感病毒 | 病毒的蛋白质受热变性 |
C | 过氧化钠作呼吸面具中的供氧剂 | 过氧化钠既是氧化剂,又是还原剂 |
D | Al(OH)3用作塑料的阻燃剂 | A(OH)3受热易分解,产生水吸收热量 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源:2017届安徽省淮南市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
用NA为阿伏伽德罗常数的数值,下列叙述正确的是
A. 1mol/L氯化铜溶液中的Cu2+数小于NA
B. 28 g聚乙烯含有的碳原子数为2NA
C. 标准状况下,22.4 L Cl2与水反应转移的电子数为NA
D. 惰性电极电解食盐水,若线路中通过2NA电子电量,则阳极产生气体22.4L
查看答案和解析>>
科目: 来源:2017届安徽省淮南市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
下列关于有机物的叙述正确的是
A. 石油干馏可得到汽油、煤油等
B. 乙酸乙酯、油脂与NaOH溶液反应均有醇生成
C. 淀粉、蛋白质完全水解的产物互为同分异构体
D. 苯不能使酸性KMnO4溶液褪色,因此苯不能发生氧化反应
查看答案和解析>>
科目: 来源:2017届安徽省淮南市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
下列有关实验操作和结论均正确的是
选项 | 操作 | 结论 |
A | 配制Fe(NO3)2溶液时加入适量的硝酸 | 抑制Fe2+水解 |
B | 浓硫酸和蔗糖反应产生的气体通过足量的KMnO4溶液,气体全部被吸收且溶液紫红色褪去 | “黑面包实验”产生的气体具有还原性 |
C | 往溶液中滴加NaOH溶液,将湿润红色石蕊试纸置于试管口试纸不变蓝 | 原溶液中无NH4+ |
D | 幼儿使用含NaF的牙膏,可以使牙齿上的Ca5(PO4)3OH转化为Ca5(PO4)3F,防止蛀牙 | Ksp[Ca5(PO4)3F]<Ksp[Ca5(PO4)3OH] |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com