
科目: 来源:2016-2017学年广东省湛江市高二上学期期末调研考试化学试卷(解析版) 题型:简答题
(1)固体氧化物燃料电池的工作原理如图所示,已知电池中电解质为熔融固体氧化物,O2-可以在其中自由移动。当燃料气为C2H4时,其正极、负极反应式分别为
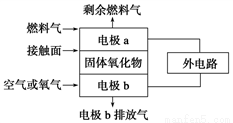
正极:______________________;
负极:____________________。
(2)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,则Co2+在阳极的电极反应式为__________________;除去甲醇的离子方程式为___________。
(3)如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。
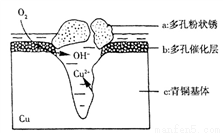
①环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为______________________;
②若生成4.29 g Cu2(OH)3Cl,则理论上耗氧气体积为___________L(标准状况)。
查看答案和解析>>
科目: 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:选择题
化学与生活、生产、可持续发展密切相关,下列说法中正确的是
A. 14C可用于文物年代的鉴定,14C和12C互为同素异形体
B. 在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因
C. 高纯度的SiO2可以制成光电池将光能直接转化为电能
D. 现代工业生产中芳香烃主要来源于石油化工的催化重整和煤的干馏
查看答案和解析>>
科目: 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述错误的是
A. 分子总数为NA的NO2和CO2的混合气体中含有的氧原子数为2 NA
B. 0.1 mol/L (NH4)2SO4溶液与0.2 mol/L NH4Cl溶液中的NH4+数目相同
C. 标准状况下,H2和CO混合气体8.96 L在足量O2中充分燃烧消耗O2分子数为0.2 NA
D. 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
科目: 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:选择题
下列关于有机物的叙述正确的是
A. 乙烯、聚氯乙烯和苯分子中均含有碳碳双键
B. 苯、油脂均不能使酸性KMnO4溶液褪色
C. 氯苯分子中所有原子都处于同一平面
D. 甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种
查看答案和解析>>
科目: 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:选择题
下列操作及解释都正确的是
选项 | 应用 | 解释 |
A | 在相同条件下,在两支试管中各加入2 mL 5% H2O2溶液,再向H2O2溶液中分别滴入1 mL H2O和1 mL 0.1 mol·L-1 FeCl3溶液,对比观察现象 | 可以探究催化剂FeCl3对H2O2 分解速率的影响 |
B | 向盛有1mL 0.01 mol·L-1 AgNO3溶液的试管中滴加5滴0.01 mol·L-1 NaCl溶液,有白色沉淀生成,再向其中滴加0.01 mol·L-1 KI溶液,产生黄色沉淀。 | 常温下,Ksp(AgCl)> Ksp(AgI) |
C | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液,均有固体析出 | 蛋白质均发生变性 |
D | 保存硫酸亚铁溶液需加入少量稀盐酸和铁钉 | 防止 Fe2+水解以及被 O2 氧化 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:选择题
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法错误的是
A. 原子半径:W>X>Y>Z>M
B. XZ2为直线形的共价化合物
C. X、Y、Z 分别与M元素形成的最简单化合物的沸点依次升高
D. 由X、Y、Z、M四种元素形成的化合物一定含有离子键和共价键
查看答案和解析>>
科目: 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:选择题
用NaOH溶液吸收尾气中的SO2,将所得的Na2SO3溶液进行电解再生循环脱硫,其原理如图,a、b离子交换膜将电解槽分成为三个区域,电极材料均为石墨。甲~戊分别代表生产中的原料或产品,其中丙为硫酸溶液。下列说法错误的是
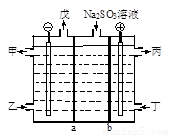
A. 图中a表示阳离子交换膜
B. 当电路中通过1mol电子的电量时,会有0.25mol的O2生成
C. 甲为NaOH溶液
D. 阳极的电极反应式为SO32-+H2O-2e-=SO42-+2H+
查看答案和解析>>
科目: 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:选择题
25℃时,向10 mL 0.1 mol·L-1 H2A溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示。下列叙述错误的是
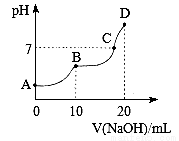
A. C点溶液中含有NaHA和Na2A
B. NaHA溶液中水的电离程度比Na2A溶液中小
C. B点,c (Na+)=2[c (H2A)+c (HA)+c (A2-)]
D. D点,c (Na+)>c (A2-)>c (OH-)>c (HA-)>c (H+)
查看答案和解析>>
科目: 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:实验题
已知硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O] (俗称莫尔盐)可溶于水,在100℃~110℃时分解。为探究其化学性质,甲、乙两同学设计了如下实验。
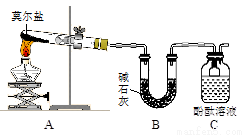
Ⅰ.探究莫尔盐晶体加热时的分解产物。
甲同学设计如右图所示的装置进行实验,装置C中可观察到的现象是____________________,由此可知分解产物中有_______________。
乙同学认为莫尔盐晶体分解的产物中还可能含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验。
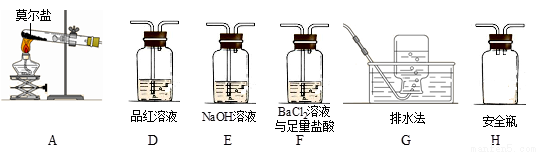
①乙同学的实验中,装置依次连接的合理顺序为:A→H→(____)→(____)→(____)→G。
②证明含有SO3的实验现象是______________;安全瓶H的作用是____。
Ⅱ.为测定硫酸亚铁铵纯度,称取m g莫尔盐样品,配成500 mL溶液。甲、乙两位同学设计了如下两个实验方案。甲方案:取25.00 mL样品溶液用0.1000 mol·L-1的酸性K2Cr2O7 溶液分三次进行滴定。乙方案:(通过NH4+测定)实验设计装置如下图所示。取25.00 mL样品溶液进行该实验。
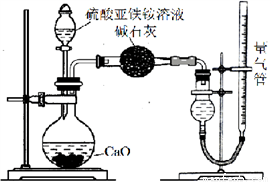
请回答:
(1)甲方案中的离子方程式为:________________________。
(2)乙方案中量气管中最佳试剂是________
a.水 b.饱和NaHCO3溶液 c.CCl4
(3)乙方案中收集完气体并恢复至室温,读数前应进行的操作是________________。
(4)若测得NH3为V L(已折算为标准状况下),则硫酸亚铁铵纯度为_____(列出计算式)。
查看答案和解析>>
科目: 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:实验题
从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是______(填字母序号)。
a.Fe b.FeO c.Fe3O4 d.Fe2O3
(2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
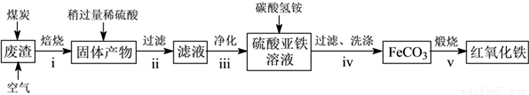
回答下列问题:
①在步骤i中产生的有毒气体可能有__________________。
②在步骤iii操作中,要除去的离子之一为Al3+。若常温时Ksp[Al(OH)3]=1.0×10-32,此时理论上将Al3+沉淀完全,则溶液的pH为____________。
③步骤iv中,生成FeCO3的离子方程式是_________________。
(3)氯化铁溶液称为化学试剂中的“多面手”,向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式_________________。请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释:___________________。
(4)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应ii的离子方程式是________________。
②如今基于普鲁士蓝合成原理可检测食品中CN-,方案如下:
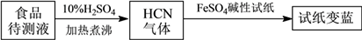
若试纸变蓝则证明食品中含有CN-,请解释检测时试纸中FeSO4的作用:
_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com