
科目: 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是:
X | Y | Z | |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液 | SiO2 | 浓盐酸 |
③ | FeCl3溶液 | Cu | 浓硝酸 |
④ | O2 | N2 | H2 |
A. ①③ B. ①④ C. ②④ D. ②③
查看答案和解析>>
科目: 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
下列有关工业生产的叙述中,不正确的是:
A. 电解氧化铝时,用冰晶石降低其熔点 B. 制玻璃时,常加入氧化铁以降低生产成本
C. 添加必要的元素可提高钢材的性能 D. 催化裂化可提高汽油的产量
查看答案和解析>>
科目: 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
如图是某同学设计的原电池装置,下列叙述中正确的是:
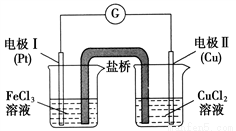
A. 电极Ⅰ上发生还原反应,作原电池的负极
B. 电极Ⅱ的电极反应式为:Cu2++2e-===Cu
C. 该原电池的总反应为:2Fe3++Cu===Cu2++2Fe2+
D. 盐桥中装有含氯化钾的琼脂,其作用是传递电子
查看答案和解析>>
科目: 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
若NA表示阿佛加德罗常数,下列说法正确的是:
A. 14 g 氮气中含有7NA个电子
B. 1 mol Cl2作为氧化剂得到的电子数为NA
C. 标准状况下,2. 24 L的CCl4中含有的C—Cl键数为0. 4NA
D. 常温常压下,3. 0 g含甲醛的冰醋酸中含有的原子总数为0. 4NA
查看答案和解析>>
科目: 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是:
A. Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
B. 水晶、干冰熔化时克服粒子间作用力的类型相同
C. Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
D. 钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1 :2
查看答案和解析>>
科目: 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
下列叙述I和II均正确并且有因果关系的是:
选项 | 叙述I | 叙述II |
A | SiO2可与HF反应 | 氢氟酸不能保存在玻璃瓶中 |
B | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
C | 溶解度:CaCO3 < Ca(HCO3)2 | 溶解度:Na2CO3 < NaHCO3 |
D | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
太阳能电池板面对太阳时,一部分电能直接供给“天宫一号”,一部分电能则储存在电池里,供背离太阳时使用。“天宫一号”使用的是镍氢电池,电解质溶液显碱性。其反应方程式为: LaNi5+Ni(OH)2 LaNi5H+NiOOH。下列有关说法不正确的是
LaNi5H+NiOOH。下列有关说法不正确的是
A. 放电时镍被还原 B. 放电时负极LaNi5H+OH——e—=LaNi5+H2O
C. 充电时OH—向阴极移动 D. 充电时每消耗lmol Ni(OH)2转移lmol电子
查看答案和解析>>
科目: 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
一定温度下,体积不变的密闭容器中,对可逆反应A(g) + 2B(g)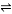 3C(g) + D(s) 的下列叙述中,能说明反应已达到平衡的是:
3C(g) + D(s) 的下列叙述中,能说明反应已达到平衡的是:
A. 单位时间内消耗a mol A,同时生成3a mol C
B. C的生成速率与C的分解速率相等
C. 混合气体的总物质的量不再变化
D. 容器内的压强不再变化
查看答案和解析>>
科目: 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
合成氨的热化学方程式为:N2(g) + 3H2(g) 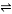 2NH3(g);△H = -92. 4 kJ/mol。现将1 mol N2 (g)、3 mol H2 (g) 充入一容积为2 L的密闭容器中,在500 ℃下进行反应,第10 min时达到平衡,NH3的体积分数为 ω,下列说法中正确的是:
2NH3(g);△H = -92. 4 kJ/mol。现将1 mol N2 (g)、3 mol H2 (g) 充入一容积为2 L的密闭容器中,在500 ℃下进行反应,第10 min时达到平衡,NH3的体积分数为 ω,下列说法中正确的是:

A. 若达到平衡时,测得体系放出9. 24 kJ热量,则H2反应速率变化曲线如图a所示
B. 如图b所示,容器Ⅰ和Ⅱ达到平衡时,NH3的体积分数为ω,则容器Ⅰ放出热量与容器Ⅱ吸收热量之和为92. 4 kJ
C. 反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为P,三者关系如图c
D. 若起始加入物料为1 mol N2、3 mol H2,在不同条件下达到平衡时,NH3的体积分数变化如图d所示
查看答案和解析>>
科目: 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:填空题
X、Y、Z、W四种短周期元素在周期表中的位置关系如右图所示,其中Z元素原子的最外层电子数是其电子层数的2倍。
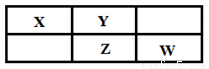
请回答下列问题:
(1)元素Z位于周期表中第_______周期,________族;
(2)这些元素的最高价氧化物对应的水化物中,水溶液酸性最强的是_______(写化学式);
(3)Y和Z组成的化合物的化学式为_______;
(4)W的单质和过量的X的氢化物可发生氧化还原反应,所得两种产物的电子式分别为____________、___________;
(5)W的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol 电子转移时,共产生9 mol 气体,写出该反应的化学方程式___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com