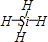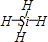四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z原子与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1.
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,a的分子式是
CH4
CH4
,b的结构式是
;中心原子的杂化轨道类型分别是
sp3
sp3
、
sp3
sp3
;a分子的立体结构是
正四面体
正四面体
;
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是
分子
分子
晶体、
原子
原子
晶体;
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)
CO2
CO2
;
(4)Y与Z比较,电负性较大的是
C
C
;
(5)W的元素符号是
Zn
Zn
,其+2价离子的核外电子排布式是
1s22s22p63s23p63d10
1s22s22p63s23p63d10
.