
科目: 来源: 题型:
【题目】本题为《化学与生活(选修1)》选做题,
(一)“北京烤鸭”举世闻名。制作烤鸭套餐的部分原料如下:① 鸭肉、② 面粉、③ 黄瓜、④ 食盐。请回答:
(1)富含淀粉的是 (填序号,下同)。(2)富含蛋白质的是 。
(3)富含维生素的是 。 (4)属于调味剂的是 。
(二).材料是人类赖以生存和发展的重要物质基础。
(1)试管、烧杯和烧瓶等化学仪器的主要材质是 ;
A.玻璃 B.陶瓷
(2)钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为 ;
A.O2+2H2O + 4e- = 4OH- B.Fe - 2e -= Fe2+
(三)含汞废水主要来源于氯碱工业和塑料工业,未经处理不得排放。某含汞酸性废水(主要含Hg2+、H+、Na+、Cl-等)的处理工艺流程如下图所示。
 请回答:
请回答:
(1)含汞废水未经处理直接排放的危害是 (填字母)。
a. 造成水体污染 b. 引起人体中毒
(2)调节废水pH时加入的溶液A可能是 (填字母)。
a. 盐酸 b. NaOH溶液
(3)Na2S与Hg2+发生反应的离子方程式是 。
(4)该废水经处理后,测得有关数据如下(其他离子忽略不计):
离子 | Na+ | Fe2+ | Cl- | SO42- |
浓度(mol/L) | 3.0×10-4 | 2.0×10-4 | 2.5×10-4 |
则c(Fe2+) = mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z三种短周期元素,它们的原子序数之和为16 。X、Y、Z三种元素常见单质在常温下都是无色气体,在适当条件下可发生如下图所示变化:

已知一个B分子中含有的Z元素的原子个数比C分子中的少一个。
请回答下列问题:
(1)X元素在周期表中的位置是______________________。
(2)X的单质与Z的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入__________(填物质名称);负极电极反应式为____________________。
(3)C在一定条件下反应生成A的化学方程式是_______________________________。
(4)已知Y的单质与Z的单质生成C的反应是可逆反应,△H<0。将等物质的量的Y、Z的单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。下列说法中,正确的是____________________(填写下列各项的序号)。
a.达到化学平衡时,正反应速率与逆反应速率相等
b.反应过程中,Y的单质的体积分数始终为50%
c.达到化学平衡时,Y、Z的两种单质在混合气体中的物质的量之比为1:1
d.达到化学平衡的过程中,混合气体平均相对分子质量减小
e.达到化学平衡后,再升高温度,C的体积分数增大
查看答案和解析>>
科目: 来源: 题型:
【题目】)实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
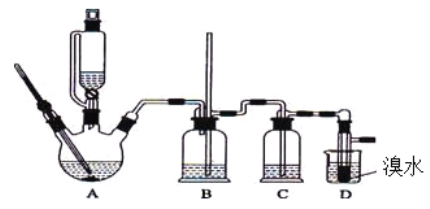
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -l30 | 9 | -1l6 |
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式 。
(2)装置B的作用是__________________________。
(3)在装置C中应加入 (填字母)。
a.水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.氢氧化钠溶液
(4)若产物中有少量未反应的Br2,最好用 (填字母)洗涤除去。
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚,可用 的方法除去。
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是
。
(7)判断该制备反应已经结束的最简单方法是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】在四个不同容器中,不同条件下进行合成氨反应.根据在相同时间内测定的结果判断生成氨的速率最快的是( )
A.v(N2)=0.1molL﹣1s﹣1 B.v(H2)=0.1molL﹣1min﹣1
C.v(NH3)=0.15molL﹣1min﹣1 D.v(H2)=0.3molL﹣1min﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)苯、四氯化碳、乙醇都是常见的有机溶剂。能与水互溶的是 ;难溶于水,且密度比水小的是 。
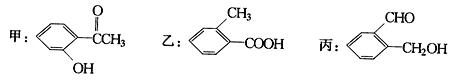
(2)现有化合物:
①请写出丙中含氧官能团的名称: 。
②请判别上述哪些化合物互为同分异构体: (填代号)。
(3)同温同压下,相同体积某烷烃的蒸气质量是氢气质量的36倍,该烃的分子式为____________,写出该烃的所有同分异构体的结构简式: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物B是一种相对分子质量不超过120的芳香烃含氧衍生物,期中含氧的质量分数为14.8%,B与NaOH溶液不发生反应。有机物A在一定条件下可发生反应
A+H2O B+C。有关C的转化关系如下图所示:
B+C。有关C的转化关系如下图所示:
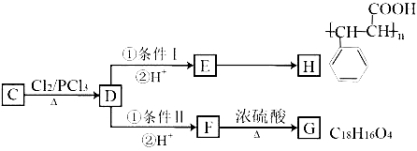
已知:![]()
根据以上信息,回答下列问题:
(1)B的结构简式为 ,条件I、II中均需要的试剂为 。
(2)有关C的转化关系图中所发生的反应中属于取代反应的有 个。
(3)C的同分异构体中,同时符合下列要求的物质有 种。
a.苯环上有两个侧链 b.能发生银镜反应 c.能发生消去反应
(4)写出F→E转化的化学方程式
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如下图所示装置进行有关实验。

(1)装置A中发生反应的化学方程式为____________________________。
(2)装置D中试管口放置的棉花应浸一种溶液,这种溶液是________,其作用是________________________。
(3)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是_______________,
(4)实验中,取一定质量的铜片和一定体积18 mol·L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,其原因是______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】【选修2:化学与技术】
地球的海水问题约有1.4×1018t,是人类最大的资源库。
(1)如下图1利用海水得到淡水的方法是___________________________;
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如图2所示.a是电源的_________极;Ⅰ口排出的是__________(填“淡水”或“浓水”).
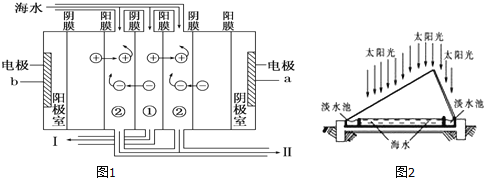
(3)海水淡化后的浓水中含大量盐分(主要含有Mg2+、Ca2+、Fe3+和SO42-),排入水中会改变水质,排到土壤中会导致土壤盐碱化,故不能直接排放,可以与氯碱工业联产.电解前需要把浓水精制,所需试剂主要包括:HCl、NaOH、BaCl2、Na2CO3等),其中HCl的作用主要是__________________________;
(4)铀是核反应最重要的燃料,其提炼技术直接关系着一个国家核工业或核武器的发展水平,海水中铀以UCl4形式存在(以离子形式存在),每吨海水只含3.3毫克铀,海水总量极大,铀总量相当巨大.不少国家正在探索海水提铀的方法.现在,已经研制成功一种螯合型离子交换树脂,它专门吸附海水中的铀,而不吸附其他元素.其反应原理为_______________________ (树脂用HR代替),发生离子交换后的离子交换膜用酸处理还可再生并得到含铀的溶液,其反应原理为_________________________;
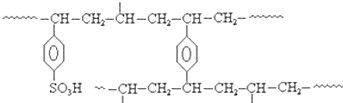
(5)离子交换树脂法是制备纯水(去离子水)的主要方法.某阳离子交换树酯的局部结构可写成(如图).该阳离子交换树脂是由单体苯乙烯和交联剂对二乙烯基苯聚合后再经_____________反应得到的.自来水与该离子交换树脂交换作用后显____________(填“酸性”、“碱性”或“中性”).
(6)中国《生活用水卫生标准》中规定,水的总硬度不能过大.如果硬度过大,饮用后对人体健康与日常生活有一定影响.暂时硬水的硬度是由__________(填阴离子符号)引起的,经___________(填操作名称)后可被去掉.永久硬水的硬度可由离子交换法去掉。
查看答案和解析>>
科目: 来源: 题型:
【题目】【选修3:物质结构与性质】
在电解冶练铝的过程中加入冰晶石,可起到降低Al2O3熔点的作用。冰晶石的生产原理为2Al(OH)3+12HF+3Na2CO3═2Na3AlF6+3CO2↑+9H2O.根据题意完成下列填空:
(1)冰晶石的晶体不导电,但熔融时能导电,则在冰晶石晶体中存在__________(填序号).
a.离子键 b.极性键 c.配位键 d.范德华力
(2)CO2分子的空间构型为__________,中心原子的杂化方式为__________,和CO2 互为等电子体的氧化物是__________;
(3)反应物中电负性最大的元素为_________(填元素符号),写出其原子最外层的电子排布图__________;
(4)冰晶石由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是______(填具体的微粒符号).

(5)Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:
若已知Al的原子半径为d cm,NA代表阿伏伽德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目为_________个;Al晶体的密度为__________(用字母表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是
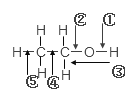
(1)和金属钠作用时,断裂______
(2)和浓硫酸共热至170 ℃时,断裂______
(3)和乙酸、浓硫酸共热时,断裂_______
(4)在铜催化下和氧气反应时,断裂_____
(5)与氢卤酸反应时,断裂______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com