
科目: 来源: 题型:
【题目】A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去):
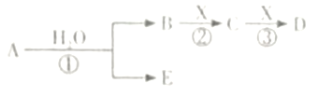
(1)若D为白色胶状难溶物,且与A摩尔质量相等,反应③的离子方程式为: 。
(2)若A为CO,则D的化学式为 。
(3)若C为当今需要减排的一种常见的温室气体,E为一种弱酸(无氧酸),则A的化学式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是以石油为原料制备某些化工产品的部分流程。请回答:

(1)写出反应②的化学方程式__________。
(2)B分子中无甲基,则B的结构简式为__________。系统命名为__________。
(3)反应①和③的类型依次是__________、__________。
(4)写出反应③化学方程式是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物。室温为非活性物质。温度升高后变得活泼。在空气中氧化成三氧化二铁和二氧化硫,主要用于接触法制造硫酸:

回答下列问题:
(1)在FeS2中的S2-的核外电子排布式是________________________;
(2)常温下Fe3+比Fe2+要更加稳定的原因是__________________________________;
(3)将FeS2与稀盐酸反应得到H2S2,H2S2分子中,共价键的类型是___________________;FeS2氧化得到SO2,在SO2分子中的S原子的杂化轨道类型是______________________ ,写出两个与SO2互为等电子体的分子或离子_______________________。-
(4)H2SO4和H2SO3都是S的含氧酸,请用结构知识解释H2SO4比H2SO3酸性强的原因:
_____________________________________________________________________。
(5)FeS2的晶体中的Fe2+离子的排列方式如下图。
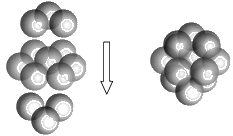
①每个Fe2+周围最近的等距离的S22-离子有____________个。
②已知FeS2的晶胞参数是a0=0.54nm,它的密度为_____________________g·cm-3(列式并计算,阿伏加德罗常数为6.02×1023)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在298K,100kPa时.CH4的燃烧热是890.0kJ/mol,写出该反应的热化学方程式__________。现有CH4和CO的混合气体0.75mol,完全燃烧后,生成CO2气体和18g液态水,共放出QkJ热量(假定热量未损失),则CH4和CO的物质的量的比为__________。
(2)利用甲烷的燃烧反应设计一个燃料电池,用氢氧化钾溶液作电解质溶液.多孔石墨作电极,在电极上分别通入甲烷和氧气,通入甲烷气体的电极上发生的电极反应是___________,当电路中转移12mol电子时,实际提供的电能是890.0kJ,则该电池的能量转化效率是__________。
(3)将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中形成如图装置:
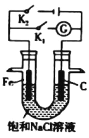
①当开关K1闭合,则铁发生电化学腐蚀中的__________腐蚀。
②当开关K2闭合,则总反应的离子方程式为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知前四周期六种元素A、B、C、D、E、F的核电荷数依次增大。B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成AC型离子化合物,其中的阴、阳离子相差一个电子层.E4+离子和氩原子的核外电子排布相同,F元素含量决定了人体内血红蛋白携氧能力的大小。请回答:
(1)A、B、C、D的第一电离能由小到大的顺序是__________(用元素符号填空)
(2)化合物BD3的分子构型为__________,B的原子轨道杂化类型为__________。B元素氢化物的沸点低于其同族上周期元素的氢化物的原因是__________。
(3)己知F2+与KCN溶液反应得F(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物.则F的基态原子价电子排布式为__________,CN-与__________(一种分子)互为等电子体.消除CN-剧毒性的方法之一是加入浓的双氧水,可将其转化为可溶性碳酸盐及氨气,写出该反应的离子方程式:__________。
(4)①E基态原子的价电子排布为__________,②EO2与碳酸钡在熔融状态下反应,所得晶体的晶胞结构如图所示,则该反应的化学方程式为__________。
③已知该晶体的摩尔质量为M(g/mol),其中E4+的氧配位数为__________。若该晶胞边长为anm,可计算该晶体的密度为__________g/cm3(阿伏加德罗常数为NA)。

查看答案和解析>>
科目: 来源: 题型:
【题目】已知X、Y、Z、W、V、U是短周期的主族元素,原子序数依次增大。X与V同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y与U同主族且Y原子的L层电子数是K层电子数的2倍。试回答下列问题:
(1)写出U元素在周期表中的位置 ;V离子结构示意图为 ;YW2的电子式 。
(2)Y、U的简单氢化物的稳定性由弱到强的顺序是 。
(3)V的最高价氧化物的水化物不能使用玻璃塞试剂瓶盛放的原因是 。(用化学方程式表示)
(4)由X、Z组成的一种化合物化学式为ZX5,其各原子均达到同周期稀有气体原子的稳定结构,该物质属于 (填“离子”或“共价”)化合物。
(5)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量氢氧化钠溶液在加热条件下反应的离子方程式为: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】【化学—选修3: 物质结构与性质】钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为________________。
②Fe的基态原子共有________种不同能级的电子。
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4===2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由大到小的顺序是______________(用元素符号表示)。
②COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为________,中心原子的杂化方式为________。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2 nm和7.8×10-2 nm。则熔点:NiO________(填“>”、“<”或“=”)FeO。
(4)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。
该合金的晶胞结构如图所示。

①该晶体的化学式为________________。
②已知该晶胞的摩尔质量为M g·mol-1,密度为d g·cm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是________ cm3(用含M、d、NA的代数式表示)。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定。已知:a=511 pm,c=397 pm;标准状况下氢气的密度为8.98×10-5 g·cm-3;储氢能力=![]() 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_______。
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增。B原子的P轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的。D原子得到一个电子后3P轨道全充满。A+比D原子形成的离子少一个电子层。C与A形成A2C型离子化合物。E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体。根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为 (用元素符号表示)。
(2)化合物BD3的分子空间构型是 。
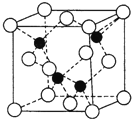
(3)上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED),其材料是E与F形成的化合物甲(属于第三代半导体),用它制造的灯泡寿命是普通灯泡的100倍,而耗能只有其10%。化合物甲的晶胞结构如右图(白球代表F,黑球代表E)。试回答:
①该晶胞中所包含的F原子(白色球)个数为 。
②与同一个E原子相连的F原子构成的空间构型为 。
③下列说法正确的是 。
A.该晶胞结构与NaCl相同 B.半导体EB与EF互为等电子体
C.电负性:F>E D.EF晶体中含有配位键
④ (CH3)3E中E原子的杂化方式为 。
⑤该晶体中紧邻的F原子之间与紧邻的F、E两原子之间距离的比值为 (写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,请参照元素
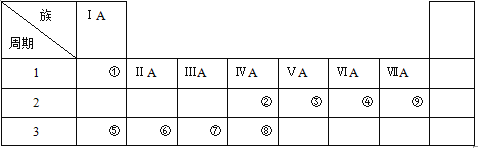
(1)①~⑨中金属性最强的元素是(填元素符号) ,非金属性最强的元素是(填元素符号) 。
(2)④、⑤、⑦的原子半径由大到小的顺序为(填元素符号) 。
(3)②、③的最高价氧化物的水化物的酸性强弱顺序为(填化学式) 。
(4)由①、④元素按原子个数比2:1组成的化合物的电子式为 。
(5)由②和④组成的化合物与⑥单质反应的化学方程式为 。
(6)⑦单质与⑤的最高价氧化物的水化物反应的离子方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)煤是宝贵的化石燃料,但是将煤直接作为燃料太浪费!可以通过煤的______获得焦炭、煤焦油和出炉煤气等产品。煤的气化是指将煤在高温下与水接触转变为可作为工业或民用燃料以及化工合成原料的煤气,请写出煤的气化的化学反应方程式:_________________。
(2)把A1和Fe2O3组成的铝热剂充分反应后的固体分成两等份,一份与足量的NaOH溶液反应生成标况下6.72升的气体,另一份与足量的HCl溶液反应生成标况下17.92升的气体。则铝热反应的方程式为____________________,原铝热剂中铝为______克。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com