
科目: 来源: 题型:
【题目】质谱图表明某有机物的相对分子质量为70,红外光谱表明有C==C和C==O的存在,1H核磁共振谱如下图(峰面积之比依次为1:1:1:3):分析核磁共振谱图,回答下列问题:
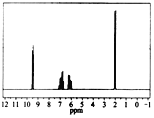
(1)分子中共有 种化学环境不同的氢原子。
(2)该物质的分子式为 。
(3)该有机物的结构简式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知3.6g碳在6.4g氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知1mol单质碳完全燃烧放出热量为Y kJ,则1molC与O2反应生成CO的热量变化为
A.放出Y kJ B.放出(5X-5Y) kJ
C.放出(10X-Y) kJ D.吸收(10X-Y) kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】苯环上原有的取代基对新取代导入苯环上的取代基的位置有一定的影响,其规律是(1)苯环上新导入的取代基所占的位置主要决定于原有取代基的性质;(2)可以把原有取代基分成两类:第一类取代基主要使新导入的取代基进入苯环的邻位和对位,如—OH、—CH3(或烃基)、—Cl、—Br、—O—COR等。第二类取代基主要使新导入的取代基进入苯环的间位,如—NO2、—SO3H、—CHO等。请写出下图中②④⑤三步反应的化学方程式。
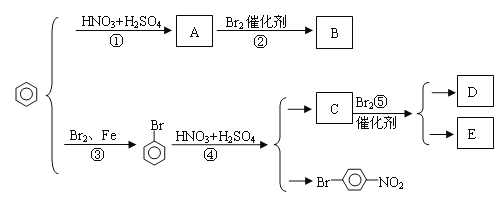
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素X、Y、Z、W的原子序数依次增大,X的原子半径比Y小,X与W同主族,Z是地壳中含量最高的元素。X、Y、Z、W原子最外层电子数之和为13。问:
(1)X是 Y是 Z是 W是 (填元素符号)
(2)写出W的最高价氧化物对应的水化物的电子式 ,写出Y的简单氢化物的电子式 。
(3)Y的最高价氧化物对应的水化物的浓溶液久置后呈现黄色,写出发生反应的化学方程式 。
(4)实验室制取Y的氢化物的方程式 ,该反应 (填“是”或“不是”)氧化还原反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】把3molA和2.5molB混合与2L密闭容器中,发生反应:3A(g)+B(g)![]() xC(g)+2D(g),5min后达平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min)。求:
xC(g)+2D(g),5min后达平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min)。求:
(1)x= 。
(2)平衡时C的浓度为多少?(要求写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
(1)C在元素周期表中的位置为_____________,G的原子结构示意图是__________________________。
(2)D与E按原子个数比1:1形成化合物甲,其电子式为_________,所含化学键类型为___________,向甲中滴加足量水时发生反应的化学方程式是____________________________。
(3)E、F、G三种元素形成的简单离子,半径由大到小的顺序是__________。(用离子符号表示)
(4)用BA4、D2和EDA的水溶液组成燃料电池,电极材料为多孔惰性金属电极。在a极通入BA4气体,b极通入D2气体,则a极是该电池的________极,正极的电极反应式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】依曲替酯是一种皮肤病用药,它可以由原料X经过多步反应合成。
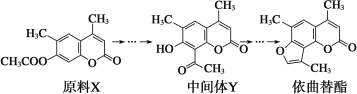
下列说法不正确的是( )
A.原料X与中间体Y互为同分异构体
B.原料X可以使酸性KMnO4溶液褪色
C.中间体Y能发生加成、取代、消去、氧化、还原反应
D.1 mol依曲替酯能与2 mol NaOH发生反应
查看答案和解析>>
科目: 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料。某A1N样品仅含有A12O3杂质,为测定AlN的含量,设计如下三种实验方案。
已知:A1N+NaOH+H2O===NaA1O2+NH3↑
[方案Ⅰ]取一定最的样品,用以下装置测定样品中AlN的纯度(夹持仪器已略去)。

(1)上图C装置中球形干燥管的作用是________________________;
(2)完成以下实验步骤:组装好实验装置,首先________________再加入实验药品,接下来的实验操作是______________,打开分液漏斗活塞,加入浓溶液,至不再产生气体.打开K1,通入氨气一段时间,测定C装置反应前后的质量变化通入氮气的目的是________________________;
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见________________________;
【方案二】
用下图装置测定mg样品中A1N的纯度(部分夹持装置已略去);
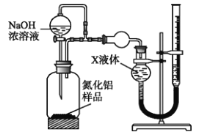
(4)为测定生成气体的体积,量气装置中的X液体可以是_________;
a.CCl4 b.H2O c.NH4Cl溶液 d.![]()
(5)若m g样品完全反应,测得生成气体的体积为V mL(已转换为标准状况),则A1N的质量分数____________________;
【方案三】
按下图步骤测定样品中A1N的纯度:
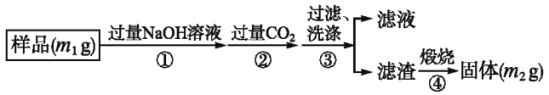
(6)步骤②生成沉淀的离子方程式为________________________;
(7)若在步骤③中未洗涤,测定结果将___________(填“偏高”“偏低’或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,分别对反应C(S)+CO2(g)![]() 2CO(g)(△H>0)进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著变大的是( )
2CO(g)(△H>0)进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著变大的是( )
A.①②③④ B.①③④ C.①② D.①③
查看答案和解析>>
科目: 来源: 题型:
【题目】为了研究碳酸钙与稀盐酸反应的反应速率,一位同学通过实验测定反应中生成的CO2气体体积随反应时间变化的情况,绘制曲线.请分析讨论以下问题。
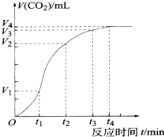
(1)碳酸钙与稀盐酸的反应是放热反应,这是由于反应物的总能量 (填“大于”或“小于”)生成物的总能量。
(2)在0~t1、t1~t2、t2~t3、t3~t4各相同的时间段里,收集到气体最多的是 时间段。反应速率最大的是 时间段,反应速率最小的是 时间段。
(3)t1~t2时间段里影响反应速率的主要外界因素 、t2~t3时间段里影响反应速率的主要外界因素是 (填“温度”或“浓度”或“压强”或“催化剂”)(提醒:多填不得分)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com