
科目: 来源: 题型:
【题目】氢能的存储是其应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为________,该能层具有的原子轨道数为________。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2![]() 2NH3实现储氢和输氢。下列说法正确的是( )
2NH3实现储氢和输氢。下列说法正确的是( )
A.NH3分子中氮原子的轨道杂化方式为sp2杂化
B.NH4+与PH4+、CH4、BH4-、ClO4-互为等电子体
C.相同压强下,NH3沸点比PH3的沸点高
D.[Cu(NH3)4]2+中,N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】丁二酮肟![]() 是检验Ni2+的灵敏试剂。
是检验Ni2+的灵敏试剂。

(1)Ni2+基态核外电子排布式为 。丁二酮肟分子中C原子轨道杂化类型为 ,1mol丁二酮肟分子所含![]() 键的数目为 。
键的数目为 。
(2)Ni能与CO形成四羰基镍[Ni(CO)4],四羰基镍熔点-19.3℃,沸点42.1℃,易溶于有机溶剂。
①Ni(CO)4固态时属于 晶体(填晶体类型)。
②与CO互为等电子体的阴离子为 (填化学式)。
(3)Ni2+与Mg2+、O2—形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求对下图中两极进行必要的联接并填空:

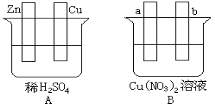
(1)在A图中,使铜片上冒H2气泡。对装置加以联接,则联接后的装置叫 。
电极反应式:锌板: ;铜板: 。
(2)在B图中,a、b两电极均为石墨,对装置加以联接,使a极析出铜,则b析出 。该装置叫 。电极反应式,a极: b极: 。经过一段时间后,停止反应并搅匀溶液,溶液的pH值 (升高、降低、不变),加入一定量的 (填化学式)后,溶液能恢复至与电解前完全一致。
查看答案和解析>>
科目: 来源: 题型:
【题目】右图是一个化学过程的示意图。已知甲池的总反应式为:
2CH3OH+3O2+4KOH=2K2CO3+6H2O
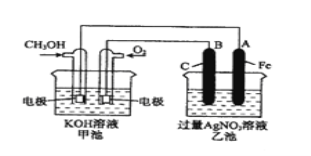
(1)请回答图中甲、乙两池的名称。甲电池是 装置,乙池是 装置。
(2)请回答下列电极的名称:通入CH3OH的电极名称是 ,B(石墨)电极的名称是 。
(3)写出电极反应式:
通入O2的电极的电极反应式是 。
A(Fe)电极的电极反应式为 。
(4)乙池中反应的化学方程式为 。
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标况)
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n,常用作还原剂。已知最简单的氢铝化合物的化学式为Al2H6,它的熔点为150℃且熔融状态不能导电,燃烧时放出大量的热量。Al2H6的球棍模型如图所示。下列说法错误的是
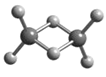
A. Al2H6中Al为-3价,H为+1价
B. Al2H6中含有离子键和极性共价键
C. Al2H6在固态时所形成的晶体是分子晶体
D. Al2H6在空气中完全燃烧,产物为氧化铝和水
查看答案和解析>>
科目: 来源: 题型:
【题目】右下图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。

请回答下列问题:
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为: 。
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置 (填“能”或“不能”)形成原电池,若不能,请说明理由;若能,请指出正、负极材料: 。当反应中收集到标准状况下224mL气体时,消耗的电极质量为 g。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的化学能直接转化为电能。
现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入 极(填a或b,下同),电子从 极流出,电解质溶液中OH-向 极移动。
(4)等质量的下列物质分别完全燃烧,放出热量较多的是 (填编号)
A.固体硫, B.硫蒸气.
查看答案和解析>>
科目: 来源: 题型:
【题目】以NaCl等为原料制备KClO4的过程如下:
①在无隔膜、微酸性条件下,发生反应:NaCl+H2O![]() NaClO3+H2↑(未配平)
NaClO3+H2↑(未配平)
②在NaClO3溶液中加入KCl发生复分解反应,降温结晶,得KClO3。
③一定条件下反应:4KClO3![]() 3KClO4+KCl,将产物分离得到KClO4。
3KClO4+KCl,将产物分离得到KClO4。
(1)电解时,产生质量为2.13g NaClO3,同时得到H2的体积为 L(标准状况)。
(2)向NaClO3溶液中加入KCl能得到KClO3的原因是 。
(3)该过程制得的KClO4样品中含少量KCl杂质,为测定产品纯度进行如下实验:
准确称取5.689g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使ClO4-全部转化为Cl-(反应为:3 KClO4+C6H12O6 ═ 6 H2O + 6 CO2↑+ 3 KCl),加入少量K2CrO4溶液作指示剂,用0.20mol/L AgNO3溶液进行滴定至终点,消耗AgNO3溶液体积21.00mL。滴定达到终点时,产生砖红色Ag2CrO4沉淀。
① 已知: Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.1×10-12,若c(CrO42-)=1.1×10-4mol/L,则此时c(Cl-)= mol/L。
② 计算KClO4样品的纯度(请写出计算过程。)
查看答案和解析>>
科目: 来源: 题型:
【题目】有一种蓝色的晶体,它的结构特征是Fe2+和Fe3+分别占据立方体互不相邻的顶点,立方体的每个棱上均有一个CN-。
(1)根据晶体结构的特点,推出这种蓝色晶体的化学式(用简单整数表示)_____________。
(2)此化学式带何种电荷________,如用Rn+或Rn-与其结合成电中性粒子,此粒子的化学式为__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】【化学一选修5:有机化学基础】
化合物A(C8H8O3)是由冬青树的叶经蒸汽蒸馏而得,因此又名冬青油。它常用作饮料、化妆品的香料,也用作制取止痛药、杀虫剂等。从A出发有如下图所示转化关系(部分反应产物已略去):

已知以下信息:
①F是苯酚;
②A的核磁共振氢谱表明其有六种不同化学环境的氢,且1mol A与溴水反应最多消耗2mol Br2.
③羧酸盐与碱石灰共热可发生脱羧反应,如实验室制甲烷:CH3COONa+NaOH![]() CH4↑+Na2CO3
CH4↑+Na2CO3
回答下列问题:
(1)A的结构简式为________________________;
(2)B→D的反应方程式为_____________________;
(3)F→H的反应类型为_____________________;H的名称为___________________;
(4)C→E的反应方程式为________________________;
(5)A的同分异构体中苯环上只有两个取代基且能发生银镜反应和显色反应的共_________种,其中核磁共振氢谱有八种不同化学环境的氢的是__________________(写结构简式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F、G七种短周期元素,其原子序数依次增大。A的原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是内层电子数的3倍;D与G处在同一族;F是地壳中含量最高的金属元素。请回答下列问题:
(1)元素F在周期表中的位置 。
(2)B、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
(3)配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于 (填晶体类型)。
(4)CA3分子的电子式为 。
(5)ED是优良的耐高温材料,其晶体结构与NaCl晶体相似。ED的熔点比NaCl高,其原因是 。
(6)由A、D、G中任两种元素构成甲、乙两种均含18个电子的分子,所含原子的数目依次为3、4。则甲分子的中心原子采取 杂化;1 mol乙分子含有 molσ键。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com