
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,请回答有关问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ | ⑩ |
(1)表中最活泼的金属是__________,单质能用作半导体材料的是__________,化学性质最稳定的是__________ (填写元素符号)。
(2)表中能形成两性氢氧化物的元素是_________ (填写元素符号),分别写出该元素的氢氧化物与⑥和⑨最高价氧化物的水化物反应的化学方程式:_________________________。
(3)③与⑩组成的化合物属于__________(填“离子化合物”或“共价化合物”)用电子式表示该化合物的形成过程________________________________。①的氢化物中含有__________(填“离子键”或“极性共价键”或“非极性共价键”)的电子式是__________。
(4)⑦和⑩的氢化物中沸点较高的是__________(写化学式)原因是_________。
(5)请设计一个实验,比较⑦⑩单质氧化性的强弱:________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸盐在能源、环保等方面有着广泛的用途。
I.高铁酸钾( K2Fe04)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图1是高铁电池的模拟实验装置:
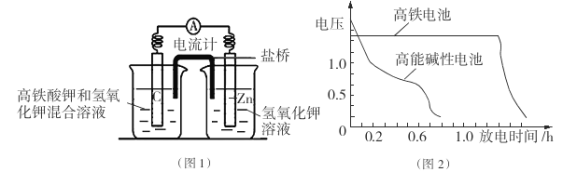
(1)该电池放电时正极的电极反应式为 ;若维持电流强度为1A,电池工作10 min ,理论消耗Zn g(已知F=96500 C/mol)。
(2)盐桥中盛有饱和KC1溶液,此盐桥中氯离子向 移动(填“左”或“右”);若用阳离子交换膜代替盐桥,则钾离子向 移动(填“左”或“右”)。
(3)图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有 。
Ⅱ.工业上湿法制备K2Fe04的工艺流程如图3。
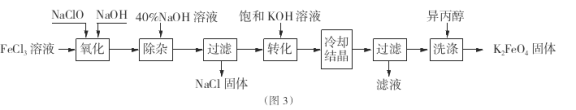
(4)完成“氧化”过程中反应的化学方程式:
![]()
其中氧化剂是 (填化学式)。
(5)加入饱和KOH溶液的目的是
(6)已知25℃时Ksp[Fe(OH)3]=4.0×![]() ,此温度下若在实验室中配制5mol/L
,此温度下若在实验室中配制5mol/L
l00mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入 mL 2 mol/L的盐酸(忽略加入盐酸体积)。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素P、Q、X、Y、Z原子序数逐渐增大。它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1) Z的价电子排布式为____________,QZ3分子的空间构型为____________;
(2) X与Z构成的分子是_________分子(填“极性”或“非极性”)
(3) P和Y形成的化合物,其分子中包含__________键(填个数及 “σ键和π键”),该分子中P原子的杂化方式为____________,
(4) 写出一个验证Y与Z的非金属性强弱的离子反应方程式_________________;
(5) 金属镁在Q的单质中燃烧得到的产物与水反应生成两种碱性物质,该反应的化学方程式是____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。

(1)装置A中盛放亚硫酸钠的仪器名称是_____,其中发生反应的化学方程式为_____。
(2)实验过程中,装置B、C中发生的现象分别是____________、______________,这些现象分别说明SO2具有的性质是____和__;装置B中发生反应的离子方程式为__________。
(3)设计装置D的目的是____________________________________________________。
(4)尾气应用____________________溶液吸收(填试剂的化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1) 如图所示为二维平面晶体示意图,所表示的化学式为AX3的是________。

(2) 下图为一个金属铜的晶胞,请完成以下各题。

① 该晶胞“实际”拥有的铜原子数是________个。
② 该晶胞称为________(填序号)。
A.六方晶胞 B.体心立方晶胞
C.面心立方晶胞 D.简单立方晶胞
③此晶胞立方体的边长为a cm,Cu的相对原子质量为64 g·mol-1,金属铜的密度为ρ g·cm-3,则阿伏加德罗常数为________(用a、ρ表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下。请回答下列问题:
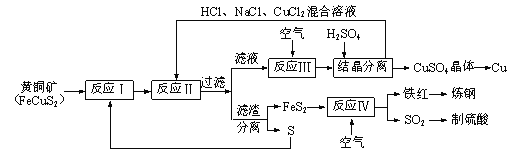
(1)反应Ⅲ的离子方程式为4CuCl2-+O2+4H+=4Cu2++8Cl-+2H2O,CuCl2-中铜元素的化合价为______,该反应中的氧化剂是___________。
(2)一定温度下,在反应Ⅲ所得的溶液中加入硫酸,可以析出硫酸铜晶体而不析出氯化铜晶体,其原因可能是____________________________________________________。
(3)炼钢时,可将铁红投入熔融的生铁中,以降低生铁的含碳量,该过程中主要反应的化学方程式是______________________________________________________________。
(4)SO2尾气直接排放到大气中造成环境污染的后果是_____________________________。
(5)已知反应Ⅱ的离子方程式为Cu2++CuS+4Cl—=2CuCl2-+S,反应Ⅰ的产物为_____________和_____________。(填化学式)
查看答案和解析>>
科目: 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
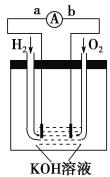
(1)氢氧燃料电池的能量转化的主要形式是由_____________,
在导线中电子流动方向为__________(用a、b表示)。
(2)负极反应式为____________________________。
(3)电极表面镀铂粉的原因是___________________________。
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断
提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种
重要的储氢材料,吸氢和放氢原理如下:
Ⅰ 2Li+H2![]() 2LiH Ⅱ LiH+H2O===LiOH+H2↑
2LiH Ⅱ LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是__________,反应Ⅱ中的氧化剂是________。(均填化学式)
②已知LiH固体密度为0.82 g/cm3,用锂吸收224 L(标准状况)H2,则被吸收的H2体积与生成的LiH体积比为______________。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学课上,围绕硫的化合物性质进行如下探究,请根据要求回答以下问题。

(1)装置A中反应的化学方程式为________________________________。
(2)装置B用来探究SO2的漂白性,则应装的试剂是________,反应一段时间后,看到的现象是________________;若将Cl2通入B中也能看到同样的现象,则二者在反应原理上________(填“相同”或“不相同”)。
(3)装置C检验SO2具有______性(填“氧化”或“还原”)。装置C试管口棉花团应蘸有_____溶液。
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
张亭栋研究小组受民间中医启发,发现As2O3(俗称砒霜)对白血病有明显的治疗作用.氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中有许多重要用途.回答下列问题:
(1)As原子的核外电子排布式为 。
(2)P和S是同一周期的两种元素,P的第一电离能比S大,原因是 。
(3)NH4+中H﹣N﹣H的键角比NH3中H﹣N﹣H的键角 (填“大”或“小”),原因是 。
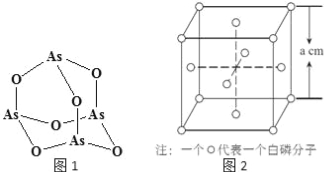
(4)Na3AsO4中含有的化学键类型包括 ;AsO43﹣的空间构型为 ,As4O6的分子结构如图1所示,则在该化合物中As的杂化方式是 。
(5)化合物NH5中的所有原子最外层都满足稳定结构,则NH5是 晶体.
(6)白磷(P4)的晶体属于分子晶体,其晶胞结构如图2(小圆圈表示白磷分子).己知晶胞的边长为a cm,阿伏加德罗常数为NA mol﹣l,则该晶胞中含有的P原子的个数为 ,该晶体的密度为 gcm﹣3(用含NA、a的式子表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。

请回答下列问题:
(1)装置F中发生反应的离子方程式为_______________________________。
(2)装置A的烧瓶中可装试剂_______________________________________________。
(3)B装置的名称是_______________________,E装置的作用______________________________。
(4)通入C装置的两根导管左边较长、右边较短,目的是_________________________。
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。写出反应的化学方程式: _,该反应中氧化剂和还原剂的物质的量之比为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com