
科目: 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如右图所示。下列说法正确的是

A.铁是阳极,电极反应为Fe-2e-+2OH-![]() Fe(OH)2
Fe(OH)2
B.电解一段时间后,镍电极附近溶液的pH减小
C.若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO42-
D.每制得1mol Na2FeO4,理论上可以产生67.2L气体
查看答案和解析>>
科目: 来源: 题型:
【题目】有资料认为NO、NO2不能与Na2O2反应。某小组学生提出质疑,从理论上分析Na2O2和NO2都有氧化性,根据化合价升降原则提出假设并进行探究:
假设Ⅰ.Na2O2能氧化NO2
假设Ⅱ.NO2能氧化Na2O2
(1)小组甲同学设计了如图实验装置,并进行如下实验:
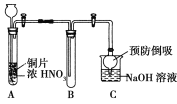
①试管A中发生反应的化学方程式是______________________________。
②待试管B中收集满气体,向试管B中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带余烬的木条迅速伸进试管内,看见木条复燃。甲同学认为假设Ⅱ正确;乙同学认为该装置不能达到实验目的,为达到实验目的,在A、B之间增加一个装置,该装置的作用是______________________________。
③乙同学用改进后装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;但带余烬的木条未复燃。得出结论:假设Ⅰ正确。NO2和Na2O2反应的化学方程式是
_____________________________________________________________________。
(2)丙同学认为NO易被O2氧化,更易被Na2O2氧化。
查阅资料:①2NO+Na2O2===2NaNO2
②6NaNO2+3H2SO4===3Na2SO4+2HNO3+4NO↑+2H2O
③酸性条件下,NO或NO都能与MnO反应生成NO和Mn2+
丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。
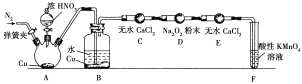
①A装置中盛装Cu片的仪器名称是__________,B中观察到的主要现象是______________________,F装置的作用是______________________________。
②在反应前,打开弹簧夹,通入一段时间N2,目的是______________________________。
③充分反应后,检验D装置中产物是NaNO2还是NaNO3的实验方法是____________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀H2SO4、NaOH溶液等试剂)
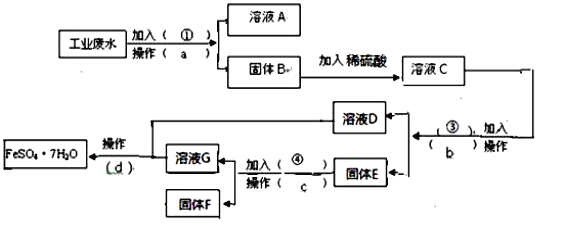
(1)操作a的名称为 ,所需要的玻璃仪器除烧杯外还需要 。
(2)固体E的成分为 ,加入的试剂④为 ,发生的化学方程式为 。
(3)加入试剂①的目的是 。
(4)从溶液D和溶液G中得到FeSO4.7H2O晶体的操作为 、 、 、洗涤、干燥。
(5)若废水中硫酸亚铁、硫酸铜和硫酸钠组成的混合溶液,其中c(Cu2+)=0.1 mol/L,c(Fe2+)=0.4 mol/L,
c(SO42-)= 0.6 mol/L,已知氢离子浓度忽略不计,则c(Na+)为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于同分异构体的说法正确的是( )
A.乙烷的二氯代物和甲烷的二氯代物数目相同
B.丙烷的一氯代物有3种
C.苯的四氯代物有3种
D.C5H12的同分异构体有4种
查看答案和解析>>
科目: 来源: 题型:
【题目】不能说明氧的非金属性比硫强的事实是( )
A. H2O的热稳定性强于H2S
B. 硫化氢水溶液露置于空气中变浑浊
C. H2O是液体,H2S常温下是气体
D. 氧气和氢气化合比硫和氢气化合容易
查看答案和解析>>
科目: 来源: 题型:
【题目】“保护环境,就是保护自己.”目前,我国城市环境中主要的大气污染物是
A.SO2、NO、CO、烟尘 B.CO2、Cl2、N2、雾
C.HCl、NO2、N2、粉尘 D.CO2、NO、NH3、H2S
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)无机化合物可根据其组成和性质进行分类。以下是一组对“一些物质与水反应”的分类图,请按要求填空:

①上述分类中,分成A、B两组的依据是 ;
②C组物质与水反应的离子方程式为 ;
③D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶1的物质有 (填化学式)。
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2
已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中,发生还原反应的过程是 → 。
②写出该反应的化学方程式,并标出电子转移的方向和数目____________。
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 。
④H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN)。H2O2被称为绿色氧化剂的理由是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学平衡原理在工农业生产中发挥着重要的指导作用。
(1) 反应C(s)+CO2(g)![]() 2CO(g)平衡常数K的表达式为 ;
2CO(g)平衡常数K的表达式为 ;
已知C(s) + H2O(g) ![]() CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)
CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g) ![]() CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为 。
CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为 。
(2)已知某温度下,反应2SO2+O2![]() 2SO3,的平衡常数K=19 mol·L-1。在该温度下的体积固定的密闭容器中充入c(SO2)=1mol·L-1,c(O2)=1 mol·L-1,当反应在该温度下SO2转化率为80%时,该反应是否达到化学平衡状态?计算过程和结论如下 :
2SO3,的平衡常数K=19 mol·L-1。在该温度下的体积固定的密闭容器中充入c(SO2)=1mol·L-1,c(O2)=1 mol·L-1,当反应在该温度下SO2转化率为80%时,该反应是否达到化学平衡状态?计算过程和结论如下 :
(3)若未达到,反应向 (填“正反应”或“逆反应”) 方向进行。
查看答案和解析>>
科目: 来源: 题型:
【题目】雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学收集了该地区的雾霾,经必要的预处理后试样溶液,设计并完成了如下的实验:

已知:3NO3-+ 8Al + 5OH- + 2H2O![]() 3NH3 + 8AlO2-
3NH3 + 8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是
A.试样中肯定存在NH4+、Mg2+、SO42-和NO3-
B.试样中一定不含Al3+
C.试样中可能存在Na+、Cl-
D.该雾霾中可能存在NaNO3、NH4Cl和MgSO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com