
科目: 来源: 题型:
【题目】将A气体通入BaCl2溶液,未见沉淀生成,然后通入B气体,有沉淀生成,再加入过量的稀盐酸后沉淀消失,则A、B气体可能是
A.SO2、H2S B.SO2、NO2 C. CO2 、NH3 D.SO2、Cl2
查看答案和解析>>
科目: 来源: 题型:
【题目】(化学与技术)用三氧化二铬制取重铬酸钾的工艺流程如下:

回答下列问题:
(1)熔炉中NaOH作熔剂,也可直接发生反应,其中Na2CO3、Cr2O3及富氧空气生成Na2 CrO4及CO2的化学方程式为________________。
(2)“熔体”浸取时,为提高Na2CrO4的浸取率,可采取的措施是___________(任写两条)。
(3)实验中两次用到“固液分离”,工业上常用的固液分离设备有(填字母)。
A.分馏塔 B.离心机 C.反应釜 D.框式压滤机
(4)“酸化”时发生反应的离子方程式为________。
(5)“转化”步骤中,为了提高K2Cr2O7的产率,参照如图所示溶解度曲线,可采取的措施是______________
(任写两条)。

(6)重铬酸钾容量法是测定土壤中有机物的常用方法,原理为:
2K2Cr2O7+8H2SO4+3C=2K2SO4+2Cr2(SO4)3+3CO2↑+8H2O
K2Cr2O7+6FeSO4+7H2SO4=K2SO4+ Cr2(SO4)3+3Fe2(SO4)3+7H2O
土壤有机物的平均含碳量为58%,该方法对土壤有机物的氧化约为90%,称取mg经预处理后的土样,用滴定管准确加入VlmLc1mol/L K2Cr2O7溶液、5 mL(过量)稀硫酸,预先加热至180—190 ℃ ,煮沸5分钟,稍冷后将试管内容物用蒸馏水洗入锥形瓶中,加入2~3滴邻菲罗琳指示剂,用c2mol /L的FeSO4溶液滴定至终点,消耗FeSO4溶液V2mL 。则该土壤样品中有机物的质量分数为________(列出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列有机物所表示的物质的分子式。
(1)![]() ___________________;
___________________;
(2)![]() ___________________;
___________________;
(3)![]() ___________ ;
___________ ;
(4)![]() __________________
__________________
查看答案和解析>>
科目: 来源: 题型:
【题目】 两份铝屑,第一份与过量的盐酸反应,第二份与过量的NaOH溶液反应,产生氢气的体积比为1:2,则第一份与第二份铝屑的质量比为
A. 1:1 B. 1:2 C. 1:3 D. 1:4
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:乙烯可被酸性高锰酸钾溶液氧化为CO2。可以用来除去甲烷中混有的少量乙烯的操作方法是( )
A. 将混合气体通过盛有硫酸的洗气瓶
B. 将混合气体通过盛有足量溴水的洗气瓶
C. 将混合气体通过盛有水的洗气瓶
D. 将混合气体通过盛有酸性高锰酸钾的洗气瓶
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为_______________________。
(2)称取两种固体各2 g,分别加入两个小烧杯中,再各加10 mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复到室温,向所得溶液中各滴入2滴酚酞溶液。
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论:____________________。
②同学们在两烧杯中还观察到以下现象。其中盛放Na2CO3的烧杯中出现的现象是________(填字母序号)。
a.溶液温度下降 b.溶液温度升高
c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。
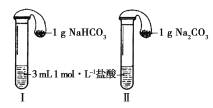
①两试管中均产生气体,________(填“Ⅰ”或“Ⅱ”)的反应程度更为剧烈。
②反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是________(填字母序号)。
a.装置Ⅰ的气球体积较大
b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算
d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成0.5 mol·L-1的溶液,设计如下方案并对反应现象做出预测:
实验方案 | 预测现象 | 预测依据 |
操作1:向2 mL Na2CO3溶液中滴加1 mL 0.5 mol·L-1 CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应:________(写离子方程式) |
操作2:向2 mL NaHCO3溶液中滴加1 mL 0.5 mol·L-1 CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应 |
实施实验后,发现操作2的现象与预测有差异:产生白色沉淀和气体,则该条件下,NaHCO3溶液与CaCl2溶液反应的离子方程式为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列材料的特性及用途说法错误的是(
A.高纯硅用于制造光导纤维,实现光电信号转化
B.石英中无色透明的晶体就是通常所说的水晶,其主要成分是二氧化硅
C.光导纤维导光的能力很强,是非常好的通讯材料
D.硅胶多孔,吸附水能力强,可以用作催化剂的载体
查看答案和解析>>
科目: 来源: 题型:
【题目】在国际环境问题中,一次性使用的聚苯乙烯材料带来的“白色污染”甚为突出。这种材 料难以分解,处理麻烦。最近研究制出一种新型的材料能替代聚苯乙烯。它是由乳酸缩 聚而生成的,该种材料可在乳酸菌作用下发生降解,下列关于聚乳酸的说法正确的是
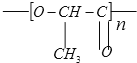
A.聚乳酸是一种纯净物
B.其聚合方式与聚苯乙烯相似
C.其单体为CH3-CH(OH)-COOH
D.聚乳酸是一种线型高分子材料
查看答案和解析>>
科目: 来源: 题型:
【题目】在特制漏斗中将铝热剂混合均匀后,引发铝热反应的操作是:____________。
(2)硅与铝同周期.地壳里硅铝的含量硅____________铝(填>,<或=)。工业上制备金属铝的化学方程式是: ____________,工业上制备硅的化学方程式有:
a.SiO2+2C![]() Si(粗)+2CO
Si(粗)+2CO
b.SiO2+3C![]() SiC +2CO(副反应),
SiC +2CO(副反应),
c.Si(粗)+ 2C12![]() SiCl4
SiCl4
d.SiC14 + 2H2![]() Si+4HC1,
Si+4HC1,
某同学将氧化还原反应、非氧化还原反应及四大基本反应绘制成上图,其中属于上图“2"区域的反应是____________ (填序号)。

(3)SiO2是硅酸盐玻璃(Na2CaSi6O14)主要成分,Na2CaSi6O14也可写成Na2OCaO6SiO2,钠长石(NaAlSi3O8)的氧化物形式____________,长石是铝硅酸盐,不同类长石其氧原子的物质的量分数相同.由此可推知钙长石的化学式为____________。
(4)某铝合金由Al、Si、Cu、Mg组成。①称取100g该铝合金样品,分成等质量的A、B两份。向A 份加入足量NaOH溶液,B份加入足量的稀盐酸。②待两份反应物都充分反应之后,称得滤渣质量相差1.60g,收集得到的两份气体的体积相差2240mL(标准状况下)。则样品中Si和Mg的物质的量分别是n(Si)____________和n(Mg)____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中,错误的是(
A.浓硫酸常见的特性是吸水性、脱水性、氧化性
B.浓硫酸也具有酸性,在常温下能够与活泼金属铁、铝等反应放出氢气
C.氟化氢的热稳定性很好,具有极弱的还原性,为一元弱酸
D.SO2、SO3都是酸性氧化物,具有酸性氧化物的通性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com