
科目: 来源: 题型:
【题目】依据一定的标准采取不同的分类方法是人们认识事物常用的方法。下列有关物质类别的判别标准中正确的是( )
A.酸:能否与金属反应放出氢气
B.电解质:水溶液是否导电
C.离子化合物:是否含有离子键
D.酸性氧化物:能否与碱反应
查看答案和解析>>
科目: 来源: 题型:
【题目】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3 H2(g)![]() CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CO2(g)+ H2(g)![]() CO(g)+H2O(g)ΔH2 II
CO(g)+H2O(g)ΔH2 II
某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:

【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)![]() H2O(g) ΔH3=44.0kJ·mol-1
H2O(g) ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K= ;反应II的ΔH2= kJ·mol-1。
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有 。
A.使用催化剂Cat.1
B.使用催化剂Cat.2
C.降低反应温度
D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是 。
(4)在右图中分别画出I在无催化剂、有Cat.1和由Cat.2三种情况下“反应过程-能量”示意图。

(5)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在___ 极,该电极反应式是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为 。
(2)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的 倍;
②达平衡时,容器内混合气体的平均分子量比起始投料时_____ (填 “增大”“减小”或“相等”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】海带中含丰富的碘元素,从海带中分离出碘可按如下步骤进行:
①滴加稀硫酸酸化后,加入适量H2O2(质量分数为3%);
②将海带焙烧成灰后加水搅拌 ;
③加CCl4振荡 ;
④用分液漏斗分液;
⑤煮沸、过滤。
合理的操作顺序是( )
A.①②③④⑤ B.②⑤①③④ C.①③⑤②④ D.②①③⑤④
查看答案和解析>>
科目: 来源: 题型:
【题目】铜有很多重要的化合物。特别是Cu2+核外电子的特殊构型,其能与很多含有氧或氮元素的配体[如NH3、乙二胺(H2N—CH2—CH2—NH2)、乙酰丙酮(CH3COCH2COCH3)等]形成配合物。
(1)C、N、O元素的电负性由小到大的顺序是 。
(2)[Cu(NH3)4]2+呈深蓝色,该粒子中配位体的空间构型为 。
(3)酞菁铜也是Cu2+的一种配合物,被广泛用于墨水生产,其结构如图。请用箭头标出其中的配位键 ,该分子中氮原子的杂化方式为 。
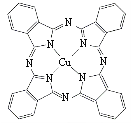
(4)CuCl2在湿空气中潮解,易溶于水、乙醇和丙酮,熔点约100℃。推测氯化铜的晶体类型为 。
(5)Cu的晶胞如图所示,铜原子的配位数为 。

查看答案和解析>>
科目: 来源: 题型:
【题目】某学生研究小组欲探究CuSO4溶液与Na2CO3溶液混合产生的蓝绿色沉淀组成,小组进行下列实验探究。
【提出假设】
假设1:沉淀为Cu(OH)2
假设2:沉淀为
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3mCu(OH)2]
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【物质成分探究】
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤
步骤2:甲同学取一定量固体,用气密性良好的右图装置(夹持仪器未画出)进行定性实验。

请回答下列问题:
(1)假设2中的沉淀为 。
(2)假设1中沉淀为Cu(OH)2的理论依据是 。
(3)无水乙醇洗涤的目的____ __。
(4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设______(填写序号)成立。
(5)乙同学认为只要将上图中B装置的试剂改用 试剂后,便可验证上述所有假设。
(6)乙同学更换B试剂后验证假设3成立的实验现象是 。
(7)在假设3成立的前提下,某同学考虑用Ba(OH)2代替Ca(OH)2,测定蓝绿色固体的化学式,若所取蓝绿色固体质量为27.1g,实验结束后装置B的质量增加2.7g,C中的产生沉淀的质量为19.7g。则该蓝绿色固体的化学式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】以NaCl、CO2、NH3为原料发生反应,制得NaHCO3和NH4Cl是“侯氏制碱法”的重要步骤。相关物质的溶解度曲线如图所示。下列说法不正确的是
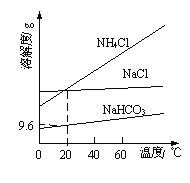
A.将NaHCO3加热分解可得纯碱
B.常温下碳酸氢钠的溶解度大于碳酸钠
C.采用蒸发结晶从溶液中分离出NaHCO3
D.20℃时,NaHCO3饱和溶液的物质的量浓度约为1.1mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】为回收利用废钒催化剂(含有V2O5、VOSO4及SiO2等,其中VOSO4可溶于水),科研人员最新研制了一种回收钒的新工艺,其主要流程如下:

(1)萃取、反萃取过程中所需的主要玻璃仪器为 。
(2)上述流程中涉及到两处氧化还原反应。
①“浸取还原”过程的产物为VOSO4,该反应的离子方程式为 。
②“氧化”过程无气体产生,溶液中VO2+转化为VO2+,该反应的离子方程式为 。
(3)“沉淀”过程中,沉钒率受温度、氯化铵系数(NH4Cl的质量与调节pH之后的料液中VO的质量比)等的影响,其中温度与沉淀率的关系如图所示,温度高于80℃沉钒率降低的可能原因是 。

(4)上述流程中所得沉淀为一系列的聚合物种[其分子组成可用NmHnVxOy表示],质谱法分析某沉淀的摩尔质量为832g/mol。取该沉淀83.2g用下列装置测定其组成,充分焙烧后玻璃管内残留V2O5固体为72.8g;所得气体通过U形管后,U形管增重3.6g。

①广口瓶中浓硫酸的作用为 。
②该沉淀的分子式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是 ( )
A. 利用质谱法
B. 利用红外光谱法
C. 利用核磁共振氢谱
D. 利用金属钠或者金属钾
查看答案和解析>>
科目: 来源: 题型:
【题目】在元素周期表的金属元素和非金属元素交界处,最容易找到的材料是( )
A. 制半导体的材料
B. 耐高温、耐腐蚀的合金材料
C. 制农药的材料
D. 制催化剂的材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com