
科目: 来源: 题型:
【题目】下列关于不锈钢和普通钢的叙述中正确的是( )
A. 组成元素相同
B. 耐腐蚀性能不同
C. 都属于钢,因此物理性质相同
D. 构成的主要元素都是铁,因此化学性质完全相同
查看答案和解析>>
科目: 来源: 题型:
【题目】I.下表为周期表的一部分,其中的编号代表对应的元素。

(1)写出上表中元素I的价层电子排布图 。元素C、D、E、F的第一电离能由大到小的顺序是 (用元素符号表示)。
(2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙。下列有关叙述不正确的有( )
A.甲、乙和丙分子的空间构型分别为正四面体形、三角锥形、V形
B.甲、乙和丙分子中,中心原子均采取sp3的杂化方式
C.三种分子中键角由大到小的顺序是丙>乙>甲
D.甲、乙和丙分子均为由极性键构成的极性分子
(3)由元素J、C、E组成一种化学式为J(CE)的配位化合物,该物质常温下呈液态,熔点为一20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断:该化合物的晶体中存在的作用力有( )
A.离子键
B.极性键
C.非极性键
D.范德华力
E.氢键
F.配位键
Ⅱ.(1) BCl3中B原子的杂化方式为 。第一电离能介于B、N之间的第二周期元素有 种。写出与BCl3结构相同的一种等电子体 (写离子)。
(2)科学家测得胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下:
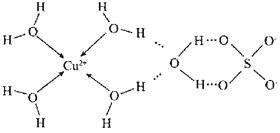
①胆矾的化学式用配合物的形式表示为的 ;
②胆矾中SO42-的空间构型为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】不粘锅的内壁有一薄层为聚四氟乙烯的涂层,用不粘锅烹烧饭菜时,不易粘锅烧焦。干、洗店常用有机溶剂洗衣服,目前使用的标准干洗剂的主要成份是四氯乙烯。关于聚四氟乙烯和的叙述,正确的是
A.它们都属于混合物
B.它们都是乙烯的同系物
C.它们的分子都不含氢原子
D. 聚四氟乙烯分子中含有双键
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A为缓释阿司匹林的主要成分。用于内燃机润滑油的有机物Y 和用于制备水凝胶的聚合物P 的合成路线如下。
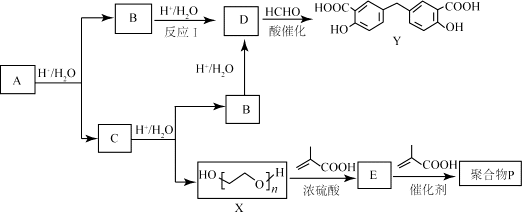
已知: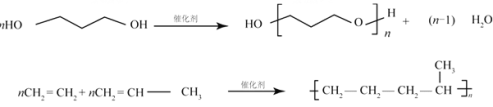
(1)D 的分子式为C7H6O3,D 中所含的官能团是 。
(2)D→Y的化学方程式是 。
(3)反应Ⅰ的另一种产物是M,其相对分子质量是60,B 、M 均能与NaHCO3反应产生CO2。
①M 是 。
②B→D的化学方程式是 。
(4)下列说法正确的是 。
a.B、C、D中均含有酯基
b.乙二醇可通过![]() 的路线合成
的路线合成
c.C能与饱和溴水反应产生白色沉淀
(5)红外光谱测定结果显示,E 中不含羟基。
①X→E的反应类型是 。
② E的结构简式是 。
(6)若X的聚合度n=1,有机物A 只存在一种官能团,A 的结构简式是 。
(7)聚合物P的结构简式是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如下图所示的装置制取乙酸乙酯,请回答下列问题。

(1)乙醇分子官能团名称是_______________。
(2)试管a中加入几块碎瓷片的目的是___________。
(3)试管a中发生反应的化学方程式为 ___________,反应类型是_______。
(4)可用_________的方法把制得的乙酸乙酯分离出来。
查看答案和解析>>
科目: 来源: 题型:
【题目】硅孔雀石是一种含铜矿石,含铜形态为CuCO3·Cu(OH)2和CuSiO3·2H2O,同时含有SiO2、FeCO3、Fe2O3、Al2O3等杂质。以其为原料制取硫酸铜的工艺流程如图:
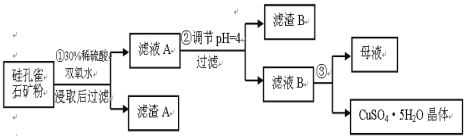
(1) 完成步骤①中稀硫酸与CuSiO3·2H2O反应的化学方程式:
CuSiO3·2H2O+H2SO4=CuSO4 +_______+H2O;双氧水的作用是____ 。
(2) 步骤②调节溶液pH,可以选用的试剂是______
A. CuO B.Fe2O3 C.Al2O3 D Cu(OH)2
(3) 有关氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
步骤②中,调节pH=4时,所得滤渣B的成分的化学式为 、 。
(4) 将滤液B通过 、 ,过滤等操作可得到硫酸铜晶体。
(5) 测定硫酸铜晶体结晶水的含量时,应将其放入______中灼烧。加热失水后,若在空气中冷却称量,测定结果__ ___(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)反应3A(g)+B(g) ===2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1 mol/(L·min)、②vC=0.5 mol/(L·min)、③vB=0.5 mol/(L·min),三种情况下该反应速率由大到小的关系是 。(用序号表示)
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应的化学方程式为__________________________。
②反应开始至2min,以气体Z表示的平均反应速率为 。
③2min反应达平衡容器内混合气体的平均相对分子质量比起始时 (填“大”,“小”或“相等”,下同),混合气体密度比起始时 。
④上述反应,在第2min时,X的转化率为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】将0.195g锌粉加入到20.0mL的0.100molL﹣1MO2+溶液中,恰好完全反应,则还原产物可能是( )
A. M B. M2+ C. M3+ D. MO2+
查看答案和解析>>
科目: 来源: 题型:
【题目】锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)锡在周期表中的位置为_____________.
(2)用于镀锡工业的硫酸亚锡(SnSO4)的制备步骤如下:
I.SnCl2加入盐酸和Sn 粉
II.分离滤渣和滤液
Ⅲ.滤液用NaHCO3调节pH至6~7 得混合物(含SnO)
Ⅳ.从混合物中分离得SnO
V.SnO和稀硫酸最终得SnSO4晶体
①步骤Ⅰ加入Sn粉的作用: _________________及调节溶液pH。
②步骤Ⅱ用到的玻璃仪器有烧杯、_______________、______________。
③步骤Ⅲ生成SnO的离子方程式:_________________________。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是_____________________,证明已洗净。
⑤步骤Ⅴ操作依次为 _____________、____________、过滤、洗涤、低温干燥。
(3)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为__________________。
实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是__________。

(4)利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是_________________。
(5)用于微电子器件生产的锡粉纯度测定:
①取2.38g试样溶于较浓硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
②加入过量的Fe2(SO4)3;
③用0.1000mol/LK2Cr2O7溶液滴定,消耗20.00mL。步骤②中加入Fe2(SO4)3的作用是:__________;此锡粉样品中锡的质量分数:____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.工业上可用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡 常数 | 温度/℃[ | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) | K3 | ||
(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=________(用K1、K2表示)。500 ℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时v正________v逆(填“>”、“=”或“<”)。
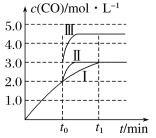
(2)在3 L容积可变的密闭容器中发生反应②,已知c(CO)—反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是_______________。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是______________。
Ⅱ.利用CO和H2可以合成甲醇,反应原理为CO(g)+2H2(g) ![]() CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。
CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。 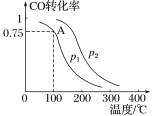
(1)p1________p2(填“>”、“<”或“=”),理由是 。
(2)该甲醇合成反应在A点的平衡常数K= (用a和V表示)。
(3)该反应达到平衡时,反应物转化率的关系是CO________H2。(填“>”、“<”或“=”)
(4)下列措施中能够同时满足增大反应速率和提高CO转化率的是________(填字母)。
A.使用高效催化剂 B.降低反应温度
C.增大体系压强 D.不断将CH3OH从反应混合物中分离出来
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com