
科目: 来源: 题型:
【题目】下列关于原子结构、元素性质的说法正确的是
A. 含有金属元素的化合物中一定含离子键
B. VIIA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
C. 同种元素的原子均有相同的质子数和中子数
D. IA族金属元素是同周期中金属性最强的元素
查看答案和解析>>
科目: 来源: 题型:
【题目】海水资源的利用具有广阔前景。海水中主要离子的含量如下表所示。
成分 | 含量(mg·L-1) | 成分 | 含量(mg·L-1) |
Cl- | 18980 | Ca2+ | 400 |
Na+ | 10560 | HCO3- | 142 |
SO42- | 2560 | Br- | 64 |
Mg2+ | 1272 |
利用海水可以提取溴和镁,提取过程如下。

(1)提取溴的过程中,经过两次Br-→Br2转化的目的是:①__ ___,
吸收塔中发生反应的离子方程式是:②_____________ _______。
用平衡移动原理解释通空气的目的:③___ ____________。
(2)吸收塔中也可采用纯碱吸收Br2,主要反应如下,请配平并表示出电子转移的方向和数目:
□Br2+□Na2CO3+□H2O―→□NaBr+□NaBrO3+□NaHCO3
(3)从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作是①____ ____、过滤、洗涤、干燥。最后一步冶炼得到金属镁的化学方程式为②____ ____;冶炼时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式③____ __________。
(4)依据上述流程,若将10 m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2
的体积为________L(忽略Cl2的溶解)。
查看答案和解析>>
科目: 来源: 题型:
【题目】空气吹出法工艺是目前“海水提溴”的最主要方法之一。其工艺流程如下:
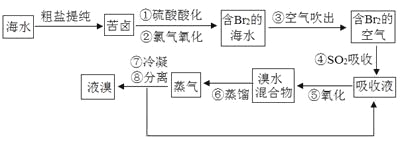
(1)步骤①中氯气氧化溴离子时在pH=3.5的酸性条件下效果最好,当使用精确pH试纸(能读数到0.1)检测步骤②氯气氧化的溶液的pH时,发现其颜色变化失常,则pH检测失败的原因是 。
(2)步骤④中反应的化学方程式为 ,该反应中体现了SO2的 性(填“氧化”或“还原”)。
(3)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,在实验室可用分液漏斗进行分离。分离时从分液漏斗的上口倒出的是 。
(4)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氧化”后再蒸馏,“空气吹出、SO2吸收、氧化”的过程实际上是一个Br2的 过程,与直接蒸馏含Br2的海水相比优点是消耗更少成本降低和
查看答案和解析>>
科目: 来源: 题型:
【题目】磷有三种同素异形体,分别为白磷(P4)、红磷和黑磷。
(1)白磷常温为白色或淡黄色固体,在40℃左右自燃,实验室保存少量白磷的方法是__________;
(2)白磷![]() 黑磷,黑磷比白磷稳定。结构与石墨相似,下列叙述正确的是_______
黑磷,黑磷比白磷稳定。结构与石墨相似,下列叙述正确的是_______
A.黑磷与白磷互为同分异构体 B.黑磷能导电
C.白磷转化为黑磷为氧化还原反应 D.白磷转化为黑磷为放热反应
(3)红磷在氯气中燃烧生成两种氯化物,其中一种氯化物分子是每个原子最外层都满足8个电子的结构,则该氯化物的空间构型与下列_______分子最相似(填字母)
A.H2O B.CCl4 C.NH3 D.CS2
(4)己知白磷、红磷燃烧的热化学方程式分别为
① P4(s,白磷)+5O2(g)=P4O10(s) △H=-2986kJ/mol
② P(s,红磷)+![]() O2(g)=
O2(g)=![]() P4O10(s) △H=-739kJ/mol
P4O10(s) △H=-739kJ/mol
写出红磷转化为白磷的热化学方程式:________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】
(1)写出铁与水蒸气反应的化学方程式______________________________。
(2)已知Cu2S可以和硝酸反应,请配平下列化学反应方程式:
Cu2S+ HNO3 ![]() CuSO4 + Cu(NO3)2+ NO↑+
CuSO4 + Cu(NO3)2+ NO↑+
(3)某校兴趣小组欲测定一种铁铝硅合金(FexAlySiz)粉末的组成,提出如下方案:准确称取1.46g该合金粉末,加入过量盐酸溶液充分反应后过滤,测定剩余固体质量0.07g。向滤液中滴加足量浓NaOH溶液,充分搅拌、过滤、洗涤得固体。再将所得固体充分加热、灼烧得红棕色粉末1.60g,通过计算确定此合金的组成为 (填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】额度图有机物分子中带“*”碳原子是手性碳原子。该有机物分别发生下列反应,生成的有机物分子中不会含有手性碳原子的是
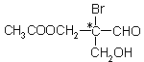
①与甲酸发生酯化反应
②与足量NaOH水溶液反应
③与银氨溶液作用只发生银镜反应
④催化剂作用下与H2反应
A、①②③④ B、①③ C、②④ D、以上反应都不成立
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾。
(1)SO2和O2反应制取SO3的反应原理为:2SO2+O2![]() 2SO3,经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s)
2SO3,经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s)
① 则这段时间为_______s。
② 该反应达到平衡状态的标志是_______。
A.容器内硫元素物质的量分数不变 B.混合物的平均相对分子质量不变
C.n(SO2):n(O2):n(SO3)=2:1:2 D.各组分的体积分数不变
(2)利用烧渣制绿矾的过程如下:
![]()
操作I的名称____________,溶液A的溶质___________,固体B是__________。
(3)某科研机构用NaOH溶液吸收废气中的SO2,将所得的Na2SO4溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示,(电极材料为石墨)

① 图中b极要连接电源的___________极(填“正”或“负” )
②SO32-放电的电极反应式为__________。
③ 若用甲烷-空气燃料电池作电源,处理标准状况下40m3的废气(其中SO2的体积分数为0.2 ) ,理论上需要消耗标准状况下甲烷___________m3。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室可利用乙二醇、铜或铜的化合物制备乙二醛,下图是某兴趣小组设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,试管C中装有水(加热装置未画出)。试回答:
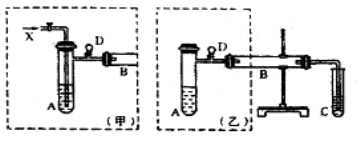
(1)两套装置中的A、B处都需加热,A处用水浴加热,A处用水浴加热的主要优点是 。
(2)若按甲装置进行实验,B管处装铜粉,通入A管的气体为X,B中反应的化学方程式为 。
(3)若按乙装置进行实验,则B管中应装 ,B中反应的化学方程式为 。
(4)实验完成时先打开D处的铁夹,再撤去酒精灯,这样做的目的是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法中正确的是
A.常温常压下,16g CH4中含有的原子总数为5NA
B.78g苯含有碳碳双键的数目为3NA
C.1mol/L NaCl溶液中含有的氯离子数目为NA
D.标准状态下,11.2L CH3COOH中含有的分子数目为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com