
科目: 来源: 题型:
【题目】有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生。
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。
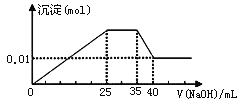
根据上述实验,以下推测不正确的是
A. 原溶液一定不存在H+、Cu2+、CO32-
B. 不能确定原溶液是否含有K+、NO3-
C. 实验所加的NaOH的浓度为2mol·L-1
D. 原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+):n(Al3+):n( NH4+)=1:1:2
查看答案和解析>>
科目: 来源: 题型:
【题目】将0.1mol/L醋酸溶液加水稀释,下列说法正确的是( )
A. 溶液中c(OH-)和c(H+)都减小
B. 溶液的pH增大
C. 醋酸电离平衡向左移动
D. 溶液中c(H+)增大
查看答案和解析>>
科目: 来源: 题型:
【题目】原电池发生的反应是可自发进行的氧化还原反应,CO/O2燃料电池以熔融状态的碳酸盐为电解质,下列说法正确的是 ( )
A、CO在正极通入
B、CO32— 在电池内部向正极移动
C、当有22.4LCO参加反应时电路中有2mol电子发生转移
D、该电池电解质在固态时,电池无法工作
查看答案和解析>>
科目: 来源: 题型:
【题目】磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)已知磷酸(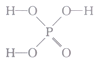 )分子中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2) 却不能与D2O发生氢交换。则H3PO2是(填“一元”“二元”或“三元”)酸,其分子的结构式为________(填字母)。
)分子中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2) 却不能与D2O发生氢交换。则H3PO2是(填“一元”“二元”或“三元”)酸,其分子的结构式为________(填字母)。

(2)H3PO2具有较强的还原性,可以通过电解的方法制备。“四室电渗析法”工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过)。

①阳极的电极反应式为_________。
②II 膜为___________(填“阴离子交换膜”或“阳离子交换膜”)。
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的交换膜,从而合并阳极室与产品室,其缺点是产品中混有______杂质。
查看答案和解析>>
科目: 来源: 题型:
【题目】某媒体以《中国酱油遭遇欧盟高门槛》为题,报道了我国广东某地生产的酱油很可能在欧洲市场被判死刑,从而失去几百万美元的份额一事,其原因是酱油中的氯丙醇严重超标.三氯丙醇(分子中只含一个羟基)的同分异构体有(—OH和—Cl不在同一个C原子上)( )
A. 3种 B. 4种 C. 5种 D. 6种
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ有机物A、B、C、D、E之间发生如下的转化:

(1)写出C物质的结构简式:_________________。
(2)上述②~⑧转化反应中,属于取代反应的有____________;
(3)属于加成反应的有____。(用反应序号填写)
(4)向A的水溶液中加入新制的Cu(OH)2并加热时产生的实验现象是______________。
请写出下列转化的化学反应方程式:
(5)B+D~E:________________________;
(6)乙烯生成聚乙烯:___________________。
Ⅱ己知葡萄糖在乳酸菌的作用下转化为乳酸,乳酸的结构简式为 。
。
试回答:
(7)乳酸分子中含有_____和_______两种官能团(写名称)。
(8)乳酸与金属钠反应的化学方程式为________________。
(9)乳酸与Na2CO3溶液反应的化学方程式为___________________________。
(10)乳酸在浓硫酸作用下,两分子相互发生酯化反应生成环状酯,此环状酯的结构简式为 __________。
查看答案和解析>>
科目: 来源: 题型:
【题目】【2016届唐山二模】目前人们对环境保护、新能源开发很重视。
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体。
4CO(g)+2NO2(g) ![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是 (填代号)。
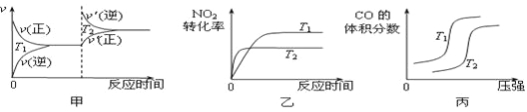
(2)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g) ΔH在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率v(CO2)= ;计算该反应的平衡常数K= 。
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是 (填字母代号)。
A.加入一定量的活性炭 B.通入一定量的NO
C.适当缩小容器的体积 D.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率 (填“升高”或“降低”),ΔH 0(填“>”或“<”).
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH= -l59.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式 。
(4)一种氨燃料电池,使用的电解质溶液是2mol/L的KOH溶液。
电池反应为:4NH3+3O2=2N2+6H2O;
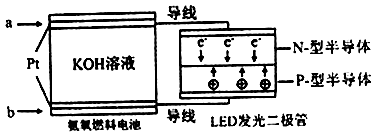
请写出通入a气体一极的电极反应式为 ;每消耗3.4g NH3转移电子的物质的量为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸是一种重要的化工产品,2SO2+O2![]() 2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是( )
2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是( )
A.只要选择适宜的条件,SO2和O2就能全部转化为SO3
B.该反应达到平衡后,反应就完全停止了,即正逆反应速率均为零
C.如果反应前充入由18O原子组成的O2,反应达到平衡状态时, 18O在所有物质中都存在
D.在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com