
科目: 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种绿色高效水处理剂。某学习小组用下图所示装置(夹持仪器已略去)制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备K2FeO4。
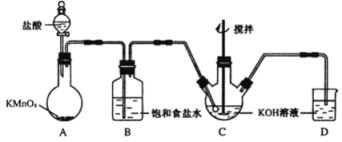
查阅资料知K2FeO4的部分性质如下:①可溶于水、微溶于浓KOH溶液;②在0℃~5℃、强碱性溶液中比较稳定;③在Fe3+和Fe(OH)3催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。请回答下列问题:
(1)装置A中发生反应的化学方程式为 。
(2)仪器C和D中都盛有KOH溶液,其中C中KOH溶液的作用是 。
(3)Cl2与KOH的浓溶液在较高温度下反应生成KClO3。为保证反应生成KClO,需要将反应温度控制在0~5℃下进行,在不改变KOH溶液浓度的前提下,实验中可以采取的措施是 。
(4)在搅拌下,将Fe(NO3)3饱和溶液缓慢滴加到KClO饱和溶液中即可制取K2FeO4,写出该反应的化学方程式 ;该操作不能将KClO饱和溶液滴加到Fe(NO3)3饱和溶液中,其原因是 。
(5)制得的粗产品中含有Fe(OH)3、KCl等杂质。提纯方案:将一定量的K2FeO4粗产品溶于冷的3 mol/LKOH溶液中,用砂芯漏斗(硬质高硼玻璃)过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置,再用砂芯漏斗过滤,晶体用适量乙醇洗涤2~3次后,在真空干燥箱中干燥。
①第一次和第二次过滤得到的固体分别对应的是(填化学式) 、 ,过滤时不用普通漏斗而采用砂芯漏斗的原因是 。
②晶体用乙醇洗涤的原因是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】尿素(H2NCONH2)是一种农业生产中常用的氮肥。在工业上,尿素还用于制造有机铁肥,如[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)]。回答下列问题:
(1)基态Fe3+的核外价电子排布式为 。
(2)C、N、O三种元素的第一电离能由大到小的顺序是 。
(3)在一定条件下,NH3与CO2能合成尿素,1mol尿素分子中,σ键的数目为 ;尿素分子中C原子的杂化方式为 。
(4)NO3-的空间构型为 ;写出NO3-互为等电子体的一种分子的化学式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学反应的离子方程式其中正确的是
A. 碳酸钙与盐酸反应:CO32—+ 2H+= CO2↑ + H2O
B. 氨水与盐酸反应:OH—+ H+= H2O
C. 氢氧化钡溶液与硫酸反应:Ba2++ OH—+ H++ SO42—= BaSO4↓+ H2O
D. 铁与氯化铁溶液反应:Fe + 2Fe3+= 3Fe2+
查看答案和解析>>
科目: 来源: 题型:
【题目】以硅孔雀石[主要成分为 CuCO3·Cu(OH)2、CuSiO3·2H2O, 含SiO2、FeCO3、Fe2O3等杂质]为原料制备CuCl2的工艺流程如下:
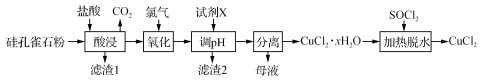
已知: SOCl2+H2O![]() SO2↑+2HCl↑
SO2↑+2HCl↑
(1) “酸浸”时盐酸与 CuCO3·Cu(OH)2 反应的化学方程式为 ________________。 为提高“酸浸”时铜元素的浸出率,可以采取的措施有:①适当提高盐酸浓度;②适当提高反应温度;③______________。
(2) “氧化”时发生反应的离子方程式为__________________。
(3) “滤渣 2”的主要成分为_______(填化学式);“调pH”时,pH 不能过高,其原因是___________。
(4) “加热脱水”时, 加入 SOCl2的目的是_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图。下列叙述正确的是( )
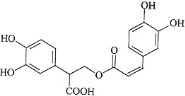
A.迷迭香酸属于芳香烃
B.1mol迷迭香酸最多能和9mol氢气发生加成反应
C.迷迭香酸可以发生水解反应、取代反应和酯化反应
 D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)对于反应2S02(g)+O2(g)=2SO3(g),当其他条件不变时,只改变一个反应条件。将生成SO3的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
编号 | 改变的条件 | 生成SO3的速率 |
① | 降低温度 | |
② | 压缩体积 | |
③ | 使用催化剂 |
(2)用铜片、锌片和稀硫酸及若干其他器材组合成一个原电池.如图所示。回答下列问题:
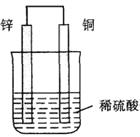
① 该原电池装置将_______(选填“化学能转化为电能”或“电能转化为化学能”);
② 此电池的负极是______,正极的电极反应方程式是________。
③ 该电池工作一段时间,将两个电极小心取出洗涤并晾干,经称量发现锌片比原来减少6.5g(锌的相对原子质量为:65)。请计算理论上导线中共通过了____mol电子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com