
科目: 来源: 题型:
【题目】已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
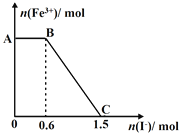
A. 图中AB段的氧化剂为K2Cr2O7
B. 图中BC段发生的反应为2Fe3++2I-=2Fe2++I2
C. 开始加入的K2Cr2O7为0.25 mol
D. K2Cr2O7可与FeSO4反应的物质的量为1:3
查看答案和解析>>
科目: 来源: 题型:
【题目】将中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用。有机物M是中药狼把草的成分之一,其结构如下图所示。下列叙述不正确的是( )

A.M是芳香族化合物,它的分子式为C9H6O4
B.1 mol M最多能与3 mol Br2发生反应
C.1 mol M最多能与含有3 mol NaOH的溶液发生反应
D.在一定条件下,M能发生取代、加成、水解、氧化等反应
查看答案和解析>>
科目: 来源: 题型:
【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
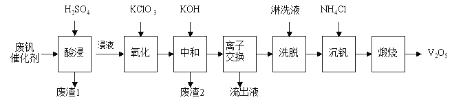
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为____________mol。
(3)“中和”作用之一是使钒以V4O124-形式存在于溶液中。“废渣2”中含有_____________。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+![]()
![]() R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈___________性(填“酸”“碱”“中”)。
R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈___________性(填“酸”“碱”“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质性质的描述和该性质的应用均正确的是( )
A.氨气具有氧化性,用浓氨水检验氯气管道是否泄漏
B.氢氟酸具有强酸性.用氢氟酸蚀刻玻璃
C.二氧化硫具有还原性,用二氧化硫水溶液吸收溴蒸气
D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关油脂的叙述中,错误的是
A.油脂分子结构中三个烃基一定相同
B.可以用纯碱溶液去除油污
C.可以用纯碱区别植物油和柴油
D.工业上可用油脂制造高级脂肪酸
查看答案和解析>>
科目: 来源: 题型:
【题目】铜单质及其化合物在很多领域中都有重要的用途。请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
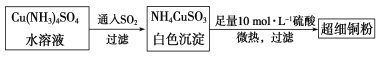
①NH4CuSO3中金属阳离子的核外电子排布式为______。N、O、S三种元素的第一电离能大小顺序为______________(填元素符号)。
②SO42-的空间构型为________,与SO42-互为等电子体的有机分子的化学式为_________。
(2)某学生用硫酸铜溶液与氨水做了一组实验,CuSO4溶液中加氨水生成蓝色沉淀,再加氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体,请解释加入乙醇后析出晶体的原因_______________;在该晶体中存在的化学键的种类有_____________。
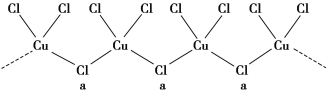
(3)氯和钾与不同价态的铜可生成两种化合物,其阴离子均为无限长链结构(如图所示),a位置上Cl原子的杂化轨道类型为________。已知其中一种化合物的化学式为KCuCl3,则另一种化合物的化学式为____________。
(4)用晶体的X射线衍射法可以测得阿伏加德罗常数的值。对金属铜的测定得到以下结果:铜晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.00 g·cm-3,则铜原子的直径约为__________pm,求算阿伏加德罗常数的表达式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料。某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下三种实验方案。(已知:AlN+NaOH+ 2H2O==NaAlO2+ NH3)
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。

(1)上图C装置中球形干燥管的作用是 。
(2)完成以下实验步骤:组装好实验装置,首先检查气密性,再加入实验药品,接下来的实验操作是 ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是 。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见 。
【方案2】用下图装置测定m g样品中A1N的纯度(部分夹持装置已略去)。

(4)为测定生成气体的体积,量气装置中的X液体可以是___________
A.CCl4 B.H2O C.NH4Cl溶液 D.苯
(5)若m g样品完全反应,测得生成气体的体积为V mL(已转换为标准状况),则AIN的质量分数是__________。
【方案3】按以下步骤测定样品中A1N的纯度:

(6)步骤②生成沉淀的离子方程式为________________
(7)若在步骤③中未洗涤,测定结果将__________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法没有科学性错误的是 ( )
A. “白雪牌”漂白粉可令所有有色物质黯然失“色”,没有最白,只有更白
B. CO有毒,生有煤炉的居室,可放置数盆清水,这样可有效地吸收CO,防止煤气中毒
C. 氯化钙具有吸水性和潮解性,夏日里用它的水溶液喷洒柏油路,可有效地保护路面
D. 氯元素有毒,禁止放入口中
查看答案和解析>>
科目: 来源: 题型:
【题目】在①乙醇与氧气在铜催化下反应;②淀粉在稀硫酸作用下在水中加热;③葡萄糖与钠反应;④乙醇一定条件下与乙酸反应中,不包括的反应类型是
A.氧化反应 B.加成反应 C.酯化反应 D.水解反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于常见有机物的说法正确的是
A.乙烯和苯都能和溴水发生化学反应而使溴水褪色
B.乙烷可使酸性高锰酸钾溶液褪色
C.糖类和蛋白质都是高分子化合物
D.乙酸和油脂都能与氢氧化钠溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com