
科目: 来源: 题型:
【题目】雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如下的实验:

已知:3NO3-+ 8Al + 5OH-+ 18H2O = 3NH3+ 8[Al(OH)4]-
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
A. 试样中一定不含Al3+
B. 试样中肯定存在NH4+、Mg2+、SO42-和NO3-
C. 试样中可能存在Na+、Cl-
D. 该雾霾中可能存在NaNO3、NH4Cl和MgSO4
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案。
方案一 滴定法:用酸性KMnO4溶液滴定,测定铁元素的含量
(1)写出该滴定反应的离子方程式 。
(2)某同学设计的下列滴定方式中,最合理的是________(夹持部分略去)(填字母序号)
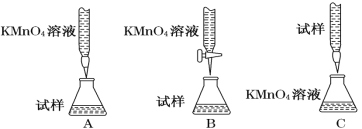
(3)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、药匙、烧杯、胶头滴管外,还需 (填仪器名称)。
在溶液配制过程中,下列操作会导致配制结果偏低的是___________(填写代号)。
a. 定容时,俯视容量瓶刻度线
b. 容量瓶在使用前内有少量蒸馏水
c. 转移溶液后的烧杯、玻璃棒未洗涤
d. 定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(4)上述实验中KMnO4溶液需要酸化,用于酸化的酸是________。
a.浓盐酸 b.稀硫酸 c.稀硝酸 d.浓硫酸
方案二 称量法:操作流程如下:

(5)写出步骤②中H2O2氧化Fe2+ 的离子方程式______ __。
步骤②中除用H2O2外还可以使用的物质是
步骤②是否可以省略 ,理由是 。
(6)步骤④一系列操作依次是:过滤、洗涤、 、冷却、称量。
(7)假设实验无损耗,则每片补血剂含铁元素的质量 g(用含a的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)冶炼金属的三种常用方法是:A.热分解法 B.热还原剂法 C.电解法。人类用量处在前三位的金属是铁、铝、铜。(填编号)(化学方程式书写每空2分,其余每空1分)
① 冶炼铝用到的方法是 ;
② 冶炼铁和铜的常用方法是 。
③ 写出电解熔融氯化镁制取金属镁的化学反应方程式: 。
(2)保护环境、保护地球已成为人类共同的呼声。(化学方程式书写每空2分,其余每空1分)
① 引起温室效应的主要物质是 ;
②以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的气体是 ,形成过程发生的化学反应有: 、 (写出两个)。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A是周期表中半径最小的元素,C的最外层电子数是内层电子的3倍;F元素是同周期元素中原子半径最小的主族元素。A、B、C、D、E形成的化合物甲、乙、丙、丁的组成如表所示:
化合物 | 甲 | 乙 | 丙 | 丁 |
化学式 | A2C | A2C2 | D2C2 | D2E |
回答下列问题:
(1)指出元素F在周期表中的位置__________________。
(2)化合物乙的电子式为_____________,用电子式表示形成化合物丁的过程_____ 。
(3)写出丙与甲反应的离子方程式:___________________。
(4)固体氧化物燃料电池是以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许O2–在其间通过,该电池的工作原理如图所示,其中多孔Pt电极a、b分别是气体C2、A2的载体。该电池的负极为____(填a或b);O2–流向____极(填“正”或“负”);该电池的正极反应式为 _____。
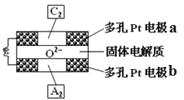
查看答案和解析>>
科目: 来源: 题型:
【题目】我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库。目前,世界各国都在研究如何充分利用海洋资源。全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65 mg·L-1。其工业提取法有:
(1)空气吹出纯碱吸收法。方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到单质溴。该方法涉及的反应有:
①_______________________________________ (写出离子方程式);
②3Br2+3CO32—=BrO3—+5Br-+3CO2↑;
③_______________________________________ (写出离子方程式);
(2)空气吹出SO2吸收法。该方法基本同(1),只是将吹出的溴用SO2溶液来吸收,使溴转化为氢溴酸,然后再用氯气氧化氢溴酸即得单质溴。写出溴与二氧化硫反应的化学方程式____________。
(3)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上可采用“硫化氢-水双温交换法”富集HDO。其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO。下图为“硫化氢-水双温交换法”所发生的两个反应中涉及的四种物质在反应体系中的物质的量随温度的变化曲线。写出100℃时所发生的反应的化学方程式______;工业上富集HDO的生产过程中,可以循环利用的一种物质是____。

查看答案和解析>>
科目: 来源: 题型:
【题目】在室温时,同种规格的铝片分别与下列物质混合,反应开始时生成氢气速率最大的是
A.0.1mol/L盐酸15ml
B.0.15mol/L硫酸8ml
C.0.2mol/L盐酸12ml
D.18mol/L硫酸15ml
查看答案和解析>>
科目: 来源: 题型:
【题目】下表中物质的分类组合完全正确的是
编号 | A | B | C | D |
强电解质 | Ba(OH)2 | 盐酸 | HClO4 | BaSO4 |
弱电解质 | HI | CaCO3 | HClO | NH3·H2O |
非电解质 | SO2 | NH3 | Cl2 | 乙醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com