
科目: 来源: 题型:
【题目】用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ..再经过一系列操作,分离得到产品。
(1)步骤Ⅰ中过滤所得滤渣主要成分为:______________________,
H2SO4溶解Al2O3的离子方程式为:_____________________。
(2)步骤Ⅱ中加入KMnO4时发生反应的离子方程式为: 。
(3)已知:生成氢氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 |
完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度均为0.1 mol·L-1
①根据表中数据解释步骤Ⅱ的目的:________________________,
②当Al3+开始沉淀时,Fe3+的浓度约为:_______________________。
(4)已知:一定条件下,MnO![]() 可与Mn2+反应生成MnO2。
可与Mn2+反应生成MnO2。
①向Ⅲ的沉淀中加入浓盐酸并加热,能说明沉淀中存在MnO2的现象是: 。
②步骤Ⅳ中加入MnSO4的目的是: 。
(5)步骤Ⅴ中“一系列操作”是__________________、_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质分类的叙述正确的是( )
A.NaCl晶体不导电,所以NaCl是非电解质
B.Na2O2能与酸反应,所以Na2O2是碱性氧化物
C.BaSO4难溶于水,但BaSO4是强电解质
D.NH4Cl不含有金属离子,所以NH4Cl不是盐
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物在气态时与相同状况下的H2的密度之比为30∶1,又知12.0 g该有机物与足量钠反应放出0.2 g H2,且不能发生银镜反应,符合条件的有机物可能有( )
A.2种 B.3种 C.4种 D.6种
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列各组物质:
A.金刚石与石墨;
B.淀粉与纤维素;
C.氕与氘;
D.甲烷与戊烷;
E.葡萄糖与果糖
F.![]() 与
与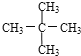
G.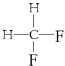 与
与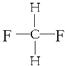
其中互为同位素 ;(填编号.下同),互为同系物的是 ,互为同分异构体的是 ,是同一种物质的是 .
(2)120℃,101kpa下,9ml由CO和C2H4组成的混合气体在足量的O2中完全燃烧后,恢复到原温度和压强.测得混合气体完全燃烧所消耗O2的体积与生成CO2的体积相等.请回答下列问题。
①等体积的CO和C2H4在相同条件下完全燃烧,生成CO2的体积比为 ;消耗O2的体积比为 .
②燃烧前混合气体中CO的体积为 , C2H4的体积为 .
(3)①化合物A的结构简式为: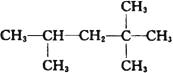 ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_______________;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为__________________。
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_______________;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为__________________。
②篮烷分子的键线式如图所示,试回答:

I写出篮烷分子的化学式____________;II篮烷分子的一氯取代物的种数为_______种。
(4)元素氮的一种液态氢化物叫肼,其分子中氮原子与氢原子个数比为1:2.肼﹣空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%﹣30%的KOH溶液.氮元素对应的燃烧产物为N2。该燃料电池的负极的电极反应式是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
A.2.4g镁在足量的O2 、CO2、 N2混合气体中燃烧,转移的电子数为0.1NA
B.标况下,11.2 L氯气完全溶于1 L水中,所得溶液中Cl﹣和ClO﹣两种粒子数之和为NA
C.0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA
D.标准状况下,20gD2O分子中所含中子数为10NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学采用工业大理石(含有少量SiO2、Al2O3、Fe2O3等杂质)制取CaCl2·6H2O,设计了如下流程:

下列说法不正确的是( )
A.固体Ⅰ中含有SiO2,固体Ⅱ中含有Fe(OH)3
B.使用石灰水时,要控制pH,防止固体Ⅱ中Al(OH)3转化为AlO2-
C.从溶液Ⅲ得到CaCl2·6H2O产品的过程中,须控制好条件防止产物分解
D.若改变实验方案,在溶液Ⅰ中直接加氨水至沉淀完全,滤去沉淀,其溶液经蒸发浓缩、冷却结晶也可得到纯净CaCl2·6H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫研究。
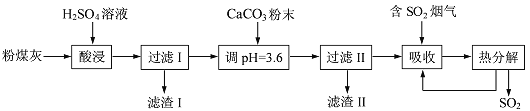
(1)酸浸时反应的化学方程式为___________;滤渣I的主要成分为____________(填化学式)。
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6-2x。滤渣II的主要成分为___________(填化学式);若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是___________________(用离子方程式表示)。
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是____________;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将__________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、 CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:
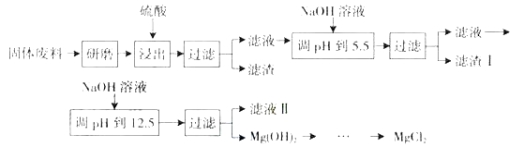
部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下表,请回答下列问题:
沉淀物 | Fe3+ | Al3+ | Mg2+ |
PH | 3.2 | 5.2 | 12.4 |
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有 (要求写出两条)。
(2)滤渣I的主要成分有 。
(3)从滤液Ⅱ中可回收利用的主要物质有 。
(4)若将MgCl2溶液加热蒸干得到的固体是__________,若要得到MgCl2应采取的操作是___________。
(5)用稀硫酸酸浸时形成滤渣的离子方程式有_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 元素周期律是元素原子核外电子排布周期性变化的结果
B. HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱
C. 第三周期非金属元素含氧酸的酸性从左到右依次增强
D. 形成离子键的阴、阳离子间只存在静电吸引力
查看答案和解析>>
科目: 来源: 题型:
【题目】氯的原子序数为17,37Cl和35Cl是氯的两种同位素,下列说法正确的是()
A. 35Cl原子所含质子数为18
B. ![]() mol的H35Cl分子所含中子数约为6.02×1023
mol的H35Cl分子所含中子数约为6.02×1023
C. 3.5 g的35Cl2气体的体积为2.24 L
D. 35Cl2气体的摩尔质量为70
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com