
科目: 来源: 题型:
【题目】下列叙述错误的是( )
A.离子键没有方向性和饱和性,而共价键有方向性和饱和性
B.离子键的强弱主要决定于离子半径和离子所带电荷数
C.配位键在形成时,由成键双方各提供一个电子形成一对共用电子
D.金属键的实质是金属中的自由电子与金属阳离子形成的一种强烈的相互作用
查看答案和解析>>
科目: 来源: 题型:
【题目】第二次世界大战期间丹麦科学家玻尔被迫离开德军占领的祖国。为了表明一定要返回祖国的决心,他把心爱的金质诺贝尔奖章放在盛有“王水”(浓盐酸和浓硝酸的混合物)的玻璃容器中:Au+HNO3+3HCl=AuCl3+NO↑+2H2O。战后玻尔返回祖国,从溶液中提取出金,又重新铸造成奖章。下列方法中,不能从溶有金的王水中提取出金的是
A.萃取 B.蒸发灼烧 C.用Fe置换 D.电解
查看答案和解析>>
科目: 来源: 题型:
【题目】某可逆反应为2X(g) ![]() 3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:
3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:
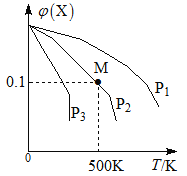
下列推断正确的是
A.升高温度,该反应平衡常数K减小
B.压强大小为:P3>P2>P1
C.平衡后加入高效催化剂使Mr增大
D.在该条件下M点X平衡转化率为
查看答案和解析>>
科目: 来源: 题型:
【题目】将质量为12.64gKMn04固体加热一段时间后,收集到amol 02;向反应后残留的固体中加入足量的浓盐酸,又收集到bmolCl2,此时Mn元素全部以Mn2+的形式存在于溶液中。(KMn04 的摩尔质量为158g/mol )
(1)请完成并配平下列化学方程式:
_______K2MnO4+_______HCl----________KCl+________MnCl2+_______Cl2↑+________
该反应中的还原剂是_________,当该反应中转移NA个电子时,氧化产物的物质的量为________mol,被氧化的还原剂的物质的量为_________mol 。
(2)用酸性高锰酸钾溶液滴定FeS04溶液写出该反应的离子方程式:____________。
(3)当KMn04固体加热生成O2 amol值最大时,向反应后残留的固体中加入足量的浓盐酸并加热,产生Cl2的物质的量b=_______mol 。(此时Mn元素全部以Mn2+的形式存在于溶液中)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质发生变化时,所克服的粒子间相互作用完全相同的是( )
A.液态HF与液态HBr分别受热变为气体
B.氯化铵与苯分别受热变为气体
C.氯化钠与氯化氢分别溶解在水中
D.碘与干冰分别受热变为气体
查看答案和解析>>
科目: 来源: 题型:
【题目】北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子化合物,具有良好的超导性。下列有关分析正确的是( )
A.K3C60中只有离子键 B.K3C60中不含共价键
C.该晶体在熔融状态下能导电 D.C60与12C互为同素异形体
查看答案和解析>>
科目: 来源: 题型:
【题目】化学科学与技术是改进生活、改善环境.促进发展的关键。下列说法正确的是 ( )
A.普通玻璃、氮化硅陶瓷、水晶饰物都是硅酸盐制品
B.“乙醇汽油”的主要成分都是可再生能源
C.碱石灰、硫酸铜、硅胶都可用作食品干燥剂
D.“天宮”系列飞船使用的碳纤维材料、光导纤维都是新型无机非金属材料
查看答案和解析>>
科目: 来源: 题型:
【题目】部分氧化的铁铜合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:
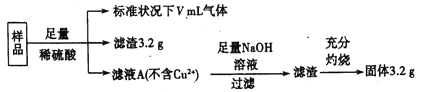
下列说法正确的是( )
A.滤液A中的阳离子为Fe3+、Fe2+、H+ B.样品中Fe元素的质量为2.24g
C.样品中CuO的质量为4.0g D.V=896
查看答案和解析>>
科目: 来源: 题型:
【题目】金刚砂(SiC)可由SiO2和碳在一定条件下反应制得,反应方程式为:SiO2 + 3C![]() SiC + 2CO↑,下列有关说法中正确的是
SiC + 2CO↑,下列有关说法中正确的是
A.该反应中的氧化剂是SiO2,还原剂为C
B.该反应中的氧化剂和还原剂的物质的量之比为1︰3
C.该反应中每生成1 mol SiC转移4 mol电子
D.该反应中的还原产物是SiC,氧化产物是CO,其物质的量之比为1︰2
查看答案和解析>>
科目: 来源: 题型:
【题目】氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺(NH2Cl)、二氯胺(NHCl2)和三氯胺(NCl3)。氯胺消毒时首先发生水解,生成具有强烈杀菌作用的次氯酸。
(1)NH2Cl中氯元素的化合价为___________,其电子式为__________。
(2)NH2Cl水解的离子方程式为____________。
(3)三氯胺在常温下为黄色黏稠的油状液体,有毒,在弱酸性溶液中稳定性较好。将0.01 mol NCl3通入100mL0.5mol/LNa2S03溶液中,转移电子的物质的量为___________。
(4)己知:2NH3(g)+3C12(g)=N2(g)+6HCl(g)△H1=-469kJ/mol
N2(g)+3C12(g)=2NC13(g) △H2=+520kJ/mol
NH3(g)+3C12(g)= NC13(g)+ 3HCl(g)△H3
则△H3=__________kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com