
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数值。下列说法正确的是
A.常温常压下,4.4g乙醛所含σ键数目为0.7NA
B.标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5 NA
C.12g石墨烯(单层石墨)中含有六元环的个数为0.5NA
D.50ml浓度为18.4mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学在画某种元素的一种单核微粒的结构的示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
![]()
(1)该微粒是中性微粒,这种微粒的符号是
(2)该微粒的还原性很弱,失去1个电子后变为原子,原子的氧化性很强,该单质与水反应的化学方程式:
(3)该微粒的还原性很弱,失去2个电子后变成原子,该元素在周期表中的位置为
(4))该微粒的氧化性很弱,得到1个电子后变为原子,原子的还原性很强,该单质与水反应的化学方程式 .
(5)该微粒的符号为X3﹣,则这种微粒的单质的电子式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】反应3X(g)+Y(g)![]() 2Z(g)+2W(g)在 2L密闭容器中进行,10min后 Y减少了1.0mol,则此反应的平均速率v为( )
2Z(g)+2W(g)在 2L密闭容器中进行,10min后 Y减少了1.0mol,则此反应的平均速率v为( )
A.v(X)=0.05mol·L-1·min-1 B.v(Z)=0.10mol·L-1·min-1
C.v(Y)=0.10mol·L-1·min-1 D、v(W)=0.05mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.汽油与水不相溶,可以用裂化汽油萃取溴水中的溴
B.石油含有烷烃、环烷烃、芳香烃,煤含有苯、甲苯、二甲苯等有机物
C.煤的气化、液化是使煤变成清洁能源,减小环境污染的有效途径
D.沸点范围:汽油>煤油>柴油>重油
查看答案和解析>>
科目: 来源: 题型:
【题目】800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g) ![]() 2NO2(g) n(NO)随时间的变化如表:
2NO2(g) n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO) (mol) | 0.020 | 0.010 | 0.009 | 0.008 | 0.008 | 0.008 |
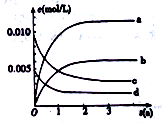
A.a线表示NO2的变化趋势,则0~2s内v(NO2)=0.006mol/(L·s)
B.800℃时,该反应的平衡常数K=1125L/mol
C.能使该反应的反应速率增大,且平衡向正方向移动的措施是及时分离出NO2
D.已知:K300℃>K350℃,则该反应时吸热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】苯酚的化学式是C6H6O,是一种有毒的物质,对皮肤、黏膜有强烈的腐蚀作用.2014年6月,一辆载有近30吨苯酚的槽罐车侧翻,约有10吨的苯酚泄漏,造成很大程度的污染.
(1)你认为下列对事故的处理方法合理的是 .
A、用碱性溶液冲洗可以减少苯酚的挥发
B、挖隔离沟、铺膜防止扩散并回收泄漏的苯酚
C、随时监测附近水源、土壤中的苯酚的含量
D、用水溶解后回收
(2)用木屑吸附残余的苯酚,然后点火燃烧除去.写出苯酚在空气中完全燃烧的化学方程式: .
(3)如图是从苯酚的乙醇溶液中分离回收苯酚的操作流程图:
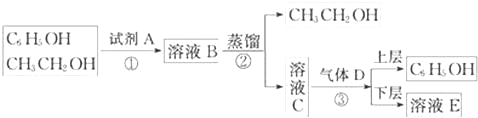
根据图示完成下列问题:
①试剂A的化学式为 .
②步骤③的操作名称为 .
③写出C+D﹣→E+C6H5OH的化学方程式: .
查看答案和解析>>
科目: 来源: 题型:
【题目】“神十搭载的长征F改进型火箭推进剂之一为无色气体N2O4.N2O4与NO2转换的热化学方程式为:N2O4(g) ![]() 2NO2(g) △H=+24.4KJ/mol
2NO2(g) △H=+24.4KJ/mol
(1)将一定量N2O4投入固定容积的真空容器中,下述现象能说明反应达到平衡的是 。
a.v正(N2O4)=2v逆(NO2) b.体系颜色不变
c.气体平均相对分子质量不变 d.气体密度不变
达到平衡后,保持体积不变升高温度,再次到达平衡时,则混合气体颜色 (填“变深”、“变浅”或“不变”),判断理由____________________。
(2)平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数(例如:p(NO2)=p总×x(NO2)。写出上述反应平衡常数Kp表达式 (用p总、各气体物质的量分数x表示)。影响Kp的因素为___________;
(3)上述反应中,正反应速率v正=k正·p(N2O4),逆反应速率v逆=k逆·P2(NO2),其中k正、k逆为速率常数,则Kp为________(以k正、k逆表示)。若将一定量N2O4投入真空容器中恒温恒压分解(温度298K、压强100kPa),已知该条件下k正=4.8×l04s-1,当N2O4分解10%时,v正=__________kPa·s-1;
(4)真空密闭容器中放入一定量N2O4,维持总压强p0恒定,在温度为T时,平衡时N2O4分解百分率为a。保持温度不变,向密闭容器中充人等量N2O4,维持总压强在2p0条件下分解,则N2O4的平衡分解率的表达式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关系互为同分异构体的是
A. 35Cl和37Cl B. CH3CH2OH和CH3OCH3
C. CH3CH3和CH3CH2CH3 D. H2O和H2O2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于实验现象的描述不正确的是
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.原电池放电时,电流的方向是从正极到负极
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com