
科目: 来源: 题型:
【题目】含汞废水主要来源于氯碱工业和塑料工业,未经处理不得排放.某含汞酸性废水(主要含Hg2+、H+、Na+、Cl﹣等)的处理工艺流程如图所示.
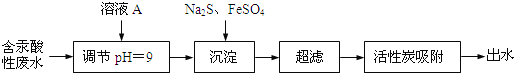
请回答:
(1)含汞废水未经处理直接排放的危害是(填字母) .
a.造成水体污染 b.引起人体中毒
(2)调节废水pH时加入的溶液A可能是(填字母) .a.盐酸b.NaOH溶液
(3)Na2S与Hg2+发生反应的离子方程式是 .
(4)该废水经处理后,测得有关数据如下(其他离子忽略不计):
离子 | Na+ | Fe2+ | Cl﹣ | SO42﹣ |
浓度(mol/L) | 3.0×10﹣4 | 2.0×10﹣4 | 2.5×10﹣4 |
则c(Fe2+)= mol/L.
查看答案和解析>>
科目: 来源: 题型:
【题目】标准状况下,m g气体A与n g气体B的分子数目一样多,下列说法不正确的是( )
A. 在任意条件下,若两种分子保持原组成,则其相对分子质量之比为m∶n
B. 25 ℃、1.25×105 Pa时,两气体的密度之比为n∶m
C. 同质量的A、B在非标准状况下,其分子数之比为n∶m
D. 相同状况下,同体积的气体A与B的质量之比为m∶n
查看答案和解析>>
科目: 来源: 题型:
【题目】已知甲烷(CH4)在一定条件下催化氧化可以生成乙烯(C2H4)、乙烷(C2H6)气体(水和其他产物忽略不计)。取一定量甲烷经催化氧化得到的混合气体在标准状况下的密度为0.85 g/L,实验测得反应中甲烷消耗了40.0%,求所得混合气体中乙烯的体积百分含量。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:HCl + NH3= NH4Cl(固体)如下图所示,抽去装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度。下列说法正确的是( )
![]()
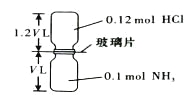
A. 反应后瓶内压强是反应前的1/10 B. 装置中氢元素的总质量为0.42 g
C. 生成物的分子数目为0.1 NA D. 反应结束后,两个集气瓶很容易分开
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中,可以说明恒容密闭容器中的反应:P(g)+Q(g)![]() R(g)+S(g)在恒温下已达平衡状态的是
R(g)+S(g)在恒温下已达平衡状态的是
A.反应容器内压强不随时间变化
B. P和S的生成速率相等
C.反应容器内P、Q、R、S四者物质的量浓度为1:1:1:1
D.反应容器内总物质的量不随时间而变化
查看答案和解析>>
科目: 来源: 题型:
【题目】锌银电池能量大、电压平稳,广泛用于电子手表、照相机、计算器和其他微型电子仪器.电解质溶液是KOH溶液,电池总反应为Zn+Ag2O═ZnO+2Ag请回答下列问题:
①该电池的负极材料是 ;电池工作时,阳离子向 (填“正极”或“负极”)移动;
②电极材料锌可由闪锌矿在空气中煅烧成氧化锌,然后用碳还原来制取,反应的化学方程式为ZnO+C![]() Zn+CO↑,此法为 .
Zn+CO↑,此法为 .
A.电解法 B.热还原法 C.热分解法.
查看答案和解析>>
科目: 来源: 题型:
【题目】纯净的水呈中性,这是因为( )
A. 纯水中c(H+)= c(OH-) B. 纯水PH=7
C. 纯水的离子积KW=1.0×10-14 D. 纯水中无H+也无OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法中正确的是
A. 标准状况下,11.2L的戊烷所含的分子数为0.5NA
B. 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA
C. 28g乙烯所含共用电子对数目为4NA
D. 1mol甲基的电子数目为10NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是
A. 植物油中由于含有碳碳双键,因此在空气中长时间放置容易氧化变质
B. 利用乙醇的氧化性以及Cr3+、Cr2O72-的颜色差异来检验酒后驾车
C. 石油可以通过裂解、裂化等物理变化获得重要化工原料乙烯
D. 黄河入海口沙洲的形成体现了胶体电泳的性质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com