
科目: 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是其电子层数的2倍;Y的气态氢化物可以使湿润的红色石蕊试纸变蓝;液态Z可作为核反应堆的热传导剂;W与X原子最外层电子数之比为3∶2。下列说法正确的是( )
A. 化合物Z2O2含有离子键和极性共价键
B. 原子半径大小:W>Z>X>Y
C. WO2能使品红溶液褪色,其漂白原理与氯水类似
D. Y的气态氢化物与其最高价氧化物的水化物可反应生成盐
查看答案和解析>>
科目: 来源: 题型:
【题目】与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚氯酸钠和稀盐酸为原料制备ClO2,反应如下:
NaClO2+HCl→ClO2↑+NaCl+H2O(没有配平)
(1)配平方程式。
![]() NaClO2+
NaClO2+![]() HCl—
HCl—![]() ClO2↑+
ClO2↑+![]() NaCl+
NaCl+![]() H2O
H2O
(2)该反应中氧化剂和还原剂的物质的量之比_______________________。生成0.2 mol ClO2转移电子的物质的量为________mol。
(3)ClO2对污水中的Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某污水中含CN- a mg·L-1,现用ClO2将CN-氧化,只生成两种无毒气体。处理100 m3这种污水,至少需要ClO2________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式。如果将它们按原子序数递增的顺序排列,可形成图①所示的“蜗牛”形状,图中每个“.”代表一种元素,其中P点代表氢元素。
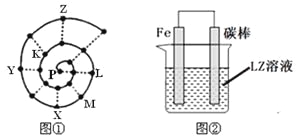
(1)X元素在常规周期表中的位置 (填周期和族)。
(2)写出M与Z两种元素形成的化合物的电子式 。
(3)下列说法正确的是_______
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2
d.由K、L两种元素组成的化合物中可能含有共价键
(4)图②装置可以模拟钢铁的腐蚀,铁棒一极的电极反应式是 。若在图②溶液中滴加少量酚酞溶液并进行电解,发现Fe电极附近溶液变红,写出该电解池的离子方程式 _。牺牲阳极的阴极保护法利用的是 _原理(填“电解池”或“原电池”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】废旧显示屏玻璃中含有SiO2、Fe2O3、CeO2、FeO等物质。某课题小组以此玻璃粉末为原料,制得Ce(OH)4和硫酸铁铵矾[化学式为xFe2(SO4)3·y(NH4)2SO4·zH2O],流程设计如下:

已知:Ⅰ、酸性条件下,铈在水溶液中有Ce3+、Ce4+两种主要存在形式,Ce4+有较强氧化性;
Ⅱ、CeO2不溶于稀硫酸,也不溶于氢氧化钠溶液。
回答以下问题:
(1)操作①的名称是_____________;该操作所用的玻璃仪器有:烧杯、_________、_________。
(2)反应(2)中过氧化氢的作用是:_________________________。
(3)反应(3)的离子方程式是:_____________________。
(4)已知有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为:
2Ce3+(水层)+6HT(有机层)![]() 2CeT3(有机层)+6H+(水层)
2CeT3(有机层)+6H+(水层)
从平衡角度解释:向CeT3(有机层)加入硫酸获得较纯的含Ce3+的水溶液的原因是_________________。
(5)硫酸铁铵矾广泛用于水的净化处理,其净水原理用离子方程式表示为:_________________。
(6)相同物质的量浓度的以下四种溶液中,铵根离子浓度由大到小的顺序是:_________________。
a.xFe2(SO4)3·y(NH4)2SO4·zH2O
b.(NH4)2SO4
c.(NH4)2CO3
d.NH3·H2O
(7)为测定某硫酸铁铵矾样品的组成,现称取14.00 g该样品,将其溶于水配制成100 mL溶液;再将溶液分成两等份,向其中一份加入足量氢氧化钠溶液,过滤、洗涤沉淀、再烘干灼烧至恒重,得到1.60 g固体;向另一份溶液中加入0.5 mol/L硝酸钡溶液100 mL,恰好完全反应。则该硫酸铁铵矾的化学式为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在下图所示的物质转化关系中,A是常见的气态氢化物,其水溶液呈碱性,B是能使带火星的木条复燃的无色无味气体, G是一种红色金属单质。(部分反应中生成物没有全部列出,反应条件未列出)

请回答下列问题:
(1)反应①的化学方程式为 。当有1molA参加反应时,转移 mol电子。
(2)反应②的化学方程式为 。
(3)反应③的离子方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】胰岛素是含有51个氨基酸的蛋白质,控制合成胰岛素的DNA和RNA分子中至少有碱基的数目分别是 ( )
A. 51和51 B. 153和51 C. 153和153 D. 306和153
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.活化分子之间的碰撞即为有效碰撞
B.使用催化剂能降低活化能,增加活化分子百分数
C.增大压强不能降低活化能,但能增加活化分子百分数
D.活化能的大小决定了反应能否自发进行
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置(图1),用环己醇制备环己烯:
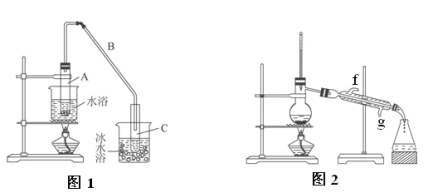
已知: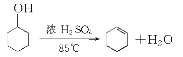
密度(g· cm-3) | 熔点(℃) | 沸点℃ | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品:将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是__________________。
②试管C置于冰水浴中的目的是___________________。
(2)制备精品:
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在________层(填“上”或“下”),分液后用____________(填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图2装置蒸馏,冷却水从________口进入。蒸馏时加入生石灰,目的是__________。
③收集产品时,控制的温度应在__________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是___________(填选项符号)
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是____________。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com