
科目: 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,下列各项对示意图的解释与图象相符的是
2NH3(g) ΔH<0,下列各项对示意图的解释与图象相符的是
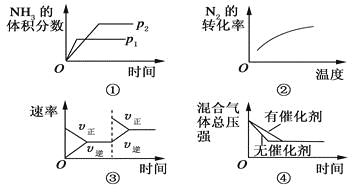
A. ①压强对反应的影响(p2>p1) B. ②温度对反应的影响
C. ③平衡体系增加N2对反应的影响 D. ④催化剂对反应的影响
查看答案和解析>>
科目: 来源: 题型:
【题目】相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.6 kJ·mol-1。
2NH3(g) ΔH=-92.6 kJ·mol-1。
实验测得起始、平衡时的有关数据如下表所示:
容器 | 起始时各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15 kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述错误的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数相等
C.若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
D.容器②中达平衡时放出的热量Q=23.15 kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量的稀硫酸与足量的铝粉反应时,为了减缓反应速率,且不影响生成氢气的总量,应向稀硫酸中加入适量的
A.KOH(固体) B.CH3COOH C.KCl(固体) D.CH3COOK(固体)
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下MO3-与M-发生反应:MO3—+5M-+6H+=3M2 +3H2O,则下列关于M元素的叙述中正确的是
A. M位于元素期表的笫VA族
B. M的氢化物的水溶液呈酸性
C. MO3-中的M元素只能被还原
D. M2在常温常压下一定是气体
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应N2+3H2 ![]() 2NH3的能量变化下图所示,该反应的热化学方程式是
2NH3的能量变化下图所示,该反应的热化学方程式是
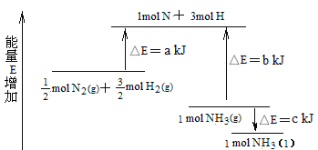
A.N2(g)+3H2(g) ![]() 2NH3(l) △H = 2(a-b+c) kJ/mol
2NH3(l) △H = 2(a-b+c) kJ/mol
B.N2(g)+3H2(g) ![]() 2NH3(l) △H = 2(a-b-c) kJ/mol
2NH3(l) △H = 2(a-b-c) kJ/mol
C.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g) ![]() NH3(l) △H = (b+c-a) kJ/mol
NH3(l) △H = (b+c-a) kJ/mol
D.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g) ![]() NH3(g) △H = (a+b) kJ/mol
NH3(g) △H = (a+b) kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】在体积、温度都相同的条件下,反应2A(g)+2B(g) ![]() C(g)+3D(g)分别从下列两条途径建立平衡:
C(g)+3D(g)分别从下列两条途径建立平衡:
Ⅰ.A、B的起始物质的量均为2 mol;
Ⅱ.C、D的起始物质的量分别为2 mol和6 mol。
以下叙述中不正确的是
A.Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成相同
B.Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的平均相对分子质量相同
C.达平衡时,Ⅰ途径的反应速率vA等于Ⅱ途径的反应速率vA
D.达平衡时,Ⅰ途径所得混合气体的密度为Ⅱ途径所得混合气体密度的![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.SiO2![]() SiCl4
SiCl4![]() Si
Si
B.FeS2![]() SO2
SO2![]() H2SO4
H2SO4
C.N2![]() NH3
NH3![]() NH4Cl(aq)
NH4Cl(aq)
D.MgCO3![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
Ⅰ.[查阅资料]
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3,所得产品常含有少量Na2SO3和Na2SO4。
Ⅱ.[制备产品]实验装置如图所示(省略夹持装置):
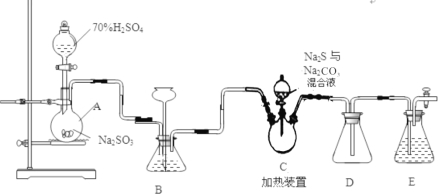
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)(I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l)(II)
S(s)+Na2SO3(aq)![]() Na2S2O3(aq)(III)
Na2S2O3(aq)(III)
实验步骤:
①待Na2S和Na2CO3完全消耗后,结束反应。
②向C中烧瓶加入Na2S和Na2CO3混合溶液
③检查装置气密性,按图示加入试剂。
④向A中烧瓶滴加浓H2SO4。
⑤过滤C中混合物,滤液经蒸发、结晶、过滤、洗涤、干燥,得到产品。
(1)E中的试剂是____________(选填下列字母编号)。
A.稀H2SO4 B.NaOH溶液 C.饱和NaHSO3溶液
(2)正确的操作顺序是
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
Ⅲ.[探究与反思]
(1)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,________________ ,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(2)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进后的操作是___________________。
(3)Na2S2O3·5H2O的溶解度随温度升高显著增大,所得产品通过____________方法提纯。
查看答案和解析>>
科目: 来源: 题型:
【题目】(Ι)HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(2)某同学把新制的氯水加到NaNO2溶液中,请写出反应的离子方程式:________________。
(3)铝能溶解在碱性亚硝酸盐溶液中,生成能使湿润的红色石蕊变蓝的气体,请写出反应的离子方程式__________________;
(Ⅱ)某暗紫色化合物A在常温和干燥的条件下,可以稳定存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀,同时产生一种气体单质。为探究其成分,某学习兴趣小组的同学取化合物A粉末进行试验。经组成分析,该粉末仅含有O、K、Fe三种元素。另取3.96g化合物A的粉末溶于水,滴加足量稀硫酸,向反应后的溶液中加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将洗涤后的沉淀充分灼烧,得到红棕色固体粉末1.60g;将所得滤液在一定条件下蒸发可得到一种纯净的不含结晶水的盐10.44g。
(1)目前,人们针对化合物A的稳定性进行了大量的探索,并取得了一定的进展。
下列物质中有可能提高化合物A水溶液稳定性的是 。
A.醋酸钠 B.醋酸 C.Fe(NO3)3 D.KOH
(2)请设计一个实验方案,研究温度对化合物A溶液稳定性的影响
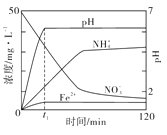
(3)下图表示足量 Fe粉还原KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去)。请根据图中信息写出t1时刻前该反应的离子方程式:
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,Q与水反应的化学方程式为_____________。
(2)NaCN超标的电镀废水可用两段氧化法处理:
1.NaCN与NaClO反应,生成NaOCN和NaCl
2.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
①写出第二次氧化时发生反应的离子方程式。
②(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成____________和H2O。
③处理200 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO_________g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com