
科目: 来源: 题型:
【题目】
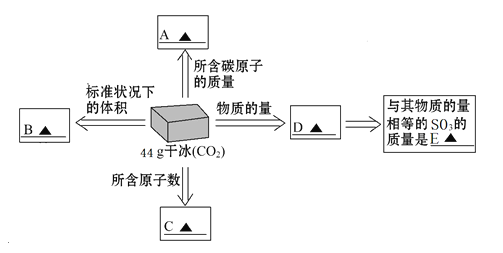
(1)干冰是固态CO2的俗称,常用于人工降雨, 44g干冰与A、B、C、D有如图所示的转化关系,请完成下图中的方框。
(2)标准状况下22.4L的HCl溶于水配成500mL溶液, 所得溶液的物质的量浓度为 。
(3)配制1L 0.5mol·L-1NaOH溶液, 需要1.25 mol·L-1的NaOH溶液的体积是 mL。
(4)19 g MgX2含有Mg2+0.2 mol, 则MgX2的摩尔质量为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,H2(g)+CO2(g)![]() H2O(g)+CO(g)的平衡常数K=
H2O(g)+CO(g)的平衡常数K=![]() 。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是( )
。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是( )
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
A. 平衡时,乙中CO2的转化率大于60%
B. 平衡时,甲中和丙中H2的转化率均是60%
C. 平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)一定温度下,Ksp[Mg3(PO4)2]=6.0×10-29,Ksp[Ca3(PO4)2]=6.0×10-26。向浓度均为0.20mol/L的MgCl2和CaCl2混合溶液中逐滴加人Na3P04,先生成___________沉淀(填化学式);当测得溶液其中一种金属阳离子沉淀完全(浓度小于10-5mol/L)时,溶液中的另一种金属阳离子的物质的量浓度c=____________mol/L。
(2)毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:

①毒重石用盐酸浸取前需充分研磨,目的是_____________________。
②加入NH3·H2O调节PH=8可除去_____________(填离子符号),滤渣II中含____________(填化学式)。加入H2C2O4时应避免过量,原因是_________________。
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.7 |
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)已知25℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100mL该条件下的CaSO4饱和溶液中加入400mL0.01mol/LNa2SO4溶液,下列叙述正确的是

A.溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)比原来的大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小
C.溶液中析出CaSO4固体沉淀.溶液中c(Ca2+)、c(SO42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO42-)比原来的大
查看答案和解析>>
科目: 来源: 题型:
【题目】CH4和H2O(g)可发生催化重整反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)已知:①2CO(g)+O2(g)![]() 2CO2(g)△H1=akJ/mol
2CO2(g)△H1=akJ/mol
②CH4(g)+2O2(g)![]() CO2(g)+2H2O(g)△H2=bkJ/mol
CO2(g)+2H2O(g)△H2=bkJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H3=ckJ/mol
CO2(g)+H2(g) △H3=ckJ/mol
④CH4(g)+H2O(g)![]() CO(g)+3H2(g)△H4
CO(g)+3H2(g)△H4
由此计算△H4=________kJ/mol
(2)T℃时,向1L恒容密闭容器中投入1molCH4和1molH2O(g),发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),经过tmin,反应达到平衡。已知平衡时.c(CH4)=0.5mol/L
CO(g)+3H2(g),经过tmin,反应达到平衡。已知平衡时.c(CH4)=0.5mol/L
①0~tmin内,该反应的平均反应速率v(H2)=____________。
②T℃时,该反应的平衡常数K=___________。
③当温度升高到(T+l00)℃时,容器中c(CO)=0.75mol/L,则该反应是___________反应(填“吸热”或“放热”)。
(3)工业上用CO与H2在催化剂作用下合成CH3OH,其反应为:CO(g)+2H2(g)![]() CH3OH(g)。按n(CO):n(H2)=1:2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。
CH3OH(g)。按n(CO):n(H2)=1:2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。

①P1__________P2(填“<”“>”或“=”)
②在C点时,CO转化率为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
(1)五种元素原子半径由大到小的顺序是(写原子序数) > > > > 。
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写结构式)________________。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:
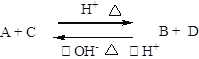 (①②表示转化的先后两个步骤)
(①②表示转化的先后两个步骤)
其中,A、B、C三种物质均由X、Y、Z三种元素组成;B、C是非电解质,误饮用C成分可导致眼睛失明;A的水溶液显酸性,相对分子质量为90,而且该分子中只含一种官能团;B分子量比A大28;D是由X、Z两种元素组成。
写出C的结构简式: ;
写出A+C反应的化学反应方程式: ;
写出转化关系图中序号①的反应类型 ;序号②发生反应的离子反应方程式: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室利用如图装置进行中和热的测定。回答下列问题:

⑴该图中有两处实验用品未画出,它们是 、 ;
⑵在操作正确的前提下提高中和热测定的准确性的关键是: ;
⑶如果用0.5mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热△H”将 (填“偏大”、“偏小”、“不变”)原因是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关组成生物体元素和化合物的叙述,正确的是
A. C是构成细胞的最基本元素,因为碳链是构成生物大分子的骨架
B. 细胞中的微量元素因含量极少而不如大量元素重要
C. 细胞中的脱氧核苷酸和脂肪都不含有氮元素
D. 蔗糖和麦芽糖彻底水解后,得到的产物是相同的
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于研究物质性质的基本程序,排列顺序正确的是
a.观察物质的外观性质 b.实验和观察 c.解释及结论 d.预测物质的性质
A.bacd B.abcd C.adbc D.dabc
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学反应的实验现象结论描述错误的是
A.钠在空气中燃烧发出黄色火焰,生成氧化钠
B.铜粉在氯气中燃烧生成棕黄色的烟
C.铁在氯气中燃烧产生红棕色烟
D.氢气在氯气中燃烧产生苍白色火焰
查看答案和解析>>
科目: 来源: 题型:
【题目】医生常给脱水的病人注射质量分数为0.9%的NaCl溶液,而不用蒸馏水或浓度更高的氯化钠溶液,说明
A. 无机盐离子容易进出细胞
B. 水分子容易进出细胞
C. Na+,Cl—过多或过少都对红细胞有差
D. 无机盐对维持细胞的形态和功能有重要作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com