
科目: 来源: 题型:
【题目】物质的量是高中化学中常用的物理量,请完成以下有关其内容的计算:
(1)标准状况下,含有相同氧原子数的CO与CO2的体积之比为____________。
(2)等温等压下,等体积的O2和O3所含分子个数比为______________,原子个数比为______________,质量比为___________。
(3)设NA为阿伏加德罗常数的数值,如果a g某气中含有的分子数为b,则c g某气在标准状况下的体积约是___________。 (用含NA的式子表示).
(4)配制100mL 1molL-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84gmL-1,质量分数为98%)的体积为__________ mL.
(5)100 mL 某Al2(SO4)3溶液中,n(Al3+)=0.20 mol,则其中c(SO42-)= _________mol/L。
(6)某氯化镁溶液的密度为1.18g/cm3,其中镁离子的质量分数5.6%,300mL该溶液中Cl-的物质的量等于_________ .
查看答案和解析>>
科目: 来源: 题型:
【题目】2SO2(g)+O2(g)===2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。
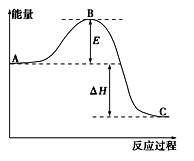
请回答下列问题:
(1)图中A、C分别表示____________、___________;
(2)E表示____________;E的大小对该反应的反应热____________(填“有”或“无”)影响。
(3)该反应通常用V2O5作催化剂,加V2O5会使图ΔH____________(填“变大”、“变小”或“不变”),理由是_____________________。
(4)图中ΔH=________kJ·mol-1;
(5)已知单质硫的燃烧热为296kJ·mol-1,计算由S(s)生成3molSO3(g)的ΔH=________。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n。己知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是( )
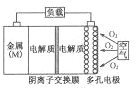
A. 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B. 比较Mg、Al、Zn三种金属-空气电池,Al-空气电池理论比能量最高
C. M-空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne-=4M(OH)n
D. 在M-空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中属于氧化还原反应,但水既不做氧化剂,又不做还原剂的是
A.ICl+H2O=HCl+HIO B.2Na2O2+2H2O=4NaOH+O2
C.2F2+2H2O=4HF+O2D.2K+2H2O=2KOH+H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】下列情况没有发生蛋白质变性的是( )
A.用福尔马林浸动物标本 B.用蘸有质量分数为75%的酒精棉花球擦皮肤
C.用紫外线光灯照射病房 D.淀粉和淀粉酶混合后微热
查看答案和解析>>
科目: 来源: 题型:
【题目】在除杂过程中要尽量除去杂质,那么,加入的试剂必须稍过量,且最后过量物质可以使用物理方法或化学方法除去。现要除 去NaCl中少量的CaCl2、Na2SO4杂质,下列选用试剂及使用顺序正确的是( )
A. Na2CO3、BaCl2、HCl B. BaCl2、Na2CO3、H2SO4
C. BaCl2、Na2CO3、HCl D. Ba(NO3 )2、Na2CO3、HCl
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机物的叙述不正确的是
A.C4H8O2的酯有4种结构
B.淀粉和纤维素互为同分异构体
C.乙醇和葡萄糖均能发生酯化反应
D.漂粉精和医用酒精均可用作消毒剂
查看答案和解析>>
科目: 来源: 题型:
【题目】标况下,H2O的质量为xg,含有y个氢原子,则阿伏加德罗常数为( )
A. 18y/x B. 9y/x C. 18y/ x mol-1 D. 9y/x mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com