
科目: 来源: 题型:
【题目】下列有关实验操作说法正确的是
A. 用分液漏斗范例汽油和植物油
B. 向试管中滴加液体时,胶头滴管紧贴试管内壁
C. 加热试管内物质时,试管底部与酒精灯灯芯接触
D. 过滤时,漏斗下端紧贴烧杯内壁
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2===4CuSO4+2H2O,该反应的还原剂是________________。当1 mol O2发生反应时,还原剂所失电子的物质的量为_________mol。
(2)焙烧明矾的化学方程式为4KAl(SO4)2·12H2O+3S===2K2SO4+2Al2O3+9SO2+48H2O,在该反应中,还原剂是_____________。
(3)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:________________________。
(4)实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
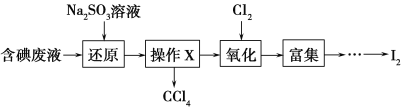
向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_________________;该操作将I2还原为I-的目的是________________________。
(5)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。在图示的转化中,化合价不变的元素是________________。

(6)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为________________,反应消耗1 mol NaBH4时转移的电子数目为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)250 mL密度为1.1 g·cm-3、质量分数为24.5%的硫酸跟铁屑充分反应。计算生成H2的体积(标准状况)(给出必要的计算过程)
(2)上述反应中转移电子数目为多少?
(3)亚硝酸钠(NaNO2)具有致癌作用,许多腌制食品中含NaNO2。酸性KMnO4溶液与亚硝酸钠反应的离子反应为 MnO4-+NO2-+H+→Mn2+ + NO3-+H2O(未配平),下列叙述错误的( )
A.生成1mol Mn2+,转移电子为5mol
B.该反应中氮元素被氧化
C.配平后,水的化学计量数为3
D.反应中氧化产物与还原产物的物质的量之比为2:5
(4)向NaOH溶液中逐渐滴入Mg(HCO3)2溶液至沉淀完全的离子方程______________
(5)现有铜片、锌片、导线、小灯泡![]() 、电流表
、电流表![]() 、硫酸铜溶液及烧杯
、硫酸铜溶液及烧杯![]() ,设计实验证明氧化还原反应中有电子转移。要求画图表示及必要的文字说明。
,设计实验证明氧化还原反应中有电子转移。要求画图表示及必要的文字说明。
查看答案和解析>>
科目: 来源: 题型:
【题目】色氨酸是植物体内生长素生物合成重要的前体物质,普遍存在于高等植物中。纯净的色氨酸为白色或微黄色结晶,微溶于水易溶于盐酸或氢氧化钠,其结构如图所示,下列关于色氨酸的说法不正确的是
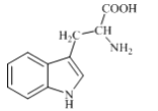
A.色氨酸的分子式为C11H12N2O2
B.色氨酸能发生取代、加成、酯化、中和反应
C.色氨酸微溶于水而易溶于酸或碱溶液是因为其与酸、碱都能反应生成盐
D.将色氨酸与甘氨酸(NH2CH2COOH)混合,在一定条件下最多可形成三种二肽
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式正确的是
A. 钠与水反应:Na+2H2O=Na++2OH一+H2↑
B. 碳酸氢钠与盐酸反应:CO32—+2H+=H2O+CO2↑
C. 铁与稀硫酸反应:Fe+2H+=Fe3++H2↑
D. 醋酸溶液与氢氧化钠溶液反应:CH3COOH+OH一=CH3COO一+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】X2+和Y﹣与氩的电子层结构相同,下列判断中正确的是( )
A.原子半径X<Y
B.离子半径 X2+<Y﹣
C.X与Y的原子序数之差为8
D.在元素周期表中,两者处于同一周期
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com