
科目: 来源: 题型:
 德国重离子研究中心于2010年2月19日宣布,以国际纯粹与应用化学联合会确认,由该中心合成的第112号化学元素从即日起获正式名称“Copernicium”,相应的元素符号为“Cn”.选择2月19日为新元素正式冠名日,也是因为这一天是哥白尼的生日,有报道称Cn原子含有165个中子.下列有关112号元素的相关说法正确的是
德国重离子研究中心于2010年2月19日宣布,以国际纯粹与应用化学联合会确认,由该中心合成的第112号化学元素从即日起获正式名称“Copernicium”,相应的元素符号为“Cn”.选择2月19日为新元素正式冠名日,也是因为这一天是哥白尼的生日,有报道称Cn原子含有165个中子.下列有关112号元素的相关说法正确的是查看答案和解析>>
科目: 来源: 题型:阅读理解
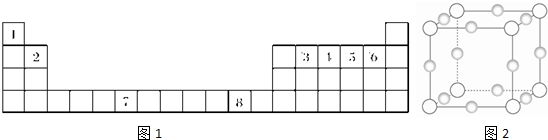
 已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.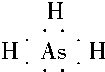
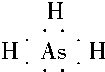
| 3 |
| ||
| 3 |
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:


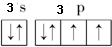

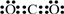
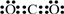

查看答案和解析>>
科目: 来源: 题型:
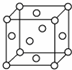
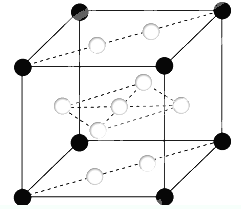
 高温下,超氧化钾(KO2)晶体结构与NaCl相似,其晶体结构的一个基本重复单元如图所示,已知晶体中氧的化合价可看作部分为0价,部分为-2价.则下列说法正确的是( )
高温下,超氧化钾(KO2)晶体结构与NaCl相似,其晶体结构的一个基本重复单元如图所示,已知晶体中氧的化合价可看作部分为0价,部分为-2价.则下列说法正确的是( )查看答案和解析>>
科目: 来源: 题型:
| SO | 2- 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com