
科目: 来源: 题型:
【题目】工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g) ΔH=Q kJ/mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是( )
Si(s)+4HCl(g) ΔH=Q kJ/mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol, 则达平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L·min)
D.反应吸收热量0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应
查看答案和解析>>
科目: 来源: 题型:
【题目】为了更好的解决能源问题,人们一方面研究如何提高燃料的燃烧效率,另一方面寻我新能源。以下做法不能提高燃料效率的是( )
A. 煤的汽化与液化 B. 液体燃料呈雾状喷出
C. 通人大大过量的空气 D. 将煤粉碎后燃烧
查看答案和解析>>
科目: 来源: 题型:
【题目】
①容量瓶 ②蒸馏烧瓶 ③量筒 ④烧杯 ⑤分液漏斗 ⑥托盘天平
(1)加热时必须垫石棉网的有:_______________,
(2)使用时必须检查是否漏水的有:________________,
(3)标有温度的有:_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸厂的烧渣主要成分是Fe2O3,其次含少量的SiO2和FeS。工业上利用硫酸厂烧渣经回收处理制得绿矾(FeSO4·7H2O)和一种聚铁胶体[Fe(OH)SO4]n。绿矾是治疗缺铁性贫血药品的重要成分,而聚铁胶体是重要的水处理剂。上述生产工艺流程如下:
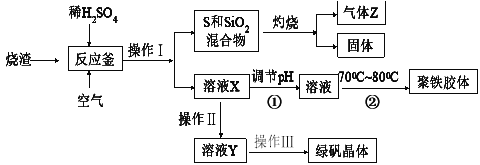
请通过分析回答下列相关问题:
(1)灼烧产生的尾气对大气有污染,因此工业生产中必须进行回收处理,下列方法可行的是_______________:
A.用氨水吸收 B. 直接用水吸收
C. 用浓硫酸吸收 D. 与空气混合用石灰石粉末悬浊液吸收
(2)操作Ⅲ是_____________、_______________、过滤、洗涤、干燥保存等;
(3)在由溶液X制聚铁胶体过程中①调节pH及②控制温度目的是___________________。
(4)在反应釜中FeS、O2及稀H2SO4反应硫酸铁等物质,则反应的离子方程式为___________________________;
(5)某研究性小组为探究绿矾(相对分子质量:278)在隔绝空气条件下加热分解反应的产物(已知分解产物全为氧化物),进行了如图所示的实验:
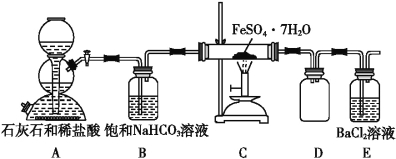
① 实验开始时,在点燃C处酒精喷灯之前应先打开活塞通CO2,其目的是_____________。 装置D的作用是______________________。
②该组同学设计的装置存在着一个明显的缺陷是____________________________。
③该组同学称取55.6 g绿矾按上图装置进行实验。待绿矾分解完全后,E瓶中产生了23.3 g白色沉淀。将C中固体产物投入足量稀硫酸中完全溶解得到溶液,取少量该溶液滴入KSCN溶液呈红色;另取少量该溶液滴入酸性KMnO4溶液,KMnO4溶液不褪色。据写出绿矾分解的化学方程式为__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如下图所示(夹持仪器已略去)。
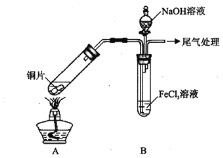
(1)实验前,应先检查装置的 ;实验中产生的尾气应通入 溶液。
(2)实验过程中需要配制100mL1mol/L FeCl3溶液,所需要的玻璃仪器有:烧杯、量筒、玻璃棒、 。
(3)该小组同学向5mL lmol/L FeCl3溶液中通入足量的SO2,溶液最终呈浅绿色,再打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管B中产生的实验现象是 。
(4)该小组同学在(3)中实验时,发现溶液变为浅绿色需要较长时间,在此期间同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象,最终溶液呈浅绿色。
【查阅资料】Fe(HSO3)2+离子在溶液中呈红棕色且具有较强的还原性,能被Fe3+氧化为SO![]() 。SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子的原因是 ;Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是 。
。SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子的原因是 ;Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是 。
(5)若实验中用5 mL一定浓度的浓H2SO4与适量Cu片充分反应,实验结束后,测得产生SO2的体积在标准状况下为672 mL,向已冷却的A试管溶液中加入4 mo1·L-1的NaOH溶液30 mL时,恰好使Cu2+完全沉淀。则所用浓H2SO4浓度为________________。(忽略过程中溶液的体积变化)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:t℃下的某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为:![]() ,有关该平衡的说法中正确的是( )
,有关该平衡的说法中正确的是( )
A.升高温度,平衡常数K变大
B.增大压强,W(g)物质的量分数变大
C.升温,若混合气体的平均相对分子质量变小,则正反应放热
D.增大X浓度,平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】现有250C 101KPa条件下的氯化氢(HCl)气体49L(注:250C 101KPa条件下气体摩尔体积为24.5L/mol)则:
①该气体所含原子总数为____________。
②该气体的质量为____________g。
③该气体溶于127mL水中,得到密度为1.20g/mL的盐酸,此盐酸的物质的量浓度为______________。
④取出20.0 mL该溶液,配成浓度为2.00 mol/L的稀溶液,则稀释后溶液的体积是________ ml
查看答案和解析>>
科目: 来源: 题型:
【题目】国外宇航员吃着“牙膏和砖块”时,中国宇航员已经在太空泡茶了,每个茶装在特制包装袋中,注水后用加热器进行加热就可以喝了,但要插上吸管以防止水珠飘起来。下列说法正确的是( )
物质 | 氧化镁 | 氯化镁 |
熔点/℃ | 2 852 | 714 |
A. 宇航员喝茶时注入的H2O的摩尔质量是18克
B. H2O+Cl2![]() HCl+HClO这反应属于氧化还原反应
HCl+HClO这反应属于氧化还原反应
C. 氢的三种同位素1H、2D、3T与16O只能形成三种水分子
D. 在标准状况下,1mol水的体积约是22.4L
查看答案和解析>>
科目: 来源: 题型:
【题目】将等物质的量的A、B、C、D四种物质混合,发生如下反应:aA+bB![]() cC(s)+dD,当反应进行一段时间后,测得A减少了n mol,B减少了
cC(s)+dD,当反应进行一段时间后,测得A减少了n mol,B减少了![]() mol,C增加了
mol,C增加了![]() n mol,D增加了n mol。此时达到化学平衡状态。
n mol,D增加了n mol。此时达到化学平衡状态。
(1)该化学方程式中各物质的化学计量数:
a=________,b=________,c=________,d=________。
(2)若只改变压强,反应速率发生变化,但平衡不发生移动,该反应中各物质的聚集状态:A________,B____________,D___________。
(3)若只升高温度,反应一段时间后,测得四种物质其物质的量又达到相等,则该反应的正反应为________反应(填“放热”或“吸热”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com