
科目: 来源: 题型:
【题目】中科院南京土壤研究所专家通过3年探索土壤中,初步揭开了“长寿之乡”如皋 “寿星”多的秘密:与当地土壤中硒含量息息相关。科研人员发现,当地百岁老人的血液中硒含量比正常人高3倍。硒有抗衰老的作用。这里的“硒”应理解为( )
A. 元素 B. 原子 C. 分子 D. 离子
查看答案和解析>>
科目: 来源: 题型:
【题目】在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
A.Ag+、Na+、Cl﹣、K+
B.Na+、Cu2+、SO42﹣、NO3﹣
C.Mg2+、Na+、SO42﹣、Cl﹣
D.Ba2+、HCO3﹣、NO3﹣、K+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是
A.空气、硫酸铜、H2SO4 B.HCl、Fe(OH)3胶体、纯碱
C.二氧化碳、胆矾、氢氧化钾 D.HNO3、食盐水、烧碱
查看答案和解析>>
科目: 来源: 题型:
【题目】下列分散系最不稳定的是
A.向NaOH溶液中通入CO2得到的无色溶液
B.向碘的水溶液中滴加四氯化碳充分振荡后,静置后的下层液体
C.向沸水中滴入饱和的FeCl3溶液得到的红褐色液体
D.向稀硫酸中加入BaCl2溶液得到的分散系
查看答案和解析>>
科目: 来源: 题型:
【题目】将0.01 molNaOH和0.01 molNa2CO3混合并配成溶液,向溶液中滴加0.1mol/L稀盐酸。下列图象能正确表示加人盐酸的体积和生成CO2的物质的量的关系的是( )
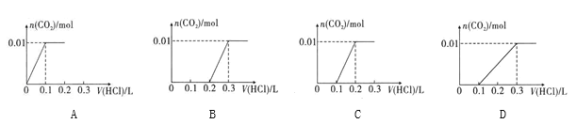
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。采用的实验方案如下:
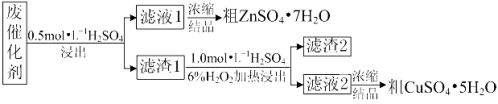
已知:① ZnS与稀硫酸反应时,化合价不变;
② CuS既不溶解于稀硫酸,也不与稀硫酸反应。
回答下列问题:
(1)在下列装置中,第一次浸出必须用________________,第二次浸出应选用______________。(填标号)。第二次浸出时,加热温度不宜过高的原因是 。

(2)滤液1中含有Fe2+,请根据提供的试剂进行检验,则检验方法为: 。
(提供的试剂:稀盐酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水)
(3)将滤液1、滤液2蒸发浓缩至 时,停止加热,然后冷却结晶得到相应的粗产品。
(4)若滤渣2中含有淡黄色固体,写出第二次浸出的化学反应方程式: 。
(5)某同学在实验完成之后,得到1.50 g CuSO4·5H2O,则铜的回收率为___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定量的Na2O2、Na2O、Na的混合物与足量的水反应,在标准状况下得到VL混合气体。将该混合气体通过电火花引燃,恰好完全反应,则原混合物中的Na2O2、Na2O、Na物质的量之比可能为( )
A.2:2:1 B.1:1:1 C.2 :l :2 D.l :l :2
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化镁、氧化铝的熔点高,常作耐高温材料。以MgC12和AlCl3的混合液为主要原料,设计实验制备氧化镁、氧化铝。实验步骤如下:
Ⅰ.取混合液于烧杯中,加入过量的氢氧化钠溶液,充分搅拌,静置;
Ⅱ.过滤得到沉淀和滤液;洗涤、灼烧,得到固体X;
Ⅲ.在步骤Ⅱ所得滤液中加人足量盐酸,再滴加过量的浓氨水;
Ⅳ.过滤、洗涤、灼烧,得到固体Y 。
(1)固体X的名称是_______。
(2)写出步骤Ⅰ中的离子反应方程式:________;________。
(3)步骤Ⅱ过滤中使用的三种玻璃仪器分别为烧杯、漏斗、______。
(4)步骤Ⅲ中,能否使用氢氧化钠溶液替代浓氨水_____(填“能”或“否”)。
(5)写出步骤Ⅳ中“灼烧”发生的化学反应方程式:___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知甲为恒压容器、乙为恒容容器。相同条件下充入等物质的量NO2气体,且起始时体积相同。发生反应:2NO2(g)![]() N2O4(g) △H<0。一段时间后均达到平衡状态。下列说法中正确的是
N2O4(g) △H<0。一段时间后均达到平衡状态。下列说法中正确的是
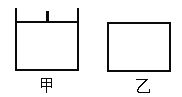
A. 平衡时NO2体积分数:甲<乙
B. 达到平衡所需时间,甲与乙相等
C. 该反应的平衡常数表达式K=c(N2O4)/c(NO2)
D. 若两容器内气体的压强保持不变,均说明反应已达到平衡状态
查看答案和解析>>
科目: 来源: 题型:
【题目】将0.1 mol的镁、铝混合物溶于100 mL2 mol/L的H2SO4溶液中,然后再滴加1 mol/LNaOH溶液。请回答:
(1)若在滴加NaOH溶液的过程中,沉淀质量m 随加入NaOH溶液的体积V变化如图所示。当V1=160 mL 时,则金属粉末中n(Mg) = __________mol ,V2=_________mL 。
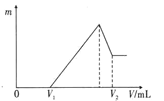
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V (NaOH) = __________mL 。
(3)若混合物仍为0.1mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加人450 mL 1 mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com