
科目: 来源: 题型:
【题目】工业上从铝土矿(主要成分是Al2O3,还含有SiO2、Fe2O3等杂质)中提取铝可选用如下工艺流程:

已知:SiO2不溶于水且不与盐酸反应。
请回答下列问题:
(1)图中涉及分离溶液与沉淀的实验方法是______(填操作名称)。
(2)步骤(Ⅱ)中加入的烧碱溶液应该是______(填“少量”或“过量”)。沉淀B的成分是______(填化学式,下同);溶液D中含铝元素的溶质的是______。
(3)①物质M在生产生活中有重要用途,写出沉淀F转化为物质M的化学方程式:______;
②溶液D中通入______CO2生成沉淀F的离子方程式为:______.
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)机智如化学老师的你用固体烧碱配制500mL 0.20 mol L-1的NaOH溶液,需要称取____g固体,定容时除了胶头滴管和玻璃棒,还需要的仪器为______。
(2)语文老师要用36.5% (ρ=1.18g cm-3)的浓盐酸配制0.4 mol L-1的盐酸240 mL,需准确量取36.5%的浓盐酸____mL。
(3)若配制0.5mol L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,下列所配制的硫酸溶液浓度偏低的是_______(填序号)。
A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒。
B.移液时容量瓶中有少量蒸馏水。
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切。
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切。
E.稀释后没冷却到室温就将溶液转移至容量瓶。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.20mL0.1mol/LBaCl2溶液中Cl-的物质的量浓度为________,Ba2+的物质的量为_______。
II.把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6 LH2(标准状况下)。
(1)合金中镁的物质的量_________。
(2)写出该合金溶于足量NaOH溶液的化学方程式_________。同时产生H2的体积(标准状况下)为____________ 。
III.在一定质量的AlCl3和MgCl2混合溶液中逐渐滴入一定溶质质量分数的NaOH溶液,生成沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则:
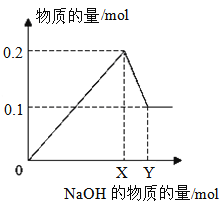
①生成Mg(OH)2的质量为__________;
②X=_______;Y=_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示:
![]()
I.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是______nm。
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:___________。检验反应后溶液中还存在Fe3+的试剂是__________。
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是______,生成1molNa2FeO4转移电子数目为__________。
II.现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是______,加铁粉后溶液增重的是______;
(2)向Fe2+的溶液中滴加NaOH溶液,现象是___________________。
(3)欲除去FeCl2中FeCl3选用合适的试剂和分离方法,并写出相应离子方程式:__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】元素铬及其化合物工业用途广泛,但含+6价铬的污水会损害环境。电镀厂产生的镀铜废水中往往含有一定量的Cr2O72-,处理该废水常用直接沉淀法、还原沉淀法、电解法。
I.直接沉淀法
(1)已知含铬废水中存在着平衡:![]() 。在实际工业生产中,加入沉淀剂BaCl2溶液之前还要加入一定量的NaOH,这样有利于沉淀的生成,则生成沉淀的化学式为
。在实际工业生产中,加入沉淀剂BaCl2溶液之前还要加入一定量的NaOH,这样有利于沉淀的生成,则生成沉淀的化学式为
Ⅱ.还原沉淀法
![]()
(2)下列溶液中可以代替上述流程中Na2S2O3溶液的是 (填选项序号)
A.FeSO4溶液 B.浓H2SO4溶液
C.酸性KMnO4溶液 D.Na2SO3溶液
(3)上述流程中,每消耗0.1molNa2S2O3转移0.8mole-,则加入Na2S2O3溶液时发送反应的离子方程式为
(4)Cr(OH)3的化学性质与Al(OH)3相似。在上述生产过程中加入NaOH溶液时要控制溶液的pH不能过高,原因可用离子方程式表示:
(5)实际工业生产中有时还采用阳离子交换树脂法来测定沉淀后溶液中Cr3+的含量,其原理是Mn++nNaR=nNa++MRn,其中NaR为阳离子交换树脂,Mn+为要测定的离子。
常温下,某次测定过程中,将pH=5的废水经过阳离子交换树脂后,测的溶液中Na+比交换前增加了4.6×10-2g/L,则该条件下Cr(OH)3的Ksp的值为 ,当Cr3+浓度小于10-5mol/L时可认为沉淀完全,处理后测得溶液的PH=6,则溶液过滤后 (填“能”或“否”)直接排放
Ⅲ.电解法
(6)该法是用铁作电极点解含Cr2O72-的酸性废水,电解时阴极上有大量气泡生成,并产生Cr(OH)3、Fe(OH)3沉淀,反应中1mol Cr2O72-完全生成Cr(OH)3沉淀,外电路通过的电子的物质的量为 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】埋在地下的输油铸铁管道,在下列各种情况下被腐蚀速度最慢的是( )
A. 在含铁元素较多的酸性土壤中
B. 在潮湿疏松透气的土壤中
C. 在干燥致密不透气的土壤中
D. 在含碳粒较多、潮湿透气的土壤中
查看答案和解析>>
科目: 来源: 题型:
【题目】填空:
(1)0. 5 mol NH3分子中所含氮原子数为__________个;
(2)1.2g RSO4中含0.01 mol R2+,则RSO4的摩尔质量是__________;
(3)0.1 mol·L-1的 Cu(NO3)2溶液中NO3-的物质的量浓度是__________;
(4)新制氯水在阳光照射下产生的无色气体是__________;
(5)配制100 mL 1 mol/L NaCl溶液,定容后,把容量瓶倒置摇匀后发现液面低于刻度线,补加水至刻度处,会引起所配溶液物质的量浓度__________(选填“偏高、偏低、无影响”);
(6)实验室制备氯气时,收集氯气常采用__________法。
查看答案和解析>>
科目: 来源: 题型:
【题目】右下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍。下列说法正确的是( )
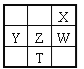
A. X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增
B. Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增
C. 根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性
D. YX2晶体熔化、液态WX3气化均需克服分子间作用力
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
①31g白磷含有的P-P键数为N A
②1molCH3+(碳正离子)中含有电子数为10NA
③1mol铜与足量硫蒸气反应,转移电子数为2NA
④1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2N A 个电子
⑤用惰性电极电解CuCl2溶液,阴极析出16g铜时,线路中通过电子数为N A
⑥0.84gNaHCO3晶体中阳离子和阴离子总数为0.03N A
⑦3.9gNa2O2吸收足量的CO2时转移的电子数是0.05 N A
⑧标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1N A
⑨28g C16O与28g C18O中含有的质子数均为14×6.02×1023
⑩标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2×6.02×1023
A.②④⑦⑧ B.③④⑥⑦⑧ C.④⑦ D.④⑥⑨⑩
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com