
科目: 来源: 题型:
【题目】在下列物质转化中,A是一种酸式盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如下的转化关系:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。请回答:
(1)A是________, Z是________。
(2)当X是强酸时,写出B生成C的化学方程式:___________________。
(3)当X是强碱时,E是________,写出E和铜反应生成C的化学方程式:__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g)![]() CO2(g)十H2 (g)十Q(Q>0),CO和H2O浓度变化如下图:
CO2(g)十H2 (g)十Q(Q>0),CO和H2O浓度变化如下图:
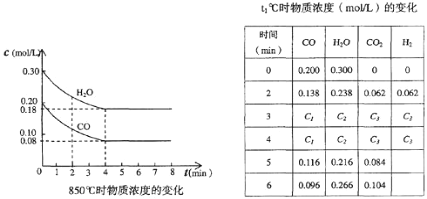
(1)则0~4 min的平均反应速率v(CO)=________mol/(L·min),该反应在850℃的平衡常数K=________
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3 min~4 min之间反应处于_________状态;C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4 min~5 min间,平衡向逆方向移动,可能的原因是_________(单选),表中5 min~6 min之间数值发生变化,可能的原因是_________(单选)。
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:C(s,金刚石)=C(s,石墨) △H=-1.9KJ/mol
C(s,金刚石)+O2(g)=CO2(g) △H1
C(s,石墨)+O2(g)=CO2(g) △H2
根据已述反应所得出的结论正确的是( )
A.△H1=△H2 B.△H1>△H2
C.△H1<△H2 D.金刚石比石墨稳定
查看答案和解析>>
科目: 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且有些可以再生。下列属最有希望的新能源的是( )
①天然气②煤③核能④水电⑤太阳能⑥燃料电池⑦风能⑧氢能
A.⑤⑥⑦⑧ B.①②③④ C.③④⑤⑥ D.除①②外
查看答案和解析>>
科目: 来源: 题型:
【题目】将11.5g金属钠投入到足量水中,得到溶液a,将12g镁投入到与水等质量的足量的稀硫酸中,得到溶液b,则a和b的质量关系为
A.a=b
B.a>b
C.a<b
D.无法确定
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)从氧化还原的角度分析水在下列化学反应中只做还原剂的是_______________
A电解水 B钠和水的反应(2Na+2H2O===2NaOH+H2↑)
C氟气和水反应(2F2+2H2O===4HF+O2) D氯气和水反应(Cl2+H2O===HCl+HClO):
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应物中还原产物是________;若反应方程式中转移了0.4 mol电子,则氧化产物的质量是_____ g。
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为:2Fe2++Cl2===2Fe3++2Cl-,这个事实说明Fe2+、Cl-、Br—三种粒子还原性由强到弱的排列顺序为:__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温下,将Xmol N2 和Ymol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3N2(g)![]() 2NH3(g)
2NH3(g)
⑴若反应进行到t时刻,n(N2)=10mol,n(NH3)=4mol,计算X的值。
⑵反应达到平衡时,混合气体的体积为672L(标准状况下),其中NH3的体积分数为20%,计算N2的转化率和Y的值。
查看答案和解析>>
科目: 来源: 题型:
【题目】从下列事实,找出不能用勒沙特列原理解释的是( )
A.溴水中存在如下平衡![]() ,当加入NaOH溶液后颜色变浅
,当加入NaOH溶液后颜色变浅
B.对![]()
![]()
![]() 平衡体系增加压强使颜色变深
平衡体系增加压强使颜色变深
C.反应![]()
![]()
![]() 升高温度使平衡向逆方向移动
升高温度使平衡向逆方向移动
D.合成氨反应:![]()
![]()
![]() ,为使氨的产率提高,理论上应采取低温高压的措施
,为使氨的产率提高,理论上应采取低温高压的措施
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应mX(g)+nY(g)![]() qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为n/m
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com