
科目: 来源: 题型:
【题目】将小块生石灰投入盛有水的试管中,发生剧烈反应。一段时间后,用手触摸试管外壁感觉烫手,这个实验事实说明该反应
A. 是放热反应 B. 是吸热反应
C. 反应过程中热能转化为化学能 D. 反应物的总能量等于生成物的总能量
查看答案和解析>>
科目: 来源: 题型:
【题目】古代的很多成语、谚语都蕴含着很多科学知识,下列对成语、谚语的解释正确的是
A. “爆竹声中除旧岁,春风送暖入屠苏’’.爆竹爆将炸发生的是分解反应
B. “甘之如饴’’说明糖类均有甜味
C. “玉不琢不成器”,“百炼方能成钢”发生的均为化学变化
D. “火树银花’’中的焰火实质上是金属元素的焰色反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关1molNaOH的说法中,正确的是
A. NaOH的摩尔质量为40g
B. 1mol NaOH 的质量为40g/mol
C. 标准状况下,1molNaOH 所占的体积为22.4L
D. 将1molNaOH溶于水配成100mL溶液,则溶液中溶质的物质的量浓度为10mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
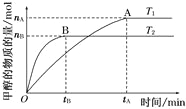
下列说法正确的是 (填序号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(2) 用乙醇燃料电池做电源进行工作,KOH溶液做电解质,写出负极的电极反应式为:____________。电池工作一段时间后溶液PH值___________(变大,变小或不变)
(3) 若在常温常压下,1克乙醇完全燃烧生成二氧化碳和液态水放热约为30KJ的热量,写出乙醇燃烧热的热化学方程式________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是
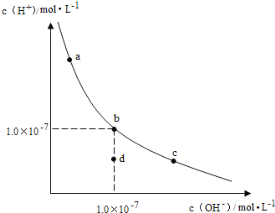
A升高温度,可能引起由c向b的变化
B该温度下,水的离子积常数为1.0×10-13
C该温度下,加入FeCl3可能引起由b向a的变化
D该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目: 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
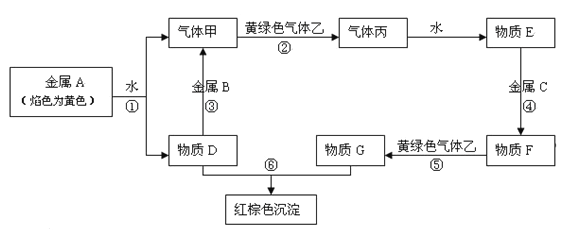
请根据以上信息回答下列问题:
(1)写出金属元素A的原子结构示意图:_______________。
(2)写出下列反应的离子方程式:
反应③___________;反应⑤____________________
(3)检验物质G中阳离子的操作方法_____________________。
(4)实验室制取黄绿色气体乙的化学方程式为__________________,在该反应中如有0.5 mol乙生成,转移的电子的物质的量是_____mol。制取完毕,多余的乙将用D的水溶液来吸收,其离子方程式为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢为原料制取氧气,当制得同温同压下相同体积的氧气时,三个反应中转移的电子数之比为( )
A.1:1:2 B.2:2:1 C.2:3:1 D.4:3:2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列热化学方程式或离子方程式中,正确的是:
A. 甲烷的标准燃烧热为890.3kJ.mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ.mol-1
B. CO(g)的燃烧热是283.0 kJ/mol ,则CO2(g)=2CO(g)+O2(g)的反应热△H=+2×283.0 kJ/mol
C. NaOH和HCl反应的中和热 △H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol
D. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ/mol
2NH3(g) △H=-38.6kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】研究大气中含硫化合物和含碳化合物的转化对环境保护具有重要意义。
(1)SO2的大量排放会引起严重的环境问题是 ,潮湿条件下,写出大气中SO2转化为HSO3-的方程式 ;
(2)土壤中的微生物可将大气中H2S经两步反应氧化成SO42-,两步反应的能量变化示意图如下:
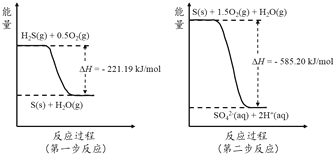
1mol H2S(g)全部氧化成SO42-(aq)的热化学方程式为 ;
(3)SO2是工业制硫酸的原料之一,一定温度下,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g),过程中测定的部分数据见下表:
2SO3(g),过程中测定的部分数据见下表:
时间/min | n(SO2)/mol | n(O2)/mol |
0 | 0.10 | 0.05 |
4 | 0.04 | 0.02 |
6 | 0.02 | |
8 | 0.01 |
①反应在0-4min内的平均速率为v(SO2)= ;
②此温度下该反应的化学平衡常数K= ;
③8min时,维持温度不变,向反应容器中再通入0.02mol SO2(g)和0.01mol O2(g),重新达到平衡时混合气体中SO2的百分含量将 (填“减小”、“增大”或“不变”)。
(4)科学家用氮化镓材料与铜组装如下图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4的反应。
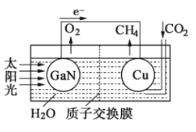
写出铜电极表面的电极反应式 ,为提高该人工光合系统的工作效率,可向装置中加入少量 (填“盐酸”或“硫酸”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com