
科目: 来源: 题型:
【题目】下列反应能用H++OH-=H2O表示的是
A.氢氧化镁和稀盐酸 B.Ba(OH)2 溶液滴入稀硫酸中
C.澄清的石灰水和稀硝酸反应 D.二氧化碳通入澄清石灰水
查看答案和解析>>
科目: 来源: 题型:
【题目】计算下列微粒中划“___”原子的孤电子对数。
(1)H2S________,
(2)PCl5_______,
(3)BF3___________,
(4)NH3__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚铁是一种重要的化工产品,在工业上有重要的用途。某校化学兴趣小组,利用工业烧渣为原料,设计如下制备硫酸亚铁的方案。学生探究烧渣(主要成分为铁的氧化物及少量FeS、SiO2 等)制备绿矾(FeSO4·7H2O)。工艺流程如下所示:
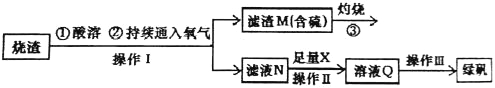
(1)烧渣在进行酸溶时用到了稀硫酸。他们在配制所需的稀硫酸时使用了自来水,有同学提出自来水中含有少量的Cl-,会影响到制出的FeSO4 的纯度。请你设计实验证明已配制的稀硫酸中混有Cl-。
_______________________。
(2)过程③灼烧时产生的气体通入下列溶液中,溶液不会褪色的是___________
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.红色的酚酞试液
(3)X 是 , 此时滤液N 中发生反应的离子方程式为 。检验溶液Q 中含有的金属阳离子的实验方法是 。
(4)操作III 的操作步骤为蒸发浓缩、 、过滤( 填操作名称)、 、干燥。
(5)硫酸亚铁可以用于治疗缺铁性贫血症,某严重贫血患者共需补充2.8g铁元素,服用的药品中相当于需要绿矾的质量为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn), 发生反应:Sn(s)+Pb2+(aq) ![]() Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是
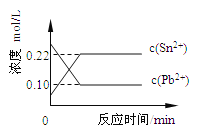
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0
D.25℃时,该反应的平衡常数K=2.2
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,0.2 mol·L-1的一元酸HCl与等浓度的MOH溶液等体积混合后,所得溶液中部分微粒组成及浓度如图所示,下列说法正确的是( )
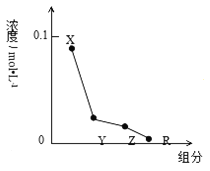
A.MOH的电离方程式:MOH=M++OH-
B.该混合溶液中水电离出的c(H+)<10-7mol·L-1
C.该混合溶液中:c(Y)+c(X)=c(R)+c(Z)
D.图中c(X)+c(Z)=0.1mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应 CO2(g)+C(s)![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如下图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如下图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
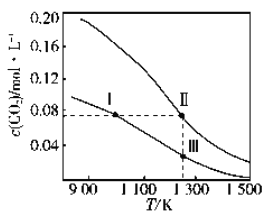
A. 反应 CO2(g)+C(s)![]() 2CO(g)的 ΔS>0、 ΔH<0
2CO(g)的 ΔS>0、 ΔH<0
B. 体系的总压强p总:p总(状态Ⅱ) <2p总(状态Ⅰ)
C. 体系中 c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D. 逆反应速率v逆: v逆(状态Ⅰ)>v逆(状态Ⅲ)
查看答案和解析>>
科目: 来源: 题型:
【题目】碲锌镉(Te-Zn-Cd)晶体可以用于制造红外探测器的基础材料,下列有关它的叙述中不正确的是( )
A.它是由Te、Zn、Cd按一定比例混合而成的,无固定的熔沸点
B.它易导电、导热,具有延展性
C.它的熔沸点比Zn的低
D.它的硬度和强度比Cd的大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 第三周期所含的元素中钠的第一电离能最小
B. 铝的第一电离能比镁的第一电离能大
C. 在所有元素中,氟的第一电离能最大
D. 钾的第一电离能比镁的第一电离能大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列判断哪些是正确的
①氢氧化钠是电解质
②强电解质溶液的导电性一定比弱电解质溶液导电性强
③氯化银难溶于水,所以氯化银是非电解质
④蔗糖易溶于水,所以是电解质
⑤氯气溶于水后导电,所以Cl2是电解质
A.① B.①③ C.①②⑤ D.①②③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com