
科目: 来源: 题型:
【题目】二氧化硫的含量是空气质量监测的一个重要指标。
I.二氧化硫被雨水吸收后就形成了酸雨,某兴趣小组同学汲取热电厂附近的雨水进行实验。
① 测得该雨水样品的pH为4.73;
② 每隔1 h,通过pH计测定雨水样品的pH,测得的结果如下表:

根据以上信息,回答下列问题:
(1)正常雨水的pH为5.6,偏酸性,这是因为___________________。
(2)分析上述数据变化,你认为形成这一变化的原因是__________________。
II.兴趣小组同学为测定空气中二氧化硫的体积分数,做了如下实验:取标准状况下的空气1.000L(内含氮气、氧气、二氧化硫、二氧化碳等),慢慢通过足量氯水,(反应的化学方程式为SO2+Cl2+H2O=2HCl+H2SO4),在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g。
(1)过滤时,除去沉淀中附着的过量氧化钡的方法是_____________。
(2)计算该空气样品中二氧化硫的体积分数(写出计算过程)________
查看答案和解析>>
科目: 来源: 题型:
【题目】太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、锎、硼、镓、硒等。回答下列问題:
⑴二价铜离子的电子排布式为 ,已知高温下Cu2O比CuO更稳定,试从铜原子核外电子结构变化角度解释 。
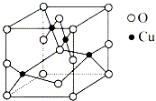
⑵如图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 。
⑶往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是 。
⑷铜与类卤素(SCN)2反应生成Cu(SCN)2,1mol(SCN)2中含有π键的数目为 ,类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H—S—C≡N)的沸点低于异硫氰酸(H—N=C=S)的沸点。其原因是 。
⑸硼元素具有缺电子性,其化合物可与具有孤电子对的分子或离子形成配合物,如BF3能与NH3反应生成BF3NH3,在BF3NH3中B原子的杂化方式为 ,B与N之间形成配位键,氮原子提供 。
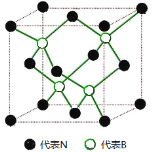
⑹六方氮化硼晶体结构与石墨晶体相似,层间相互作用为 。六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构和硬度都与金刚石相似,晶胞结构如下图所示,晶胞边长为361.5pm,立方氮化硼的密度是 g/cm3。(只要求列算式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】把下列四种物质分别加入到盛有100 mL蒸馏水的烧杯中,不能使蒸馏水导电性发生明显变化的是( )
A.10 g NaCl固体
B.10 g NaOH固体
C.10 g BaSO4固体
D.10 g Cu(NO3)2固体
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A. 用胆矾炼铜、烧结粘土制陶瓷都涉及化学变化
B. 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
C. 食盐、醋酸、氨水和硫酸钡都是电解质
D. 胶体区别其它分散系的本质特征是分散质微粒直径在1nm~100nm之间
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中正确的是( )
A.能电离出氢离子的化合物叫做酸
B.能电离出氢氧根离子的化合物叫做碱
C.能电离出酸根离子的化合物叫做盐
D.由金属离子和酸根离子组成的化合物属于盐
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学试剂的保存方法正确的是
A. 短时间存放FeCl2溶液时,可添加少量铁粉防止Fe2+被氧化
B. Na2CO3溶液存放在带玻璃塞的玻璃试剂瓶中
C. 氢氟酸存放在玻璃试剂瓶中
D. 钠单质存放在四氯化碳中
查看答案和解析>>
科目: 来源: 题型:
【题目】I、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入润洗过的锥形瓶中,并加入1或2滴酚酞溶液
⑤滴入一滴标准液后,溶液颜色由无色变为红色立即停止滴定,记录液面读数
请回答:
(1)以上步骤有错误的是(填编号) 。
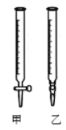
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入_________中。(从图中选填“甲”或“乙”)
(3)下列操作会引起实验结果偏大的是:_________(填编号)
A.酸式滴定管未润洗
B.滴定前,滴定管尖嘴无气泡,滴定后有气泡
C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D.滴定结束时仰视滴定管,并记录数据
E.滴定过程中有一滴标准液飞溅出锥形瓶
(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视 。
II.利用中和滴定的原理,在工业生产中还可以进行氧化还原滴定测定物质含量。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉状TiO2。
用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(5)除去TiCl4含有的杂质A3+可选用调节pH的方法使其转化为A(OH)3沉淀除去。已知Al(OH)3的![]() ,若想将Al3+完全沉淀(不考虑钛离子的沉淀),则溶液的pH一定不能小于__________。(
,若想将Al3+完全沉淀(不考虑钛离子的沉淀),则溶液的pH一定不能小于__________。(![]() 时,即可认为完全沉淀)
时,即可认为完全沉淀)
(6)TiCl4水解生成TiO2·xH2O的化学方程式为__________________________。
(7)滴定终点的现象是___________________________。
(8)滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为____________________。
查看答案和解析>>
科目: 来源: 题型:
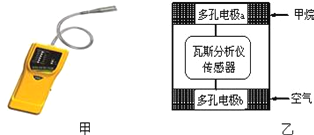
【题目】瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3﹣Na2O,O2﹣可以在其中自由移动.
下列有关叙述正确的是( )
A. 电极a的反应式为:CH4+4O2﹣﹣8e﹣=CO2+2H2O
B. 电极b是正极,O2﹣由电极a流向电极b
C. 瓦斯分析仪工作时,电池内电路中电子由电极 a流向电极b
D. 当固体电解质中有2 mol O2﹣通过时,外电路通过电子8 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列反应的化学方程式。
(1)电解饱和食盐水:____________。
(2)氢氧化钠溶液腐蚀磨砂玻璃塞:____________。
(3)实验室用亚硫酸钠与浓硫酸反应制备二氧化硫:____________。
(4)氢氧化铝溶于氢氧化钠溶液:____________。
(5)氨在催化剂的作用下与氧气发生反应,生成一氧化氮____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com