
科目: 来源: 题型:
【题目】Ⅰ.下列物质中:
①N2、②MgCl2、③NH4Cl、 ④ZnSO4、⑤CO2、⑥HClO4、⑦KOH、⑧H3PO4(填编号)
(1)属于非电解质的是______;属于弱电解质的是_______。
(2)属于共价化合物的是_____;不含有共价键的离子化合物是______。
(3)既含有离子键又含有共价键的是________。
Ⅱ.写出化学方程式或离子方程式:
(1)碳和浓硫酸反应的化学方程式_______。
(2)Na2O2和水反应的离子方程式________。
(3)NH3的催化氧化反应化学方程式_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将0.01 molNH4Cl和0.005mol NaOH溶于水配成1 L 溶液(Ph>7).
(1)该溶液中存在的三个平衡体系是: __ _____、__ ____、_____________。
(2)溶液中存在的离子物质的量浓度由大到小顺序为 。
(3)这些粒子中浓度为0.01 mol/L 的是_________,浓度为0.005 mol/L 的是_________。
(4)物质的量之和为0.01 mol的两种粒子是:_________________________。
(5)NH4+和H+两种离子数量之和比OH-多_______mol。
查看答案和解析>>
科目: 来源: 题型:
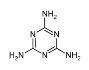
【题目】三聚氰胺俗称“蛋白精”,工业上通过下列流程合成三聚氰胺。请回答下列问题:
(1)基态Ca原子的电子排布式:___________________;CaC2的电子式________________。
(2)尿素分子中所含除氢以外元素第一电离能由小到大的顺序为________________。
(3)CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和________(填化学式),由此可以推知CN22-的空间构型为________。
(4)三聚氰胺分子中碳原子的杂化方式为________,分子中处于同一平面的氮原子有_____个。
(5)动物摄入三聚氰胺和三聚氰酸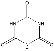 后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
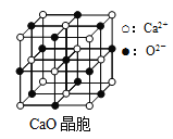
(6)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为______________,已知CaO晶体的密度为ρ,用NA表示阿伏伽德罗常数,求晶胞中距离最近的两个钙离子之间的距离__________(用含ρ、NA代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】固体粉末X中可能含有K2S03、KAlO2、MgC12,Na2C03中的一种或几种.为确定该固体粉末的成分,做如下实验:①溶于水后,无明显现象;②取固体X进行下列实验,实验过程及现象如下:
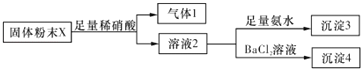
根据上述实验,以下说法正确的是( )
A.气体I可能为SO2和CO2的混合物
B.沉淀3一定为Mg(OH)2和Al(OH)3的混合物
C.固体粉末X中一定有Na2C03,可能有KA102
D.固体粉末X中一定有K2SO3和KA102
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K = 。
(2)该反应为 反应(选填“吸热”、“放热”)。
(3)能说明该反应达到化学平衡状态的是 。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为 ℃。
(5)830℃时,在1L密闭容器中分别投入lmolH2和1molCO2反应达到化学平街时,CO2的转化率为 保持温度不变.在平衡体系中再充入1molH2和1 molCO2重新达到化学平衡时,CO2 的平衡转化率 (填“增大”“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在已达到电离平衡的0.1 mol/L醋酸溶液中,欲使平衡向电离的方向移动,同时使溶液的pH降低,应采取的措施是( )
A.加少量盐酸 B.加热 C.加少量醋酸钠晶体 D.加少量水
查看答案和解析>>
科目: 来源: 题型:
【题目】为验证卤素单质氧化性的相对较弱,某小组用下图装置进行实验(夹持仪器已略去,气密性已检验)。实验过程:
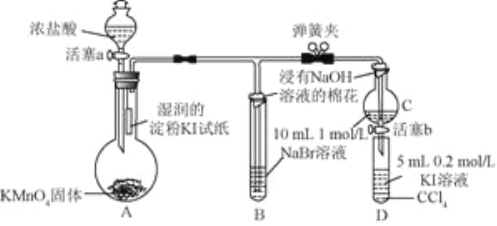
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸,A中产生黄绿色气体。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)D中四氯化碳的电子式是 。
(2)验证氯气的氧化性强于碘的实验现象是 。
(3)B中溶液发生反应的离子方程式是 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 。
(5)过程Ⅲ实验的目的是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组中两种物质在溶液中的反应,可用同一离子方程式表示的是( )
A. Cu(OH)2+HCl;Cu(OH)2+CH3COOH
B. CaCO3+H2SO4;Na2CO3+HCl
C. H2SO4+NaOH;H2SO4+Ba(OH)2
D. BaCl2+H2SO4;Ba(OH)2+Na2SO4
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组只领取下列仪器和用品:铁架台、铁夹、铁圈、三角架、石棉网、烧杯、漏斗、分液漏斗、 酒精灯、玻璃棒、量筒、蒸发皿、锥形瓶、牛角管、火柴。不能进行的实验操作是( )
A. 蒸发 B. 萃取 C. 过滤 D. 蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com