
科目: 来源: 题型:
【题目】将2 mol A与2 mol B混合于2 L的密闭容器中,发生如下反应:2A(g)+3B(g) ![]() 2C(g)+zD(g),若2分钟后达到平衡,A的转化率为50%,测得v(D)=0.25 mol/(L·min),则下列推断正确的是
2C(g)+zD(g),若2分钟后达到平衡,A的转化率为50%,测得v(D)=0.25 mol/(L·min),则下列推断正确的是
A.v(C)=0.2 mol/(L·min)
B.z=3
C.B的转化率为25%
D.C的体积分数约为28.6%
查看答案和解析>>
科目: 来源: 题型:
【题目】化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是 ( )
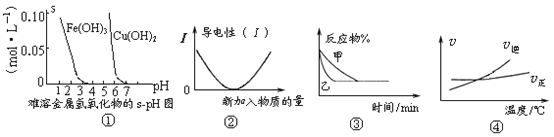
A. 根据图①溶解度与溶液pH关系,若除去CuSO4溶液中的Fe3+可向溶液中加入适量Cu,至pH在4左右。
B. 图②可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
C. 图③表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
D. 根据图④可判断可逆反应A2(g)+3B2(g)![]() 2AB3(g)的化学平衡常数K随温度升高而变小
2AB3(g)的化学平衡常数K随温度升高而变小
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W、R、T均为前四周期元素且原子序数依次增大,X与Y相邻且Y原子的最外层电子数是次外层电子数的3倍,Z是前三周期金属性最强的元素,W的单质常用作太阳能电池材料,R元素的非金属性强于硫,T的合金是现在世界上用量最大的合金。请回答下列问题:
(l) X、W的元素符号分别是_______、________, T在周期表中的位置是__________。
(2) Y的简单氢化物的沸点比同主族相邻元素的氢化物沸点______(填“高”或“低”),原因是________
(3)R元素和硫元素最高价氧化物水化物的酸性强弱是________。(用化学式表示)
(4)分别写出一种由以上元素组成的能用于自来水消毒的单质和化合物的化学式____、______。
(5)写出Y、Z两种元素形成的阴、阳离子数目比为1:2的所有化合物的电子式_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A.离子化合物中可以含有共价键,但共价化合物中一定不含离子键
B.含有共价键的物质一定是共价化合物
C.HCl溶于水只需克服分子间作用力
D.干冰升华时,分子内共价键会发生断裂
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中正确的是()

A. 钠与W可能形成Na2W2化合物
B. 由Z与Y组成的物质在熔融时能导电
C. W得电子能力比Q强
D. X有多种同素异形体,而Y不存在同素异形体
查看答案和解析>>
科目: 来源: 题型:
【题目】以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:下列说法不正确的是( )

A. 在阴极室,发生的电极反应为:2H2O + 2e 2OH -+ H2↑
B. 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+ 浓度增大,使平衡2CrO42- + 2H+ ![]() Cr2O72- + H2O向右移动
Cr2O72- + H2O向右移动
C. 该制备过程中总反应的化学方程式为4K2CrO4 + 4H2O ![]() 2K2Cr2O7 + 4KOH + 2H2↑+ O2↑
2K2Cr2O7 + 4KOH + 2H2↑+ O2↑
D. 测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr) 为d,则此时铬酸钾的转化率为(1-d/2)。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲酸的下列性质中,可以证明它是弱电解质的是
A.甲酸以任意比与水互溶
B.0.1mol/L甲酸溶液的c(H+)=10-3mol/L
C.10mL 1mol/L甲酸恰好与10mL 1mol/L NaOH溶液完全反应
D.甲酸溶液的导电性比一元强酸溶液的弱
查看答案和解析>>
科目: 来源: 题型:
【题目】在10L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,发生反应:SO2(g)+ NO2(g)![]() SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
试求:该温度下、该容器中,再继续加入1mol的SO2(g),则:
(1)化学平衡将向________方向移动,NO2的转化率将____________(填“增大” 、“不变”或“减小”);
(2)经计算,当达到新的平衡状态时,容器中SO2(g)的浓度是___________mol/L;
(3)整个过程中,SO2的转化率由50%变为___________%,NO2的转化率由__________%变为___________%。
(4)计算结果给我们的启示是:增大一种反应物物的用量,其转化率将_______________(填“增大” 、“不变”或“减小”)另一反应物的转化率将____________(填“增大” 、“不变”或“减小”)。现实生产中的意义是:可以通过增大________的用量,来提高成本高的反应物的利用率。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 三种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出对应的元素符号:C________,D_______
(2)用电子式表示A与E两元素形成化合物的过程:___________________________ ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com