
科目: 来源: 题型:
【题目】下列离子组一定能大量共存的是( )
A. 酚酞呈红色的溶液中:Al3+、Cl-、NO3-、Na+
B. 石蕊呈蓝色的溶液中:Na+、[Al(OH)4]-、NO3-、HC![]() O3-
O3-![]()
C. 能与铝反应发出H2的溶液中:K+、Na+、NO3-、ClO-
D. 含大量OH-的溶液中:CO32-、Cl-、F-、K+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是()
A.由于水中存在氢键,所以水很稳定
B.能与酸反应生成盐和水的氧化物一定是碱性氧化物
C.Na2O2中既含有离子键,又含有非极性键
D.由于C=O键是极性键,所以CO2 是极性分子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质鉴别的方法可行的是( )
A. 用KMnO4 酸性溶液检验石蜡中是否有不饱和烃
B. 用石蕊试纸区别苯酚溶液和小苏打溶液
C. 用BaCl2 溶液区别硫酸和盐酸
D. 用Cu(OH)2 的碱性浊液区别甲醛溶液和乙醛溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下列现象与电化学腐蚀无关的是
A. 炒菜的铁锅未及时洗干净(残液中含NaCl)而生锈
B. 海军黄铜(含Zn、Cu和1%的Sn)不易产生铜绿
C. 银质物品久置表面变暗
D. 钢铁在潮湿的露天环境中容易生锈
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学平衡移动叙述中正确的是( )
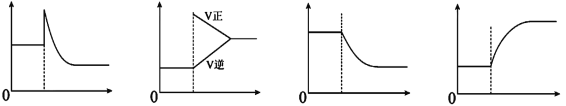
图一 图二 图三 图四
A.可逆反应:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+达平衡状态溶液呈橙黄色,滴加少量的浓硫酸,溶液变橙色,氢离子浓度随时间变化曲线如上图一
2CrO42-(黄色)+2H+达平衡状态溶液呈橙黄色,滴加少量的浓硫酸,溶液变橙色,氢离子浓度随时间变化曲线如上图一
B.可逆反应Co(H2O)62+(粉红色)+4Cl-![]() CoCl42- (蓝色)+6H2O达平衡状态溶液呈紫色,升高温度,溶液变蓝色,反应速率随时间变化曲线如上图二
CoCl42- (蓝色)+6H2O达平衡状态溶液呈紫色,升高温度,溶液变蓝色,反应速率随时间变化曲线如上图二
C.可逆反应:2NO2![]() N2O4达平衡状态呈红棕色,加压红棕色变深,NO2物质的量随时间变化曲线如上图三
N2O4达平衡状态呈红棕色,加压红棕色变深,NO2物质的量随时间变化曲线如上图三
D.可逆反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0达平衡状态,升高温度,NH3体积分数随时间变化曲线如上图四
2NH3(g) △H<0达平衡状态,升高温度,NH3体积分数随时间变化曲线如上图四
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=﹣41kJ/mol,相同温度下,在体积相同的三个密闭容器中,加入一定量的物质发生反应,相关数据如下:
CO2(g)+H2(g)△H=﹣41kJ/mol,相同温度下,在体积相同的三个密闭容器中,加入一定量的物质发生反应,相关数据如下:
容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||||
CO | H2O | CO2 | H2 | Ar[ | ||
① | 1 | 4 | 0 | 0 | 0 | 放出热量:32.8 kJ |
② | 0 | 3 | 1 | 1 | 0 | 热量变化:Q1 |
③ | 0.5 | 3.5 | 0.5 | 0.5 | 1 | 热量变化:Q2 |
下列说法中,不正确的是( )
A.容器①中反应达平衡时,CO的转化率为80%
B.热量数值:Q2 < Q1 =32.8 kJ
C.平衡时,三容器中CO2的浓度相等
D.容器③中反应开始时正反应的浓度商小于该反应平衡常数K
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定量的镁铝合金投入100 mL一定浓度的盐酸中,合金溶解。向所得溶液中滴加5 mol/L NaOH溶液,生成的沉淀质量与加入的NaOH溶液的体积如图所示,由图中数据分析计算,正确的是( )
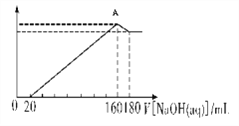
A. 原合金中镁的质量为9.6g
B. 铝的质量为5.4g
C. 盐酸的物质的量浓度为8mol/L
D. 图像中A点沉淀为Al(OH)3
查看答案和解析>>
科目: 来源: 题型:
【题目】根据题意回答问题:
(1)中和热的测定所需的玻璃仪器有:大小烧杯、量筒、温度计、 ;
已知:0.55 mol·L-1 HCl和0.50 mol·L-1的NaOH溶液各50 mL反应放出热量为1.42kJ,写出该反应的中和热的热化学方程式: 。
(2)101kpa时,1克乙醇(CH3CH2OH)液体完全燃烧生成稳定氧化物放出热量akJ,写出乙醇燃烧热的热化学方程式: 。
(3)已知H-H、O=O和O-H键的键能分别为436 kJ/mol、498 kJ/mol和463 kJ/mol,2H2O(g) = 2H2(g)+ O2(g) ΔH2= 。
(4)用CO2和氢气合成CH3OCH3(甲醚)是解决能源危机的研究方向之一。
已知:CO(g)+2H2(g ![]() CH3OH(g) ΔH=-90.7 kJ·mol-1
CH3OH(g) ΔH=-90.7 kJ·mol-1
2CH3OH(g ![]() CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CO(g)+H2O(g ![]() CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
则CO2和氢气合成CH3OCH3(g)的热化学方程式为: 。
(5)① 25℃时,浓度均为0.1 mol/L的①氨水②氢氧化钠溶液③盐酸溶液④醋酸溶液,其c(H+)由大到小排列的顺序为: (用序号填空)。
② 95℃时,水中的H+的物质的量浓度为10-6 mol·L-1,若把0.01 mol的NaOH固体溶解于95℃水中配成1 L溶液,则溶液的pH为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com